Какими антибиотиками лечат стрептококковую инфекцию у
Обновлено: 13.05.2024
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор раздела: Трубачева Елена Сергеевна, врач – клинический фармаколог, более 15 лет занимающаяся практическими вопросами лечения и профилактики внутрибольничных инфекций и эпидемиологического надзора. Автор множества печатных работ на указанную тематику.
"Идея "Азбуки антибиотиков" вынашивалась в течение трех лет как способ донести сложные вещи максимально понятным языком для тех, кто только начинает постигать этот действительно сложный раздел практической медицины, и дать импульс к дальнейшему изучению, не продираясь через дебри терминологии и смежных дисциплин, теряя интерес по дороге."
Тема эта очень узконаправленная, и вопрос в том, насколько она может быть интересна широкому кругу читателей. Однако ради одних только отдаленных последствий заболеваний, вызванных S. agalactiae, ее стоит рассмотреть.
Стрептококки – это большая разнородная группа микроорганизмов, включающая следующие группы.
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Пневмококк, он же Streptococcus pneumoniae, является одним из основных возбудителей заболеваний верхних и нижних дыхательных путей. Однако проблема в том, что те же заболевания точно так же и с той же симптоматикой вызывает и множество вирусов, а потому микробиологическая диагностика буквально жизненно необходима, причем не когда-то там, а прямо здесь и сейчас.
В этой статье мы поговорим о более сложных темах на примерах тех представителей микробного мира, которые в большинстве случаев являются нашими добрыми соседями и очень редко, при очень специфических условиях, вызывают заболевания. Но так как лаборатории, особенно оснащенные автоматизированными системами детекции, все это определяют и буквально вываливают на врачей, ориентироваться и в этом море информации все-таки необходимо.
Информация о препаратах, отпускаемых по рецепту, размещенная на сайте, предназначена только для специалистов. Информация, содержащаяся на сайте, не должна использоваться пациентами для принятия самостоятельного решения о применении представленных лекарственных препаратов и не может служить заменой очной консультации врача.
Свидетельство о регистрации средства массовой информации Эл № ФС77-79153 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 15 сентября 2020 года.

Тонзиллофарингит является частым заболеванием в детском возрасте. Среди бактериальных возбудителей основную роль играет beta-гемолитический стрептококк группы А (БГСА). Установлено, что эффективность коротких курсов ряда антибиотиков сопоставима с 10-днев
Жалоба на боль в горле является одним из наиболее частых поводов для обращения за медицинской помощью к педиатру. Основной причиной боли в горле является воспаление небных миндалин и слизистой оболочки глотки — тонзиллофарингит. Данный термин широко используется в научной литературе, несмотря на то, что согласно Международной классификации болезней тонзиллит и фарингит являются отдельными нозологиями.
Ключевой проблемой антибактериальной терапии при тонзиллофарингитах у детей является определение показаний к ее назначению. Установлено, что чаще всего острый тонзиллофарингит является проявлением острой вирусной инфекции (ОРВИ) и, соответственно, не требует назначения антибактериальной терапии. Среди бактериальных возбудителей тонзиллофарингита у детей безусловным лидером является β-гемолитический стрептококк группы А (БГСА, Streptococcus pyogenes), на долю которого приходится 15–36% случаев острого тонзиллофарингита [1–3]. В 2012–2013 гг. мы обследовали 119 детей с острым тонзиллофарингитом с помощью экспресс-теста на БГСА с высокой диагностической точностью (Стрептатест), положительный результат получен у 19% больных.
Необходимость обязательного назначения антибактериальной терапии при стрептококковом тонзиллофарингите не вызывает сомнений. В систематическом обзоре Кокрановского сотрудничества (2013 г.), в который вошли десятки исследований (начиная с 1951 г.), было показано, что назначение антибиотиков при боли в горле существенно снижает вероятность осложнений — как поздних негнойных (острая ревматическая лихорадка), так и ранних гнойных (средний отит, синусит, паратонзиллярный абсцесс) [4].
Решение обозначенной проблемы кроется в своевременной верификации стрептококкового тонзиллофарингита. В многочисленных исследованиях показано, что внедрение методов экпресс-диагностики, обладающих высокой чувствительностью и специфичностью, позволяет непосредственно при осмотре всего за несколько минут пациента выявить заболевание, вызванное БГСА, дает возможность, с одной стороны, своевременно назначить антибактериальную терапию при стрептококковом тонзиллофарингите, а с другой стороны — значительно снизить частоту необоснованного назначения антибиотиков [5–6].
В то же время существует еще целый ряд актуальных проблем антибактериальной терапии при тонзиллофарингитах у детей, которые требуют обсуждения. Это проблемы, связанные с выбором антибактериального препарата, и режима его применения.
Бактерии рода Streptococcus, в том числе БГСА, не способны продуцировать β-лактамазы. Кроме того, данный возбудитель не обладает и другими механизмами резистентности к β-лактамным антибиотикам. До настоящего времени в мире не выделено ни одно штамма БГСА, резистентного к пенициллинам, цефалоспоринам и карбапенемам. Также возбудитель в 100% случаев сохраняет чувствительность к гликопептидам и оксазолидинонам. В то же время наблюдается резистентность БГСА к макролидам, линкозамидам, фениколам, тетрациклинам, фторхинолонам, сульфаниламидам [7].
В ходе многоцентровых российских исследований, проводившихся в 2001–2005 гг., была оценена резистентность более 1000 штаммов БГСА (табл. 1): выявлен очень высокий уровень резистентности БГСА к тетрациклинам, высокий к хлорамфениколу, небольшой уровень резистентности к 14- и 15-членным макролидам (менее 10%), минимальная резистентность к 16-членным макролидам и линкозамидам (менее 2%) и отсутствие резистентности к фторхинолонам [8].
Учитывая высокую стабильную активность пенициллина в отношении БГСА, этот антибиотик (феноксиметилпенициллин перорально, а также бензатинпенициллин внутримышечно) в течение многих лет рассматривается как препарат выбора для лечения стрептококкового тонзиллофарингита и в отечественных, и в зарубежных руководствах [9–12]. В ряде руководств в качестве препарата выбора также рассматривается амоксициллин [10–11].
Однако в 80-х годах XX века была выявлена серьезная проблема — нарастающая частота клинической и микробиологической неэффективности пенициллина при стрептококковом тонзиллофарингите, по данным отдельных исследований эрадикации БГСА не удавалось достичь у каждого четвертого пациента [13]. Вместе с тем было установлено, что другие антибиотики превосходят пенициллин по эффективности, в частности, если частота формирования носительства БГСА у детей после стрептококкового тонзиллофарингита при лечении пенициллином составила 11,3%, то при использовании макролидов и цефалоспоринов она была существенно меньше — 7,1% и 4,3% соответственно [14].
Изучение несоответствия эффективности пенициллина in vitro и in vivo при стрептококковом тонзиллофарингите позволило определить ключевую причину данного феномена — наличие в миндалинах у пациентов ко-патогенных бактерий (Bacteroides spp., Staphylococcus aureus и др.), которые продуцируют β-лактамазы и, соответственно, разрушают природные пенициллины и аминопенициллины [15–16]. Поэтому у пациентов, недавно получавших β-лактамные антибиотики, а также в случае рецидивирования тонзиллофарингита, в современных руководствах рекомендуется назначение препаратов, которые устойчивы к действию β-лактамаз, — ингибиторозащищенных аминопенициллинов и цефалоспоринов, а в отдельных случаях — линкозамидов [9–12].
Дополнительным фактором, ограничивающим применение пенициллина при тонзиллофарингите, является возможная аллергическая реакция на данный препарат, которая по данным различных исследований составляет от 1% до 20% случаев [17]. В случае аллергии на пенициллин рекомендуется применение макролидов или линкозамидов [9–11].
Суммированные рекомендации по антибактериальной терапии при стрептококковом тонзиллофарингите в современных руководствах можно представить в виде алгоритма (табл. 2).
Данный алгоритм основывается на двух основных факторах, определяющих выбор антибиотика. Однако в научной литературе представлены данные еще о ряде факторов, влияющих на эффективность антибактериальной терапии стрептококкового тонзиллофарингита. В частности, показано, что эффективность антибактериальной терапии зависит от частоты носительства штаммов бактерий, продуцирующих β-лактамазы, в целом в популяции, а не только у больных тонзиллофарингитом. В исследовании, проводившемся в течение года, была проанализирована по месяцам эффективность амоксициллина при стрептококковом тонзиллофарингите у детей и частота выявления в ротоглотке у здоровых детей штаммов бактерий, продуцирующих β-лактамазы. Частота неудач при использовании амоксициллина в течение года колебалась от 8% до 32%, и при этом прослеживалась очевидная корреляция с частотой носительства штаммов бактерий, продуцирующих β-лактамазы (рис. 1) [18].
В качестве одной из возможных причин неэффективности пенициллина при стрептококковом тонзиллофарингите рассматривается подавление пенициллинами α-гемолитических стрептококков, которые являются представителями нормальной микрофлоры ротоглотки и препятствуют колонизации БГСА [19].
Учитывая названные дополнительные факторы, влияющие на выбор антибактериального препарата, большой интерес представляет применение цефалоспоринов в лечении стрептококкового тонзиллофарингита у детей. Препараты данной группы устойчивы к действию многих β-лактамаз [20], они оказывают меньшее по сравнению с пенициллинами влияние на α-гемолитические стрептококки, что способствует более эффективной эрадикации БГСА [22, 23].
Данные 35 доказательных клинических исследований (более 7000 пациентов), оценивавших эффективности различных цефалоспоринов при стрептококковом тонзиллофарингите у детей, были обобщены в метаанализе. В анализировавшихся исследованиях сравнивался 10-дневный курс перорального цефалоспорина 1–3 поколения и перорального пенициллина. Данные метаанализа показали, что цефалоспорины значительно превосходят пенициллин по клинической и микробиологической эффективности (p < 0,00001) (рис. 2) [24].
Одним из препаратов, показавших существенно большую эффективность, чем пенициллин, является пероральный цефалоспорин III поколения цефиксим. В многоцентровом рандомизированном контролируемом исследовании было проведено сравнение эффективности и безопасности 10-дневных курсов цефиксима и пенициллина у 154 детей от 2 до 12 лет со стрептококковым тонзиллофарингитом. Клинический эффект был достигнут у всех пациентов. Микробиологическая эффективность составила 83% для группы детей, получавших цефиксим, и 77% — для группы детей, получавших пенициллин. Нежелательные явления в обеих группах были единичными [25]. В аналогичном рандомизированном исследовании, включавшем 110 детей со стрептококковым тонзиллофарингитом, микробиологическая эффективность цефиксима была существенно выше, чем у пенициллина, — 94% против 77% (p < 0,05) [26].
При стрептококковом тонзиллофарингите важно не только обеспечить выздоровление пациента от инфекционного заболевания, но и предотвратить развитие поздних осложнений и распространение инфекции. Поэтому целью антибактериальной терапии является эрадикация возбудителя. Проведенные исследования показали, что высокий уровень эрадикации достигается при использовании 10-дневного курса лечения пенициллином. Такая же длительность курса лечения рекомендуется и при использовании большинства других антибиотиков [10, 27]. Установлено, что в случае нарушения назначенной врачом длительности курса лечения пенициллином эффективность терапии при стрептококковом тонзиллофарингите снижается в среднем на 20% [28]. Еще более 50 лет назад были проведены исследования, которые показали, что назначенный 10-дневный курс лечения не выполняют подавляющее большинство больных. В одном исследовании было показано, что только 46% детей с тонзиллофарингитом продолжают получать пенициллиин на 3-й день терапии, 31% — на 6-й день и 8% — на 9-й день [29]. В аналогичном исследовании показатели были лучше: 81% пациентов принимали пенициллин на 5-й день лечения и 56% — на 9-й день. Авторы изучили факторы, которые влияют на выполнение рекомендаций врача. Было показано, что длительность курса терапии не зависела от возраста и пола ребенка, оцененной врачом тяжести заболевания и длительности сохранения симптомов. Одновременно было установлено, что на длительность лечения влияли оценка матерью тяжести состояния ребенка, назначение терапии врачом, длительно наблюдающим ребенка, или другим врачом, а также отношение матери к врачу [30].
Учитывая низкую комплаентность при 10-дневном курсе антибактериальной терапии тонзиллофарингита, а также неодинаковую эффективность различных антибиотиков, большой интерес представляют клинические исследования эффективности сокращенных курсов лечения стрептококкового тонзиллофарингита. В ряде исследований было показано, что 6-дневный курс амоксициллина, 4–5-дневный курс цефалоспоринов и 5-дневный курс азитромицина сопоставимы по эффективности с 10-дневным курсом пенициллина. При этом отмечен ряд преимуществ коротких курсов: более высокая комплаентность, меньшая частота нежелательных эффектов, лучшее отношение родителей пациента к лечению, снижение стоимости лечения [31]. В 2009 г. был опубликован систематический обзор Кокрановского сотрудничества, в котором проведено сравнение эффективности при остром стрептококковом тонзиллофарингите у детей коротких курсов антибактериальной терапии по сравнению с 10-дневным курсом пенициллина. В обзоре проанализированы 20 исследований, включавших более 13 000 пациентов. Короткие курсы более эффективных антибиотиков характеризовались более быстрым прекращением лихорадки и боли в горле. По частоте рецидивов тонзиллофарингита 10-дневный курс пенициллина и короткий курс других исследованных антибактериальных препаратов не имели достоверных отличий [32].
Одним из препаратов, эффективность короткого курса которого доказана при стрептококковом фарингите, также является цефиксим. В рандомизированном исследовании, включавшем 160 детей со стрептококковой ангиной, сравнивалась эффективность 5-дневного курса цефиксима и 10-дневного курса пенициллина. Клиническая эффективность была достигнута у 96% пациентов, которые лечились цефиксимом, и у 97,4% пациентов, получавших пенициллин, эрадикация БГСА достигнута соответственно у 82,8% и 88,2% детей. В течение 4 недель после окончания лечения рецидивы заболевания отмечены у 6 пациентов, получавших цефиксим, и у 8 пациентов, получавших пенициллин. В целом достоверных отличий результатов лечения в исследуемых группах не выявлено, что позволило авторам сделать вывод о сопоставимой эффективности короткого курса цефиксима и стандартного курса пенициллина [33]. Важной фармакокинетической особенностью цефиксима является относительно длительный период полувыведения, который позволяет принимать препарат 1 раз в сутки [34], что способствует повышению приверженности к лечению.
В нашей клинике был обобщен опыт применения цефиксима (Супракс®) с оценкой клинической эффективности и безопасности в качестве препарата эмпирической терапии при инфекции дыхательных путей у детей в возрасте от 1 до 12 лет, в том числе у пациентов с острым тонзиллитом и обострением хронического тонзиллита. У всех детей с тонзиллитом была отмечена быстрая положительная динамика. В целом в исследовании была отмечена хорошая переносимость цефиксима — у 8,3% больных отмечены нежелательные явления в виде легкой диареи, которая не требовала отмены препарата [34].
Цефалоспорин III поколения для перорального применения цефиксим обладает высокой активностью в отношении многих клинически значимых грамположительных и грамотрицательных бактерий. Хорошая биодоступность препарата после приема внутрь (около 50%) позволяет создать высокую сывороточную концентрацию и эффективные концентрации в тканях. Проведенные исследования свидетельствуют о высокой эффективности цефиксима при тонзиллофарингите, препарат входит в Стандарт Министерства здравоохранения Российской Федерации по оказанию первичной медико-санитарной помощи при остром тонзиллите у детей и взрослых в амбулаторных условиях [35]. На российском фармацевтическом рынке представлен оригинальный препарат цефиксима — Супракс®, который выпускается в виде гранул для приготовления суспензии, диспергируемых таблеток и капсул, что дает возможность использовать его у детей начиная с раннего возраста.
Литература
И. А. Дронов 1 , кандидат медицинских наук
Н. А. Геппе, доктор медицинских наук, профессор
У. С. Малявина, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва
Abstract. Tonsillitis-pharyngitis is frequent childish disease. Among pathogenic bacteria the main role plays A group β-hemolytic streptococcus (GAS). Effectiveness of short courses of treatment with antibiotics may be compared with 10-days course of treatment with penicillin. Clinical trial showed that oral intake of III generation cephalosporin — cefixime is highly efficient with children with streptococcus tonsillitis-pharyngitis including treatment by short courses.

Род бактерий, относящихся к условно патогенной микрофлоре. Носителями различных стрептококков являются практически все люди, включая младенцев. В норме активность микробов подавляет иммунитет. При ослаблении его защиты или получении извне большой заражающей дозы развиваются стрептококковые инфекции: воспалительные заболевания, поражающие слизистые дыхательных путей, ткани внутренних органов, зубы или оболочки мозга. Стрептококки очень устойчивы к факторам внешней среды, способны вырабатывать резистентность к антибактериальным препаратам.
Что такое стрептококки
Род Streptococcus объединяет разнообразные грамположительные микроорганизмы, способные размножаться в анаэробных условиях. Бактерии имеют шаровидную форму, их оболочки чрезвычайно устойчивы к агрессии внешней среды. В высушенных образцах биологических материалов стрептококки сохраняются жизнеспособными более года. Погибают при кипячении, химические дезинфицирующие препараты убивают их в течение 20 минут. По этой причине поверхностного антисептирования часто бывает недостаточно.
Источник распространения стрептококков — носители: зараженные или больные люди. В большой концентрации инфекция содержится на поверхности слизистых оболочек, в жидкостных выделениях: гное, экссудате, слюне. Микробы передаются от человека к человеку воздушно-капельным путем при чихании или кашле. В отличие от вирусов стрептококки разлетаются на относительно небольшое расстояние от источника: в радиусе не более трех метров. Высокая устойчивость бактерий во внешней среде определяет также алиментарный путь заражения: через грязные руки, продукты питания. Стрептококки длительное время сохраняются в молоке, мясных и морепродуктах, которые являются для этой группы инфекций питательную среду.
При размножении в организме человека стрептококки провоцируют интенсивные воспалительные реакции:
микробы группы А чаще поражают слизистые носа, ротовой полости, гортани, бронхов и легких, слухового аппарата, кожи, становятся возбудителями синуситов, тонзиллита, кариеса, ангины, пневмонии, дерматитов, рожи, скарлатины, осложнения ран и ожогов;
стрептококки группы В обычно провоцируют воспаления тканей мочевыделительной системы, суставных структур, соединительной ткани, вызывают цистит, адрекситы, инфекционные нефриты, ревматические процессы, послеродовые осложнения у женщин, эти микробы могут передаваться при половых контактах.
Развитию стрептококковых инфекций способствуют различные системные патологии и повреждения тканей. В том числе: сахарный диабет, злокачественные опухоли, иммунодефицитные, послеоперационные состояния, гиповитаминозы, открытые раны.
Признаки инфицирования
Распространенные симптомы стрептококковых инфекций:
повышение местной или общей температуры тела;
зуд, жжение, сухость в области гортани;
отечность и покраснение миндалин, образование желтого или сероватого налета на слизистых;
заложенность носа с последующими густыми выделениями зеленоватого или желтого цвета;
резкая боль и заложенность слухового прохода, серозные выделения с примесью гноя.
У большинства людей природная высокая склонность к заражению стрептококками. При передаче того или иного вида инфекции воспаляются так называемые входные ворота. Возникают ларингит, фарингит, ангина, отит. При распространении микробов из очагов заражения страдают нижние дыхательные пути, мозг, почки, кишечник и другие органы. К инфекциям вторичной формы можно отнести процессы с включением аутоиммунных механизмов: ревматоидный артрит, стрептококковый васкулит, гломерулонефрит.
Стрептококки — частые провокаторы токсических и некротических осложнений, в том числе тяжелой лихорадки, абсцессов и сепсиса.
Диагностика и лечение стрептококковых инфекций
Специфическая диагностика патогенов требует проведения бактериологического анализа соскобов слизистых, образцов слюны, мочи, мокроты, гнойного отделяемого и других биоматериалов. Кроме того, часто бывает необходимо тестирование крови на антитела к стрептококкам. Лабораторные исследования устанавливают вид возбудителя болезни в течение 20–30 минут.
Кроме этиологических анализов при различных патологиях требуется диагностика общего состояния поражениях органов: обследование у отоларинголога, проведение УЗИ, флюорографии и некоторых других.
Тактику лечения подбирают с учетом выявленных нарушений и устойчивости микробов к медикаментам. Терапию проводят врачи различных профилей: гинекологи, терапевты, пульмонологи, дерматологи. Для подавления активности инфекционной микрофлоры больным назначают курс антибиотиков. Против стрептококков эффективны Азитромицин, Эритромицин,препараты из ряда фторхинолонов: Ципрофлоксацин, Левофлоксацин. Покупать и применять медикаменты важно по назначению врача. Самодеятельность в этом вопросе приводит к развитию суперинфекций. Терапию дополняют также иммуномодулирующими средствами.
Предотвратить развитие стрептококковых заболеваний помогают санитарные меры, закаливание, использование антисептических средств.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Возрастные ограничения 18+
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С., врач – клинический фармаколог
Микробиологические аспекты
S.pyogenes является грамположительным кокком, собранным в цепочки. В норме колонизирует глотку у 3% взрослых и 15-20% детей школьного возраста. Так что без клинической картины острого фарингита не надо хвататься за антибиотики, как собственно и что-то сеять вне обострений.
100% штаммов чувствительны к пенициллинам, при этом Резистентность к макролидам в Европе – от 2 до 32%, в США – 7%. У нас в связи с великой любовью к этой группе, особенно среди педиатров, скорее всего, как в Европе. То есть о макролидах в этой ситуации надо забыть, к тому же тем же азитромицином не получится создать необходимую экспозицию в связи с ограничениями по срокам применения.
Клинические аспекты
При всем вышеперечисленном БГСА – зверь страшный, и основная проблема в том, что страх к нему мы почти потеряли. Лирическое отступление on. Именно этот зверь был постоянной причиной хирургических инфекций и родильной горячки (послеродового сепсиса) в доантибиотиковую эру. А женщины, как вы помните, умирали от нее, как мухи, пока Земмельвейс не заставил врачей мыть руки (за что закончил в психушке), но они их хотя бы на руках таскать перестали. Но даже сейчас, не дай бог, хирургу со стрептококковой ангиной подойти к операционному столу, и к концу первых суток стрептококк организует очень больную и страшно воняющую проблему в конкретной послеоперационной ране. Лирическое отступление off.
Потому напомним, что S.pyogenes может вызывать следующие заболевания:
- Фарингиты
- Поражения кожи и мягких тканей – целлюлиты, эризипелоид, лимфангит, рожа
- Некротические миозиты и фасцииты
- Послеродовый сепсис
- Пневмонии
- Сепсис
- Бактериальные эндокардиты (раньше редко, все же ангины и скарлатины старая школа требовала лечить строго 14 дней и ампициллином в задницу: сейчас стали встречаться почаще – привет коротким курсам антибиотиков при лечении ангин)
- Действие токсинов запускают синдром токсического шока и скарлатину
- Аутоиммунное воздействие приводит к ревматическим лихорадкам, с последующими возможным формированием пороков сердца и острому гломерулонефриту
- Послеоперационные раневые инфекции первых суток
Практические вопросы диагностики:
Микробиологическая диагностика S.pyogenes не представляет никакого труда, здесь в прямом смысле достаточно покрасить мазок по Граму. Все упирается в организационные аспекты – пока мазок доберется до лаборатории, пока покрасят. Пока ответят, пациент успеет много раз осложнится, если это стрептококк, или выздороветь, если это был фарингит и вызвавший его вирус (все-таки до 60% фарингитов вызваны вирусами, а не бактериальной флорой). Не хотелось бы останавливаться подробно на каждом перечисленном заболевании, но не упомянуть о диагностике острого фарингита, которая чаще всего и запускает множество вторичных осложнений, мы не можем. Для облегчения диагностики острого существуют несколько диагностических шкал. Автору более всего симпатична шкала Мак-Айзека в виду максимальной простоты ее использования.
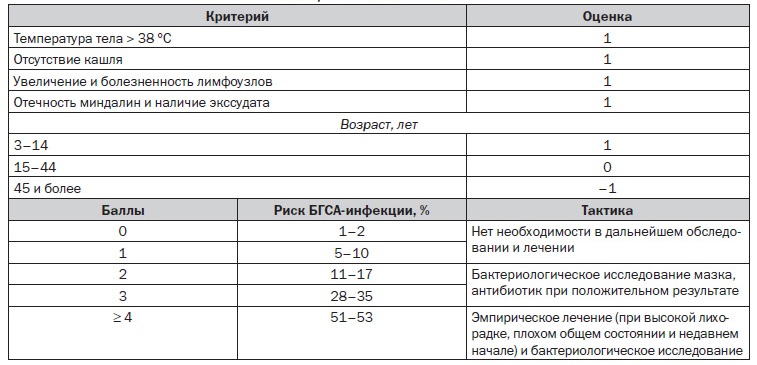
Но самым быстрым тестом для точной диагностики на месте является стрептатест, который в течение пяти минут дает ответ о вероятности наличия БГСА у больного с острым фарингитом.
Аспекты медикаментозного лечения
- Итак, мы определили, что имеем дело с БГСА, и тогда препаратами выбора в амбулаторной практике будут являться аминопенициллины, так как их много, они доступны, и главное, к ним 100% чувствительность у возбудителя.
Если ангина произошла впервые в жизни – лечим 10 дней. Если имеем дело с постоянными рецидивами – 14 дней, так как зверь может уйти во внутриклеточное состояние, оттуда руля процессом, и, чтобы до него добраться, доза должна быть выше средней, а курс лечения соответствующим.
Когда БГСА может уйти внутрь клетки? На тех самых пресловутых 5-7 днях, когда налеты с миндалин только сошли, температура только-только нормализовалась, а антибиотик взяли и отменили. И хорошо, если после подобного произойдет только рецидивирование фарингита, а не начнутся такие осложнения, как ревматизм, гломерулонефриты и далее по списку.
- Если пациент оказался в стационаре и ему обеспечен венозный доступ, то могут использоваться и пенициллины, и ампициллин в разных его вариациях. Главное – правильная доза, правильная кратность и ПРАВИЛЬНАЯ ДЛИТЕЛЬНОСТЬ КУРСА. Идеальный вариант из серии "дешево и сердито". Но обязательно должна быть доказанная микробиология.
При непереносимости пенициллинов помним о клиндамицине как об их адекватной замене.
- Пиогенный стрептококк, как мы выше упомянули, является причиной ранней послеоперационной раневой инфекции. Напомним, что стандартная послеоперационная раневая инфекция развивается к седьмым суткам. А если это произошло в первые сутки, да к тому же страшно завоняло (пиогенный стрептококк недаром называют мясоедным), немедленно делаем мазок, бежим с ним в лабораторию (можно даже своими ногами – это же ваш пациент осложнился, там так же бегом делают мазок по Граму, обнаруживают цепочки, и после этого начинаем лить аминопенициллин в вену, если не использовали его для периоперационной антибиотикопрофилактики (если использовали, то просто продолжаете дальше). Если совсем все бедно, можно пенициллин – 12 млн в сутки. Но если вы провели правильную периоперационную антибиотикопрофилактику, учли все риски и не забыли про свой личный стрептококк в горле, то риск ранней раневой минимален, а если профилактика продленная на 72 часа, то она и раскрутиться не успеет.
- При инфекциях кожи и мягких тканей, а также стрептококковом сепсисе препаратами выбора будут клиндамицин (который блокирует выработку токсических продуктов) в сочетании с пенициллином (24 млн ЕД в сутки) – это наиболее предпочтительная и малозатратная комбинация
Альтернативой в режиме монотерапии могут служить:
-
600 мг в/в каждые 6 часов 2,0 каждые шесть часов 2-3 г в/в каждые 6 часов или цефтриаксон по 2 г в сутки внутривенно в расчете 15 мг/кг в/в каждые 12 часов
Почему максимально важно соблюдать как дозировку, так и кратность введения читаем тут – /vracham/antibiotikoterapiya/polozheniya (часть 1 и часть 2).
В заключение хочется снова воскликнуть – пожалуйста, помните о пиогенном стрептококке и о правильной длительности его лечения.
Читайте также:

