Мрт при болезни лайма
Обновлено: 25.04.2024
Для цитирования: Елисеев Ю.В., Котов А.С., Котов С.В. Поздний нейросифилис (клинический случай). РМЖ. 2015;12:725.
Сифилис – это инфекция, передающаяся половым путем, возбудителем которой является Treponema pallidum. Сифилитическое поражение нервной системы является результатом хронического воспалительного процесса менингеальных оболочек. Проникновение в нервную систему происходит на ранних этапах нелеченного сифилиса. В последнее время наблюдается резкое увеличение заболеваемости сифилисом, особенно в крупных городах [9]. Этот факт заставил врачей повысить настороженность в отношении данного заболевания, особенно в популяции ВИЧ-инфицированных [3].
Нейросифилис диагностируется при повышении уровня лейкоцитов в ликворе до 20 клеток в мкл и позитивном результате VDRL-теста ликвора. Патогенез нейросифилиса аналогичен таковому сифилиса, протекающего в других системах организма, за мезенхимальным поражением следует паренхиматозное. Лица с патологией в ликворе, не получающие лечения, подвержены риску развития нейросифилиса с клиническими проявлениями. Поздними паренхиматозными формами сифилиса являются спинная сухотка, прогрессирующий паралич и их сочетание – табопаралич.
Спинная сухотка – медленно прогрессирующее паренхиматозное дегенеративное заболевание, вовлекающее задние столбы (демиелинизирующий процесс) и задние корешки (воспалительные изменения и фиброз) спинного мозга. Таким образом, неврологическими проявлениями данного заболевания являются: утрата болевой чувствительности, периферических рефлексов, снижение вибрационной чувствительности, мышечно-суставного чувства и прогрессирующая сенситивная атаксия [2].
Часто встречаются недержание мочи и утрата сексуальной функции. Стреляющие боли (внезапные, простреливающие, быстро распространяющиеся и исчезающие) являются ранним симптомом и требуют лечения. Тяжелые болевые (табетические) кризы после стресса или других воздействий встречаются у 90%, висцеральные кризы – у 15% пациентов. Они включают в себя мучительные боли в эпигастрии (кинжальные боли), сопровождающиеся тошнотой и рвотой.
Спинная сухотка стала редкостью, хотя в допенициллиновую эру она являлась основным клиническим проявлением нейросифилиса. При неврологическом осмотре у больного со спинной сухоткой можно выявить арефлексию, потерю глубокой чувствительности с проявлениями сенситивной атаксии, симптом Аргайла Робертсона. При этом зрачки равномерно сужены (миоз), нарушена реакция на свет при сохраненной реакции на конвергенцию с аккомодацией. Это обусловлено поражением в области, расположенной по соседству с ядром Вестфаля–Эдингера (околоводопроводное серое вещество среднего мозга). В редких случаях можно обнаружить этот симптом и у пациентов без нейросифилиса. К несифилитическим причинам симптома Аргайла Робертсона относят сахарный диабет, рассеянный склероз, энцефалопатию Вернике, болезнь Лайма, саркоидоз, опоясывающий лишай, опухоль и кровоизлияние в покрышку среднего мозга [5].
В задних столбах спинного мозга Treponema pallidum обнаружена не была, причины табетических изменений не ясны. Дебют клинических проявлений заболевания обычно возникает спустя 20–30 лет после инфицирования. Лечение малоэффективно, пенициллинотерапия не приводит к регрессу клинических проявлений, хотя может нормализовать показатели ликвора [1].
Прогрессирующий паралич иногда называют паралитической деменцией [6–8, 11]. Обычно заболевание развивается спустя 20–30 лет после заражения Treponema pallidum. Прогрессирующий паралич представляет собой хронический лобно-височный менингоэнцефалит с последующим снижением корковых функций [1].
Морфологически данное заболевание характеризуется периваскулярным и оболочечным воспалением с фиброзом мозговых оболочек, гранулематозным эпендиматитом, дегенерацией корковой паренхимы (атрофия и глиоз) и тканевым поражением Treponema pallidum [4]. Бляшки Фишера были описаны на поздних стадиях: это мелкие очаги демиелинизации в паренхиме головного мозга, преимущественно локализованные в лобной и теменной коре [10].
Начало психических проявлений может быть постепенным и отмечаться только близкими, а затем и самим пациентом. К ним относятся снижение интереса к работе, расстройства памяти, раздражительность, головокружение, апатия, снижение или потеря интереса к личной жизни. Позднее психические изменения становятся весьма разнообразными и могут мимикрировать под шизофрению, эйфорические мании, паранойю, токсические психозы или старческое слабоумие. Отметим, что старческая деменция чаще манифестирует с депрессии, расстройства сознания и тяжелого нарушения памяти и мышления.
Поздние стадии заболевания, наблюдаемые преимущественно спустя 5 лет от начала клинических проявлений, характеризуются деменцией, возможны эпилептические приступы с последующим исходом в вегетативное состояние и смерть.
Ликвор характеризуется лимфоцитарным плеоцитозом, повышением уровня белка, наличием специфических IgM и IgG, позитивным VDRL-тестом. VDRL-тест (Venereal Disease Research Laboratory) представляет собой современный вариант реакции Вассермана и используется в целях первичной диагностики врожденного и нейросифилиса.
В диагностике используется реакция иммунофлюоресценции с абсорбированным антигеном. Лечение включает пенициллин, эффективный при раннем назначении, в дальнейшем – только симптоматическую терапию.
Некоторые клинические проявления при прогрессивном параличе (простреливающая боль, проходящий гемипарез или сенсорный дефицит, парестезии, головная боль, атаксия) сходны с таковыми при рассеянном склерозе. Поведение пациента с прогрессирующим параличом может имитировать конверсионное, а не органическое расстройство.
Таким образом, к типичным нейропсихиатрическим проявлениям нейросифилиса относят делирий, манию, галлюцинации или психоз, деменцию и депрессию. Заболевание представлено комплексом меняющихся клинических проявлений [12]. Приводим клиническое наблюдение, которое может быть полезным практикующим врачам.
Клинический случай
При оценке соматического статуса данных, свидетельствующих о патологии, получено не было. АД 140/90 мм рт. ст. ЧСС 76 уд./мин. В неврологическом статусе: больная замкнута, контакт затруднен, дезориентация в пространстве и времени, анизокория за счет миоза слева, фотореакции отсутствуют, симптом Аргайла Робертсона. Парезов нет, мышечный тонус резко снижен во всех группах мышц, феномен переразгибания в коленных и локтевых суставах. Анизорефлексия коленных рефлексов, ахилловы рефлексы отсутствуют. Поверхностная чувствительность сохранена. Умеренное двустороннее нарушение суставно-мышечного чувства. При проверке вибрационной чувствительности градуированным камертоном – резкое снижение чувствительности на стопах до 2 баллов. Снижение когнитивных функций до уровня умеренных когнитивных нарушений по данным Монреальской шкалы оценки когнитивных функций – 22 балла. Батарея лобной дисфункции – 12 баллов.
Лабораторные данные общего и биохимического анализов крови и мочи не показали значимых нарушений. Однако скрининговый тест на сифилис оказался положительным. Развернутый анализ крови на сифилис резко положительный: РПГА с титрами 1/163840 и RPR 1/64. Анализ ликвора позволил установить диагноз позднего нейросифилиса. Сифилидологом МОККВД назначена стандартная внутривенная терапия пенициллином в объеме 20 млн единиц в сутки длительностью 10 дней.
В течение госпитального периода неоднократно отмечались преимущественно ночные приступы психического расстройства: психомоторное возбуждение, зрительные галлюцинации, бред преследования, агрессия, стремление покинуть лечебное учреждение. Больная консультирована психиатром, выявлены психоорганический синдром, выраженные интеллектуально-мнестические нарушения. Назначена комбинированная антипсихотическая терапия хлорпромазином и дифенгидрамином в стандартных суточных дозах.
На фоне проводимой терапии получен положительный клинический эффект в виде умеренного регресса когнитивных расстройств, продуктивной психиатрической симптоматики, также наблюдался положительный лабораторный эффект в виде снижения титров трепонемных тестов сыворотки крови. Больная переведена на амбулаторное лечение. Рекомендовано повторное ликворологическое обследование через 6 мес. для оценки эффективности проведенной терапии.
Представленный клинический пример иллюстрирует случай позднего нейросифилиса. Клинические данные характерны как для спинной сухотки, так и для прогрессирующего паралича. Полиморфизм клинических проявлений такого типа характерен для нейросифилиса, выделение изолированных форм спинной сухотки и прогрессивного паралича условно, основывается на преобладании тех или иных проявлений. Данный пример демонстрирует положение о необходимости ликворологического обследования всех пациентов, имеющих положительный результат нетрепонемных тестов в крови и процессуальное неврологическое заболевание. Только проведение ликворологического исследования позволяет диагностировать нейросифилис.
Своевременное назначение адекватной антибактериальной терапии – ключевой фактор благоприятного прогноза. Наши наблюдения показывают, что даже при выраженных нарушениях проведение адекватной пенициллинотерапии приводило к положительным сдвигам – уменьшению выраженности когнитивного дефицита, улучшению ходьбы, снижению выраженности атаксии. В некоторых случаях менинговаскулярного сифилиса с развитием ишемического инсульта пенициллинотерапия приводила к драматическому регрессу симптомов вплоть до полного возвращения гемипарезов и афатических расстройств.
- Елисеев Ю.В. Нейросифилис у лиц пожилого возраста // Клиническая геронтология. 2012. № 11. С. 66–70.
- Елисеев Ю.В., Котов С.В., Котов А.С. Спинная сухотка // Клиническая геронтология. 2014. № 7. С. 32–34.
- Chahine L.M., Khoriaty R.N., Tomford W.J., Hussain M.S. The changing face of neurosyphilis // Int. J. Stroke. 2011. Vol. 6(2). P. 136–143.
- Cintron R., Pachner A.R. Spirochetal diseases of the nervous system // Curr. Opin. Neurol. 1994. Vol. 7(3). P. 217–222.
- Dacso C.C., Bortz D.L. Significance of the Argyll Robertson pupil in clinical medicine // Am. J. Med. 1989. Vol. 86(2). P.199–202.
- Duffy J.D. General paralysis of the insane: neuropsychiatry's first challenge // J. Neuropsych. Clin. Neurosci. Spring 1995. Vol. 7(2). P. 243–249.
- Hutto B. Syphilis in clinical psychiatry: a review // Psychosomatics. 2001. Vol. 42(6). P. 453–460.
- Lair L., Naidech A.M. Modern neuropsychiatric presentation of neurosyphilis // Neurol. 2004. Vol. 63(7). P.1331–1333.
- Mattei P.L., Beachkofsky T.M., Gilson R.T., Wisco O.J. Syphilis: a reemerging infection // Am. Fam. Physician. 2012. Vol. 86(5). P. 433–440.
- Obi K., Tsuchiya K., Anno M. et al. Autopsy case of meningovascular neurosyphilis associated with Fischer's plaques // Brain Nerve. 2007. Vol. 59(7). P.797–803.
- Rundell J.R., Wise M.G. Neurosyphilis: a psychiatric perspective // Psychosomatics. 1985. Vol. 26(4). P. 287–290, 295.
- Yao Y., Huang E., Xie B., Cheng Y. Neurosyphilis presenting with psychotic symptoms and status epilepticus // Neurol. Sci. 2012. Vol. 33(1). P. 99–102.
Диагностика болезни Лайма по МРТ головного мозга
а) Терминология:
1. Сокращения:
• Болезнь Лайма (БЛ), нейроборрелиоз Лайма (НБЛ)
2. Определение:
• Мультисистемное воспалительное заболевание:
о Вызывается спирохетами Borrelia burgdorferi (различные подвиды в Европе)
о Передается при укусе твердотельного клеща
б) Визуализация:
2. КТ признаки болезни Лайма:
• Бесконтрастная КТ:
о Обычно изменений не выявляется
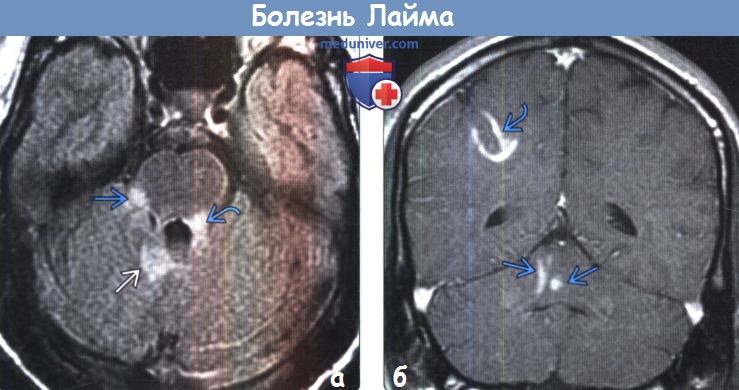
(а) MPT, FLAIR, аксиальный срез: у пациента с диагностированной серологически болезнью Лайма определяются множественные гиперинтенсивные очаги в левой верхней ножке мозжечка правых боковых отделах моста и мозжечке.
(б) МРТ, постконтрастное Т1-ВИ, корональный срез: у этого же пациента определяется контрастирование поражений, расположенных в белом веществе правого большого полушария, а также в структурах задней черепной ямки. Болезнь Лайма обычно проявляется в виде гиперинтенсивных на Т2-ВИ очагов, контрастного усиления нервных корешков или мозговых оболочек.
4. Рекомендации по визуализации:
• Совет по протоколу исследования:
о МРТ головного мозга (включая постконтрастные Т1-ВИ, ДВИ)
в) Дифференциальная диагностика:
1. Демиелинизирующее заболевание:
• Поражение БВ, зрительного нерва, спинного мозга, каллозо-септальной области более часто встречается при PC
2. Васкулит:
• Гиперинтенсивные на Т2-ВИ поражения ± сужение просвета артерий (ЦСА)
3. Саркоидоз:
• Мозговые оболочки, периваскулярные пространства, воронка гипофиза
г) Патология:
1. Общие характеристики болезни Лайма:
• Этиология:
о Спирохета Borrelia burgdorferi (США)
о Передается твердотельными клещами рода Ixodes
2. Микроскопия:
• Периваскулярныелимфоцитарные/плазмоцитарные инфильтраты:
о Эндо-/пери-/эпиневральные кровеносные сосуды
о Вызывают облитерирующий эндартериит
• Дегенерация аксонов
• Скопление лимфоцитов, плазматических клеток в вегетативных ганглиях
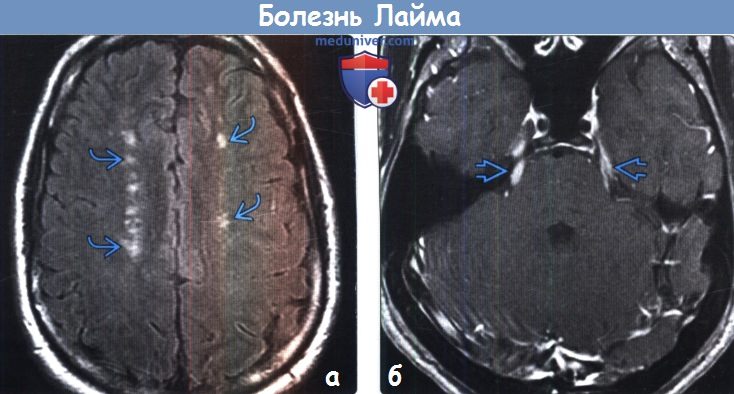
(а) MPT, FLAIR, аксиальный срез: у пациента с эпизодом укуса клеща в анамнезе и мигрирующей эритемой определяются множественные гиперинтенсивные очаги, расположенные в глубоком белом веществе. Повреждение БВ при болезни Лайма может напоминать множественные бляшки рассеянного склероза, хотя вовлечение каллозосептальной области встречается реже.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у мужчины 24 лет, который недавно занимался кемпингом, определяется контрастирование цистернальных сегментов обоих тройничных нервов. При нейроборрелиозе Лайма может наблюдаться контрастирование черепных нервов III, V и VII пар.
д) Клиническая картина:
2. Демография:
• Эпидемиология:
о Наиболее часто встречающееся трансмиссивное заболевание в США:
- Заболеваемость в США 9,7 случаев на 100000 человек
- Штаты северо-восточного побережья, Среднего Запада и Западные штаты
- Пик заболеваемости: с мая по июль
о Наиболее значимые резервуары: белохвостый олень/полевая мышь
3. Течение и прогноз:
• Прогрессирующее истощающее течение при отсутствии лечения на ранних стадиях
• У 10-15% пациентов при отсутствии лечения развиваются неврологические проявления
• У большинства пациентов восстановление происходит с сохранением минимального остаточного неврологического дефицита или без него
4. Лечение:
• Взрослые: доксициклин, тетрациклин, хлорамфеникол
• Дети: амоксициллин
• Кетолиды (новый, экспериментальный метод)
е) Диагностическая памятка. Обратите внимание:
• Предполагайте ИБЛ при выявлении PC-подобных поражений у пациента с мигрирующей эритемой:
о ± контрастирование черепных нервов, конского хвоста
• Учитывайте регион проживания, отдыха/путешествия пациента, время года
Болезнь Лайма - клещевой боррелиоз. Диагностика болезни Лайма.
Возбудителем болезни Лайма является спирохета Borrelia burgdorferi, переносимая иксодовыми клещами. Эндемичными районами болезни Лайма в США являются северо-восточное побережье от Массачусетса до Мэриленда (с особенно высокой концентрацией заболеваемости в Нью-Йорке), в среднезападной части страны — в Миннесоте и Висконсине, а также на побережье Тихого океана в Калифорнии и в Южном Орегоне. Выделяют три стадии болезни Лайма.
На первой стадии появляется мигрирующая эритема — увеличивающаяся в размерах кольцевидная эритема с просветлением в центре. Она возникает на месте укуса клеща в течение 3 дней — 1 месяца с момента укуса и может сопровождаться общими симптомами, включая головную боль, ригидность мышц шеи и признаки, характерные для острой респираторной инфекции. Вторая стадия характеризуется поражением сердца, мозговых оболочек (менингит), а также черепных и периферических нервов (нейропатии), корешков спинномозговых или черепных нервов (радикулопатии). Самым частым проявлением второй стадии болезни Лайма является менингит.
Его клиническая картина напоминает проявления вирусного менингита. Больные жалуются на головную боль, у них отмечаются менингеальные знаки, тошнота, рвота, невысокая лихорадка и светобоязнь. Наряду с этими симптомами может развиться односторонний или двусторонний паралич мимических мышц (поражение лицевого нерва) или симптоматика радикулопатии (парестезии и гиперстезии, иногда с фокальной мышечной слабостью).

На третьей стадии болезни Лайма (поздняя или хроническая стадия) развивается прогрессирующая энцефалопатия, которая характеризуется нарушением памяти, концентрации внимания и общей слабостью. В некоторых случаях наблюдается сенсомоторная аксональная полирадикулонейропатия. Изредка на поздних стадиях клещевого боррелиоза отмечается прогрессирующий энцефаломиелит. Единственным достоверным клиническим признаком болезни Лайма является мигрирующая эритема. К сожалению, этот признак наблюдается не у всех больных и поэтому часто болезнь остается нераспознанной. При подозрении на болезнь Лайма проводится стандартный серологический тест на антитела к Borellia Burgdorferi.
Большинство лабораторий используют иммуноферментный метод (ELISA). Основной проблемой лабораторной диагностики являются ложноположительные результаты. Причины данного явления следующие:
Результаты исследования одной и той же сыворотки могут быть разными, при проведении разными лабораториями. Поскольку методы диагностики не стандартизированы, рекомендовано проведение исследования только в лаборатории, которая имеет опыт работы с данным тестом. Положительный результат анализа может указывая только на состоявшуюся встречу с возбудителем, но не на активный процесс. Высокие титры антител к возбудителю обычно отмечаются у здоровых лиц, проживающих в эндемичном по боррелиозу районе. 2. Ложноположительные результаты анализов могут наблюдаться при ревматоидном артрите, лихорадке Скалистых Гор, инфекционном мононуклеозе, сифилисе, туберкулезном менингите и лептоспирозе.
При болезни Лайма часто обнаруживаются отклонения в составе ЦСЖ. Необходимо исследовать клеточный состав ЦСЖ, концентрацию глюкозы, белка и определять инт-ратекальный синтез антител к В. Burgdorferi Центры контроля заболеваемости США (Centers of Disease Control — CDC) разработали следующие критерии диагностики болезни Лайма: наличие мигрирующей эритемы диаметром не менее 5 см; по крайней мере одного из поздних признаков заболевания (со стороны нервной системы, сердца или суставов); а также данных лабораторной диагностики: выделения спирохеты из ЦСЖ, нарастания титров специфических антител в ЦСЖ или сыворотке крови больного. Однако большинство врачей склонны назначать специфическое лечение болезни Лайма при симптомах, не противоречащих этому заболеванию и анамнестических данных об укусе клеща.
- Вернуться в оглавление раздела "Неврология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
П оражение глаз при болезни Лайма считается достаточно редким явлением. Болезнь Лайма - мультисистемное инфекционное заболевание, вызываемое спирохетой Borrelia burgdorfery. Известно три группы боррелий: собственно B. burgdorfery, B. garinii, B. afzelii. В Европе боррелиоз может быть вызван любой из указанных спирохет. Спектр клинических проявлений болезни, называемой также боррелиозом Лайма, варьирует от явлений эритемы мигранс до артритов, неврологических и кардиологических расстройств. Первый случай внутриглазного боррелиоза был описан в 1985 г.
В 11% случаев на стадии ранней диссеминации инфекции у больных обнаруживаются явления конъюнктивита, однако на этой стадии больные редко попадают к окулисту. К ранним проявлениям относят также такие нейроофтальмологические расстройства, как парез окуломоторных нервов и неврит зрительного нерва, что связано с проникновением спирохет через гематоэнцефалический барьер уже через неделю после инфицирования. На поздних стадиях (через месяцы и годы после начала заболевания) развиваются кератиты и внутриглазные воспалительные поражения. При биомикроскопическом исследовании выявляются весьма необычные признаки, например, рубцовые инфильтраты роговицы, атипические парспланиты, витрииты по типу паутины, выраженные отеки диска зрительного нерва, изменения, подобные пигментному ретиниту. Многие изменения напоминают таковые при сифилитических поражениях глаза.
Глазной боррелиоз распознается крайне редко вследствие позднего появления симптомов и частых случаев серонегативной реакции ELISA.
Можно заподозрить боррелиоз в случае необычной клинической картины внутриглазного воспалительного процесса, но точный диагноз ставится с помощью иммуноблоттинга или путем обнаружения ДНК боррелии. Скрининг всех больных увеитом на предмет выявления боррелиозной этиологии процесса нецелесообразен. При кератитах возможно успешное применение антибиотиков per os, но при наличии пареза окуломоторных нервов и внутриглазных воспалительных изменений требуется назначение антибиотиков внутривенно. Обычно используют цефтриаксон (2 г/сут) или цефотаксим (6 г/сут). Передозировка цефтриаксона может привести к развитию осложнений со стороны желчевыделительной системы.
Karma A, Mikkila H. Ocular manifestations and treatment of Lyme disease. Current Opinion in Ophthalmology 1996;7(111):7-12.
НОВЫЕ ВОЗМОЖНОСТИ В ЛЕЧЕНИИ РЕТИНОБЛАСТОМЫ
И. Лоскутов
I. Loskutov
П рогноз для зрения и жизни больных с ретинобластомой значительно улучшился в последние десятилетия вследствие раннего выявления заболевания и совершенствования методов лечения. Сто лет назад ретинобластома почти всегда приводила к гибели больного. Ведение больного с ретинобластомой должно быть комплексным. Первой и главной целью лечения было и остается сохранение жизни больного, в известной степени вторичным оказывается вопрос сохранения глаза и зрения. Основными методами лечения данной опухоли являются: энуклеация глазного яблока, облучение, лазерное воздействие, криоаппликации, термотерапия, химиотерапия, хеморедукция, хемотермотерапия и экзентерация орбиты.
Проведение энуклеации показано при развитой стадии заболевания, а также при инвазии опухоли в зрительный нерв, хориоидею или орбиту. При вторичной глаукоме, вовлечении плоской части цилиарного тела или передней камеры также производится удаление глазного яблока.
Ретинобластома относится к опухолям, чувствительным к воздействию ионизирующего излучения. Результаты такого лечения во многом зависят от размеров и локализации опухоли, а также возникновения осложнений вследствие облучения (например, ретинопатии). Аргоновая или ксеноновая лазерная фотокоагуляция может быть успешно применена при лечении опухолей маленького размера, расположенных в заднем полюсе. Криотерапия используется для лечения маленьких опухолей, расположенных периферично к экватору.Термотерапия - метод воздействия на опухолевую ткань ультразвуком, микроволновым или инфракрасным излучением. Целью термотерапии является достижение температурного воздействия от 42 до 47 ° С, что ниже порога коагуляции. Комбинация термотерапии и химиотерапии определяется как хемотермотерапия, которая наиболее эффективна при опухолях, расположенных в заднем полюсе глазного яблока.
Хеморедукция - метод уменьшения объема опухолевой ткани для лучшей фокусировки последующего терапевтического воздействия, что делает его менее опасным.
Если заболевание распознано лишь в развитой стадии, на что указывает вовлечение тканей орбиты, то для спасения жизни больного необходимо проведение экзентерации орбиты с последующим курсом химиотерапии и облучения.
Shields C, Shields J, Potter P. New treatment modalities for retinoblastoma. Current Opinion in Ophthalmology 1996;7(111):20-6.
Для цитирования: Антелава О.А., Ушакова М.А., Ананьева Л.П. и др. Клиническая манифестация нейроинфекции при болезни Лайма на фоне иммуносупрессивной терапии. РМЖ. 2014;7:558.
Лайм-боррелиоз (ЛБ), или болезнь Лайма (Lyme disease), Лаймовский боррелиоз, или иксодовый клещевой боррелиоз – это инфекционное природно-очаговое трансмиссивное мультисистемное инфекционное полиорганное воспалительное заболевание, вызываемое спирохетами рода Borrelia, переносчиками которых являются иксодовые клещи. ЛБ характеризуется стадийностью, склонностью к хронизации и рецидивирующему течению [1].
Особое место в клинической картине болезни занимает поражение нервной системы, или нейроборрелиоз, частота выявления которого зависит от географической зоны, наблюдается в России у 10–60% больных [5]. Колебание в частоте его развития связано с особенностью геновидов боррелии и недостаточной изученностью проблемы в ряде регионов. Наиболее высокая частота поражения нервной системы наблюдается на Северо-Западе и в Центре России – 43–64%.
Широкий спектр клинических симптомов и синдромов при нейроборрелиозе объясняется способностью Воrreliа burgdorferi поражать все отделы нервной системы на любой стадии болезни [6, 7]. При нейроборрелиозе описаны:
- сенестонейропатии, нейропатии и радикулопатии;
- поражения черепно-мозговых нервов (ЧМН): моно(поли)неврит (лицевого, языкоглоточного, блуждающего нервов, зрительного, слухового нервов);
- синдром Банавартца (менингорадикулоневрит);
- периферические невриты, плексит. У 1/3 больных выявляется периферический судорожный синдром (тремор кистей рук и судороги в мышцах голеней);
- миелит;
- миелорадикулоневрит;
- лимфоцитарный менингит;
- очаговый или диффузный энцефалит;
- пароксизмальные расстройства сознания;
- эпилептические припадки, церебральный васкулит;
- прогрессирующий энцефаломиелит.
Хронический боррелиоз, или III стадия ЛБ, развивается у 10% больных через 6 мес. – 2 года после острого периода [8]. Наиболее изученными в этом периоде являются хронические неврологические синдромы, напоминающие по срокам развития третичный период нейросифилиса, названные хроническим нейроборрелиозом. При этом развиваются хронический энцефаломиелит, спастический парапарез, некоторые расстройства памяти, деменция, хроническая аксональная полирадикулопатия. Эта стадия характеризуется чередованием ремиссий и рецидивов, однако в некоторых случаях болезнь имеет непрерывно рецидивирующий характер.
Частота развития хронических форм нейроборрелиоза, по данным разных авторов, составляет от 4 до 20% всех больных ЛБ. Однако имеются данные о том, что реальный показатель может быть значительно выше и после перенесенной безэритематозной формы заболевания достигать 85% [9–11]. Считается, что диагностика этих форм заболевания затруднена в связи с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [12].
Для хронической нейроинфекции наиболее характерно постепенное поражение нервной системы с развитием патологического процесса, имитирующим другие нозологические формы, в частности рассеянный склероз, рассеянный энцефаломиелит. Большинство больных c хронической нейроинфекцией не указывают на предшествующую мигрирующую эритему или укус клеща. Полагают, что укусы самцов и незрелых особей клещей часто проходят незаметно для людей [13]. Кроме того, могут встречаться безэритематозные формы ЛБ в 2–20% случаев [14–15]. Известно, что в 6–8% случаев возможно субклиническое течение боррелиозной инфекции, при этом отсутствуют клинические проявления болезни. Отсутствие симптомов болезни не исключает развития в последующем II и III стадий заболевания. Все это является фактором риска развития хронической нейроинфекции, т. к. обусловливает отсроченную диагностику [16–18]. Латентный период инфекции при позднем нейроборрелиозе может составлять от 1,5 до 17 лет. Столь длительное латентное течение заболевания связывают с возможным переходом боррелии в неактивные L-формы с последующей их активацией [19–21].
Впервые хронический боррелиозный энцефаломиелит был описан R. Ackermann et al. в 1985 г. [23]. Позже была изучена группа из 44 больных, у которых встречались преимущественно церебральные проявления, напоминающие мультифокальный энцефалит, или спинальные симптомы. В настоящее время частота выявления энцефаломиелита при ЛБ невысока и составляет в среднем 4–5% от всех случаев нейроборрелиоза. Хроническое течение ЛБ в России изучено мало, что связано с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [24].
В литературе выделяют разные варианты течения нейроинфекции при хроническом ЛБ, включая прогрессирующий энцефаломиелит, хроническую радикулополиневропатию, хронический лимфоцитарный менингит, церебральный васкулит, энцефалопатию и др. Прогрессирующий энцефаломиелит при ЛБ нередко имитирует рассеянный склероз [25, 26]. Согласно наблюдению ряда исследователей, при хроническом ЛБ процесс носит генерализованный характер поражения нервной системы, несмотря на то, что клинически определяется изолированное поражение какого-либо нерва [27, 28]. Пo данным магнитно-резонансной томографии (МРТ) отмечаются поражения очагового характера преимущественно белого вещества головного мозга [29], которые могут определяться после длительного латентного периода.
Ведущие симптомы прогрессирующего боррелиозного энцефаломиелита – это спастические пара- и тетрапарезы, атаксия, дисфункция тазовых органов, когнитивные расстройства в виде снижения памяти и концентрации внимания. Больше чем у 50% больных ЛБ с поражением ЦНС наблюдаются сопутствующее поражение корешков и периферических нервов, множественные парезы черепных нервов, преимущественно вестибулокохлеарного.
Диагностические критерии хронической нейроинфекции включают:
- Наличие признаков поражения ЦНС при боррелиозе после перенесенных I и II стадий заболевания.
- Развитие неврологической симптоматики позднее 6 мес. от появления мигрирующей эритемы и/или факта присасывания клеща или сохранение симптоматики на протяжении более 6 мес.
- Обнаружение умеренных или высокоположительных титров антител к Borrelia burgdorferi в сыворотке крови больного при двукратном обследовании.
- Исключение другой этиологии патологического процесса, протекающего в нервной системе, который мог явиться причиной развития имеющейся у больного клинической симптоматики.
Поражение нервной системы на поздних стадиях ЛБ у 40% больных бывает изолированным и почти в 60% сочетается с экстраневрональными проявлениями ЛБ [6, 30]. Наиболее часто отмечаются поражения опорно-двигательного аппарата в виде артралгии, миалгии и других проявлений. В связи с развитием ревматических синдромов до 30% больных с ЛБ ежегодно обращаются к ревматологам.
Особая сложность диагностики наблюдается при отсроченном развитии поражения нервной системы, когда трудно определить связь развития поражения нервной системы с фактом присасывания клеща, особенно в случае безэритематозных форм. Также позитивность по антителам к Borrelia burgdorferi в ликворе выявляется только у 18% больных ЛБ [31–35].
В патогенезе хронического нейроборрелиоза играют роль проникновение инфекции и лимфоцитов в ткани нервной системы, чему способствуют активация или повреждение эндотелиальных клеток, нарастание уровня растворимой формы одной из основных клеточных молекул адгезии – ICAM-1, металлопротеиназы-9 [32]. В ряде исследований имеются доказательства развития аутоиммунных процессов в виде обнаружения антител, направленных против протеинов Borrelia burgdorferi и белков нервной ткани, вызывающих воспаление и демиелинизацию [33]. Высказывается предположение о возможном участии боррелии в инициации аутоиммунного процесса в результате активации миелин-специфичных Т-клеток и обнаружения аутореактивных антител к миелину и компонентам миелина при ЛБ [34]. По мере прогрессирования заболевания расширяется спектр антител ко многим белкам боррелии, что может приводить к перекрестному реагированию иммунной системы с антигенами боррелии и макроорганизма. Ведущая роль в этом отводится длительной персистенции возбудителя в тканях и его внутриклеточному расположению [35].
Комплексная оценка эпидемиологических, клинико-лабораторных и инструментальных данных, отражающих поражения нервной системы при хроническом ЛБ, демонстрирует отличие клинической картины хронической нейроинфекции в России от таковой в Европе в виде более частого поражения периферической нервной системы (радикулополиневропатии) и энцефалопатии, а также отсутствия сочетания полиневропатии с хроническим атрофическим акродерматитом.
Факторами риска развития хронического нейроборрелиоза названы: множественные присасывания клещей, отсутствие у больных мигрирующей эритемы на месте присасывания клеща в острый период ЛБ, раннее развитие признаков диссеминации, отсроченный и неполный курс лечения в острый период заболевания.
Спектр редких проявлений хронического нейроборрелиоза включает изолированное поражение черепных нервов, множественные мононевропатии, церебральный васкулит, синдромы паркинсонизма и бокового амиотрофического склероза, описан миастеноподобный синдром как проявление хронического ЛБ [36].
Представляют клинический интерес особенности течения хронической микст-инфекции ЛБ с клещевым энцефалитом и эрлихиозом, анаплазмозом. Так, в единичных случаях возможно хроническое течение клещевой микст-инфекции с характерными клинико-лабораторными проявлениями данных заболеваний. Показано, что в единичных случаях возможно хроническое течение клещевого энцефалита и ЛБ с типичными клиническими проявлениями последних. В случае возможной хронической микст-инфекции ЛБ и эрлихиоза по сравнению с изолированным течением ЛБ преобладает системность проявлений в сочетании с общеинфекционным синдромом и изменением лабораторных показателей крови (лейкопения, повышение уровня трансаминаз).
Диагностика и течение ЛБ в целом и нейроборрелиоза в частности при ревматических заболеваниях осложняется некоторым атипизмом клинический картины и скоростью прогрессирования ее проявлений, связанных со скомпрометированностью иммунной системы этой группы пациентов на фоне терапии высокими дозами глюкокортикоидов (ГК) и цитостатиками.
Клинический случай
Пациент Г., 1972 г. р. Анамнез болезни: считает себя больным с июля 2013 г., когда без объективной причины возникли повышение температуры до 37,4°С, параорбитальный отек, первые признаки мышечной слабости, утомляемость, боли в области правого тазобедренного сустава. При обследовании (июль 2013 г.) в общем анализе крови: гемоглобин – 148 г/л, скорость оседания эритроцитов (СОЭ) – 8 мм/ч, лейкопения – 2,82х109 (норма 4,0–9,0), тромбоцитопения, аспартатаминотрансфераза (АСТ) – 49 Ед/л (норма до 35 Ед/л), аланинаминотрансфераза (АЛТ) – 26,2 Ед/л, показатели креатинфосфокиназы (КФК) не исследовали. Белковые фракции: альбумины – 57,3%, (норма 55,7–66,1%), α1 – 6,3% (норма 2,9–11,8%), α2 – 9,1% (норма 7,1–11,8%), β1 – 5,5% (норма 4,7–7,2%), β2 – 5,9% (норма 3,2–6,5%), γ – 15,9% (норма 11,1–18,8%). Общий анализ мочи – без особенностей.
С августа 2013 г. – нарастание параорбитального отека, эритема на лице, груди (в зоне декольте), шее, лихорадка, общая слабость, утомляемость, появление признаков мышечной слабости преимущественно нижних конечностей. При обследовании в сентябре 2013 г. впервые выявлено повышение КФК до 841 Ед/л, лактатдегидрогеназы (ЛДГ) – до 657 Ед/л, креатинина – до 118 мкмоль/л (61–115), сохранялись тромбоцитопения (150х109) и лейкопения (2,8х109).
С учетом наличия в клинической картине параорбитального отека, эритемы на лице и в зоне декольте, проксимальной мышечной слабости, миопатических изменений по данным игольчатой электромиографии, повышения уровня КФК у больного диагностирован дерматомиозит (ДМ), начата терапия ГК в дозе 40 мг/сут, на фоне которой отмечены нормализация температуры тела и уменьшение отека вокруг глаз, снижение уровня КФК, АСТ, АЛТ, нормализации уровня лейкоцитов и тромбоцитов. Однако через 2 нед., на фоне быстрого снижения ГК, при достижении дозы преднизолона 30 мг/сут вновь отмечались возобновление лихорадки, усиление выраженности параорбитального отека, появление и нарастание признаков язвенно-некротического васкулита параорбитальной области (рис. 1 а, б). В связи с обострением заболевания и нарастанием признаков язвенно-некротического васкулита параорбитальной области было назначено повышение дозы ГК до 60 мг/сут, к терапии добавлен циклофосфамид 1000 мг в сочетании с метилпреднизолоном 500 мг в/в капельно 1 р./мес.
За период наблюдения пациенту проведен онкопоиск, включающий КТ грудной клетки, консультации специалистов, в т. ч. уролога – патологии не выявлено. Тогда же (до начала терапии циклофосфамидом в октябре 2013 г.) больному впервые выполнена МРТ головного мозга, каких-либо изменений не выявлено.
На фоне вышеуказанной терапии наблюдались: нормализация температуры тела, заживление язвенно-некротических изменений (рис. 2), нарастание мышечной силы, снижение КФК – 145 Ед/л, ЛДГ– 256 Ел/л, АСТ – 26 Ед/л, АЛТ – 35 Ед/л. Показатели гемоглобина и СОЭ, как и в начале заболевания, сохранялись в пределах нормы.
В январе 2014 г. проведена повторная МРТ головного мозга, при которой выявлено появление множественных инфильтративных очагов в кортикальном слое лобных областей, левой теменной области, супраорбитальный области, признаков отека мозга, нарушение гемодинамики (рис. 4 а–г).
Обращали на себя внимание высокие титры к Borrelia burgdorferi: IgМ – 45,0 Ед/мл (норма 12–17), IgG – 78,7 Ед/мл (до 15), однако исследование спинномозговой жидкости показало отрицательный результат.
Зараженность эрлихиозом и анаплазмозом исключена в лабораторном обследовании.
Таким образом, с учетом неоднократно подтвержденной в динамике позитивности по антителам к Borrelia burgdorferi при проведении как иммуноферментного анализа, так и методики иммуночипа, МРТ- и клинической картины очагового демиелинизирующего поражения ЦНС, факта пребывания пациента в течение более чем 2-х лет в эндемичном районе (в центре европейской части России) и после исключения других причин патологического процесса, протекающего в нервной системе, который мог бы явиться причиной развития имеющейся клинической симптоматики, у больного был диагностирован ЛБ III стадии с поражением нервной системы по типу нейроборрелиоза, наиболее вероятно в виде энцефаломиелита.
Полученные результаты обследования потребовали коррекции лечения: циклофосфамид был отменен, начато снижение дозы ГК и подключение антибактериальной терапии: цефтриаксон 4,0 г/сут в/в капельно № 30, а также ипидакрин 20 х 2 р./сут – 1 мес., тиоктовая кислота 600 мг/сут – 1 мес., витамин Е 400 мг/сут.
В настоящее время на фоне вышеуказанной антибактериальной терапии, приема преднизолона 40 мг/сут (снижение дозы продолжает) и отмены циклофосфамида отмечена стабилизация клинической картины, некоторое уменьшение выраженности амимии и признаков полинейропатии нижних конечностей.
Диагностическая и терапевтическая особенность ведения пациента обусловлена сложностью проведения дифференциальной диагностики. Так, с одной стороны, присутствие в клинической картине выраженного язвенно-некротического васкулита, энантемы, лихорадки, неоднократно выявляемых до лечения ГК лейкопении, тромбоцитопении, требовали исключения прежде всего системной красной волчанки, а также системного васкулита, однако отрицательные результаты анти-ДНК, антинуклеарного фактора, Sm, р-АNCA в иммунологическом анализе крови не позволили с уверенностью говорить об обсуждаемых диагнозах. С другой стороны, с учетом множественного прогрессирующего поражения головного мозга в круг дифференциального диагноза были включены рассеянный склероз и прогрессирующая мультифокальная лейкоэнцефалопатия. Последняя является прогрессирующим демиелинизирующим заболеванием ЦНС, вызываемым реактивацией латентно существующего JC-вируса семейства Papovaviridae, рода Polyomavirus и проявляющимся на фоне иммуносупрессии: СПИД, лимфомиелопролиферативные заболевания, злокачественные опухоли, трансплантация органов и аутоиммунные воспалительные заболевания [37]. При анализе клинико-лабораторной картины, данных анамнеза вопрос диагноза был решен в пользу ЛБ, о чем свидетельствовали картина МРТ-изменений (консультация по поводу результатов МРТ головного мозга в Центре неврологии, г. Москва), наличие высоких титров классов IgG и IgМ к Borrelia burgdorferi, а также клинически-положительная динамика неврологического статуса на фоне антибактериальной терапии.
Остается актуальным вопрос причинно-следственного диагноза. Можно ли рассматривать дебют ДМ как самостоятельный, с последующей манифестацией нейроинфекции на фоне иммуносупрессивной терапии? Или латентно протекающий ЛБ послужил триггером для ревматического заболевания?
Так, на сегодняшний день наиболее вероятным остается диагноз ДМ (параорбитальный отек, эритема в зоне декольте, на шее, язвенно-некротический васкулит, проксимальная мышечная слабость, первично-мышечные электромиографические изменения, повышение КФК).
Клещевой иксодовый боррелиоз (болезнь Лайма) III стадия: нейроборрелиоз, изменения ЦНС (по данным МРТ – очаговые изменения в кортикальном слое лобных областей, левой теменной области, супраорбитальной области), поражение ЧМН, периферическая полинейропатия; миопатический синдром, высокая серопозитивность по антителам к боррелиям классов IgG и IgМ.
Описанный случай интересен не только как клиническое наблюдение – манифестация латентно протекающего ранее ЛБ в виде быстропрогрессирующей нейроинфекции на фоне иммуносупрессивной терапии. Представляют интерес также широта дифференциально-диагностического поиска, осложненного некоторым атипизмом дебюта и течения ДМ, и начало наблюдения авторами за больным уже на фоне лечения ГК.
Читайте также:

