Острые респираторные инфекции ори
Обновлено: 25.04.2024
Острые респираторные инфекции (ОРИ) — это группа острых инфекционно-воспалительных заболеваний органов дыхания, развивающихся в результате аэрогенного инфицирования различными возбудителями (респираторными вирусами, бактериями, атипичными микроорганизмам
Вакцинопрофилактика ОРИ
В настоящее время не вызывает сомнений тот факт, что наиболее эффективным методом профилактики инфекционных заболеваний является активная специфическая иммунизация [8, 12]. Однако возможности вакцинопрофилактики респираторных инфекций существенно ограничены. Это обусловлено широким этиологическим спектром ОРИ (более 150 возбудителей), в то время как эффективные и безопасные вакцины разработаны лишь против нескольких респираторных патогенов, таких как вирус гриппа, гемофильная палочка (тип В) и пневмококк. Но, несмотря на столь ограниченный арсенал средств активной иммунизации против ОРИ, профилактический потенциал имеющихся вакцин должен быть использован максимально. Так противогриппозная вакцинация, широко проводимая в последние годы, позволила существенно уменьшить заболеваемость данной инфекцией среди привитых. При этом вводимая с 2006 г. обязательная противогриппозная иммунизация дошкольников и учеников 1–4 классов не только позволит снизить частоту гриппа среди вакцинированных, но и значительно ограничит распространение данной инфекции в организованных детских коллективах в целом [6].
Современные гриппозные вакцины являются тривакцинами, так как содержат штаммы (или их антигены) трех актуальных вирусов гриппа — А(Н1N1), A(H3N2) и В [8, 11, 12]. В России для иммунизации против гриппа у детей разрешены как живые, так и инактивированные вакцины (табл. 1). При этом живые вакцины используются только после достижения детьми 3-летнего возраста. Данный тип вакцин вводится интраназально — по 0,25 мл в каждый носовой ход, двукратно с интервалом 3–4 нед.
Среди инактивированных гриппозных вакцин различают цельновирионные, расщепленные и субъединичные. Цельновирионные вакцины содержат весь набор антигенов актуальных штаммов вируса гриппа. Иммуногенность цельновирионных вакцин высока, но из-за липидов вирусной оболочки, содержащихся в их составе, данные препараты более реактогенны. Цельновирионные гриппозные вакцины имеют существенные возрастные ограничения — их использование разрешено у детей старше 7 лет. Вакцины данного типа у детей вводятся только интраназально. При этом следует строго соблюдать рекомендованный режим дозирования — двукратное с интервалом 3–4 недели по 0,25 мл в каждый носовой ход. Следует отметить, что в последние годы цельновирионные гриппозные вакцины у детей используются редко.
Расщепленные гриппозные вакцины (сплит-вакцины) содержат поверхностные (гемагглютинин, нейраминидаза) и внутренние антигены, благодаря чему препараты характеризуются высокой иммуногенностью. При этом высокая степень очистки от реактогенных липидов определяет их хорошую переносимость. К расщепленным вакцинам относятся ваксигрип, бегривак, флюарикс. Большинство сплит-вакцин разрешены для использования у детей, начиная с 6-месячного возраста. Субъединичные гриппозные вакцины содержат только поверхностные антигены (гемагглютинин, нейраминидаза), что определяет хорошую иммуногенность и переносимость. К субъединичным вакцинам относятся гриппол, инфлювак, агриппал. Данные препараты, так же как и сплит-вакцины, разрешены для использования у детей с 6-месячного возраста. Следует отметить, что вакцинацию против гриппа необходимо проводить, строго придерживаясь международных рекомендаций по режиму дозирования. Так, иммунизация у детей первых 9 лет жизни, ранее не привитых и не болевших гриппом, должна проводиться двукратно с интервалом в 4 нед. При этом детям в возрасте от 6 мес до 3 лет 11 мес рекомендовано вводить по 0,25 мл вакцины, а начиная с 4-летнего возраста — по 0,5 мл.
Неспецифическая иммунопрофилактика и иммунотерапия ОРИ
Максимальное снижение заболеваемости ОРИ может быть достигнуто при сочетанном использовании вакцинации и средств неспецифической иммунопрофилактики (иммуномодуляторы). Для лечения и профилактики ОРИ в последние годы наиболее часто применяются такие иммуномодуляторы, как интерфероны, индукторы эндогенного интерферона и иммуномодуляторы бактериального происхождения. Кроме того, в комплексную систему неспецифической профилактики ОРИ входят фитоадаптогены с легким иммуномодулирующим эффектом (производные эхинации пурпурной, заманихи, корня солодки и т. д.) и поливитаминно-микроэлементные комплексы. Все реже в настоящее время используются препараты тимуса, а от введения с профилактической целью иммуноглобулинов (гамма-иммуноглобулинов) в последние годы отказались вообще.
Интерфероны. В течение нескольких десятилетий для лечения и профилактики респираторных инфекций у детей с успехом используются препараты интерферона, обладающие универсальным противовирусным эффектом. В результате воздействия интерферонов в клетках организма синтезируются ферменты, которые тормозят образование вирусных белков и разрушают вирусные рибонуклеиновые кислоты. Интерфероны также стимулируют экспрессию антигенов I и II классов главного комплекса гистосовместимости, что изменяет топографию клеточной мембраны, препятствует прикреплению вирусов к клеточной оболочке и нарушает их проникновение внутрь клеток. Кроме того, активизируя цитотоксическую активность Т-лимфоцитов, интерфероны стимулируют лизис клеток, инфицированных вирусами. Таким образом, интерфероны препятствуют вирусному инфицированию, а также подавляют репродукцию вирусов на стадии синтеза специфических белков [2, 7, 9]. Среди препаратов интерферона выделяют интерфероны природные (интерферон человеческий лейкоцитарный) и рекомбинатные (виферон, гриппферон и др.). При этом в последние годы для лечения и профилактики ОРИ все реже стали применять интерферон человеческий лейкоцитарный сухой и лейкинферон. В настоящее время предпочтение отдается рекомбинатным интерферонам (виферон, гриппферон). При этом наибольший опыт в педиатрической практике накоплен при использовании виферона — рекомбинатного интерферона α-2, обладающего также антиоксидантным эффектом за счет входящих в его состав витаминов С и Е. Наибольший терапевтический эффект от использования препаратов интерферона при лечении ОРИ достигается в тех случаях, когда этиология имеет вирусную или вирусно-бактериальную природу, а лечение начинается с первых часов заболевания [2, 7]. При этом включение данных препаратов в комплексную терапию ОРИ позволяет не только существенно уменьшить выраженность воспалительных процессов и продолжительность заболевания, но и снижает в целом риск развития осложнений.
Индукторы эндогенного интерферона. К химиотерапевтическим индукторам эндогенного интерферона относятся производные тилорона (амиксин), арбидол и циклоферон. Кроме того, эффектом усиления образования интерферона обладает анаферон — иммуномодулятор, содержащий сверхмалые дозы аффинно очищенных антител к гамма-интерферону человека. Имеются убедительные данные о профилактической и терапевтической эффективности данных лекарственных средств [2, 7, 9]. Следует отметить, что практически все представленные препараты не только индуцируют синтез эндогенного интерферона, но и обладают иммуномодулирующим эффектом (стимулируют фагоцитоз и клеточный иммунитет). При этом арбидол и амиксин оказывают также прямое ингибирующее действие на респираторные вирусы. При выборе конкретного препарата необходимо обращать внимание не только на его фармакологическую активность, но и на возрастные ограничения. Так анаферон разрешен к применению, начиная с 6-месячного возраста, арбидол может быть использован у детей старше 2 лет, в то время как амиксин и циклоферон имеют более жесткие возрастные ограничения [1, 10]. Циклоферон при этом разрешен у детей старше 4 лет, а амиксин (тилорон) — только у детей старше 7 лет. Особо следует подчеркнуть, что максимальная терапевтическая эффективность препаратов данного класса достигается в тех случаях, когда лечение начинается с первых часов заболевания.
Иммуномодуляторы бактериального происхождения в последние годы все шире используются для профилактики ОРИ, особенно у часто и длительно болеющих детей [3, 5, 7]. Терапевтическая эффективность и безопасность применяющихся у детей иммуномодуляторов бактериального происхождения подтверждена рядом контролируемых исследований. При этом различают следующие препараты: высокоочищенные бактериолизаты, мембранные фракции и рибосомально-протеогликановые комплексы. В свою очередь, среди высокоочищенных бактериолизатов выделяют препараты системного (бронхо-мунал, бронхо-ваксом) и топического действия (ирс 19, имудон). К препаратам, содержащим мембранные фракции бактериальной стенки, относится биостим, а также ликопид, в состав которого входит мурамилдипептид — синтетический аналог иммуноактивной части клеточной мембраны бактерий. Рибосомально-протеогликановые комплексы (рибомунил) содержат рибосомы определенных респираторных патогенов и мембранные факторы. В целом механизм действия всех иммуномодуляторов бактериального происхождения связан с их стимулирующим действием на фагоциты, повышением продукции интерферона и активацией естественных киллеров. Кроме того, ряд препаратов (бактериолизаты и рибосомально-протеогликановые комплексы) обладают легким вакцинирующим эффектом против тех возбудителей, антигены которых входят в их состав. При этом очень важно подчеркнуть, что благодаря этому поддерживается протекторная активность местного иммунитета (препараты потенцируют специфический иммунитет на слизистых). Учитывая тот факт, что в состав данных иммуномодуляторов входят антигены наиболее распространенных бактериальных возбудителей респираторных инфекций (пиогенный стрептококк, пневмококк, гемофильная палочка и т. д.), становится понятной их высокая профилактическая эффективность. Помимо этого, иммуномодуляторы бактериального происхождения обладают и терапевтическим эффектом, что позволяет назначать их короткими курсами во время ОРИ или при обострении хронических заболеваний ЛОР-органов. При этом отмечено, что данные препараты при одновременном использовании с антибиотиками потенцируют их антибактериальную активность. Установлено также, что иммуномодуляторы бактериального происхождения повышают иммуногенность вакцин, поэтому в последние годы, особенно у часто болеющих детей, плановую иммунизацию рекомендуют проводить на фоне приема данных препаратов [3, 7, 9].
В комплекс профилактических и терапевтических мероприятий при ОРИ может входить и назначение иммуномодуляторов растительного происхождения. Наиболее широко в последние годы в педиатрической практике стали использовать производные эхинацеи пурпурной (иммунал и др.). Эффективность препаратов эхинацеи пурпурной связывают с активацией неспецифического иммунитета. Иммунал назначают как для лечения неосложненных ОРИ (в течение 1 нед), так и для их профилактики (не более 8 нед). Иммунал (капли) назначают детям от 1 года до 4 лет — по 1 мл 3 раза в день, детям от 6 лет до 12 лет — по 1,5 мл 3 раза в день. При использовании иммунала в таблетках следует соблюдать следующий режим дозирования — детям от 4 до 6 лет — по 1 таблетке 1–2 раза в сутки, детям 6–1 2 лет — по 1 таблетке 1–3 раза в день [1, 10].
В последние годы иммуномодуляторы тимического происхождения, как природные (тималин, тактивин, тимоптин, тимактид, тимостимулин, вилозен), так и синтетические (тимоген) для профилактики и лечения ОРИ используются все реже. Это связано с тем, что корректное использование данных лекарственных средств требует предварительного иммунологического обследования и выявления убедительных данных о нарушении клеточного иммунитета. Иммуноглобулины, ранее широко используемые для профилактики и лечения ОРИ у детей, в настоящее время также применяются только по специальным показаниям. Назначение при данных состояниях иммуноглобулинов может быть оправдано лишь в тех случаях, когда заболевание приобретает тяжелое и осложненное течение, либо развивается на фоне выраженного иммунодефицитного состояния (агаммаглобулинемия, комбинированные иммунодефициты, общая вариабельная иммунная недостаточность, приобретенные гипогаммаглобулинемии на фоне нефротического синдрома, энтеропатий, хронического лимфолейкоза и др.). Предпочтение при этом должно отдаваться препаратам иммуноглобулина, которые предназначены для внутривенного введения (интраглобин, пентаглобин и др.).
Таким образом, в настоящее время в арсенале врачей-педиатров имеются высокоэффективные средства специфической и неспецифической иммунопрофилактики, рациональное использование которых позволяет не только существенно снизить заболеваемость ОРИ у детей, но и сократить риск развития тяжелых и осложненных форм заболевания.
Литература
А. Л. Заплатников, доктор медицинских наук, профессор
РМАПО, Москва
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
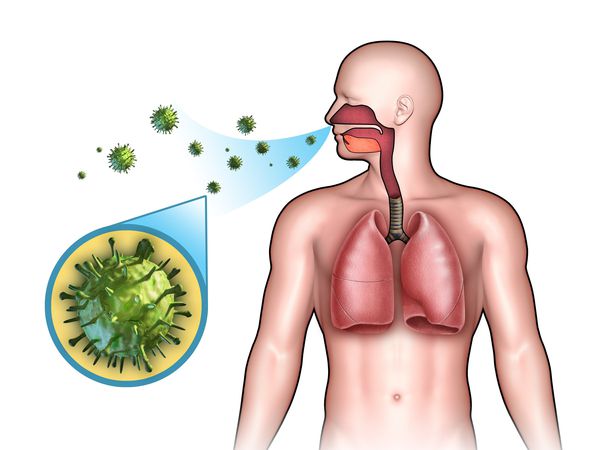
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
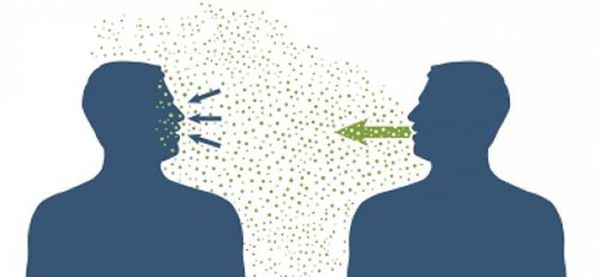
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
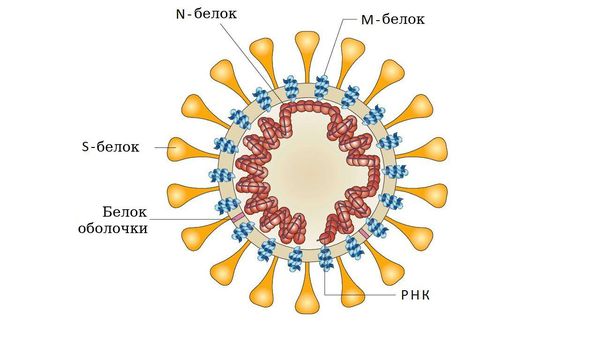
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
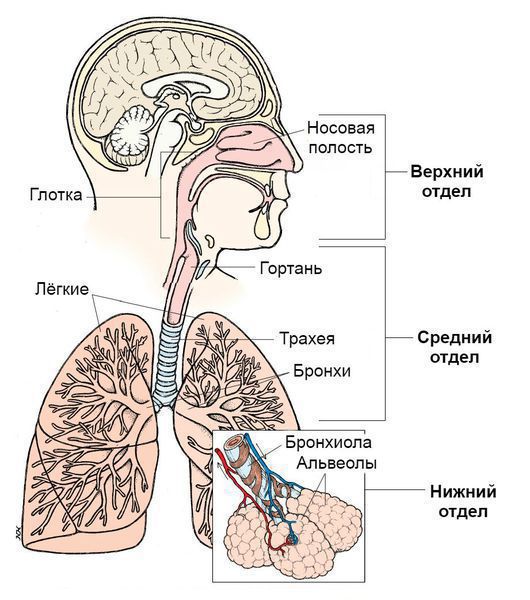
По вовлечению отдельных частей дыхательной системы:
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
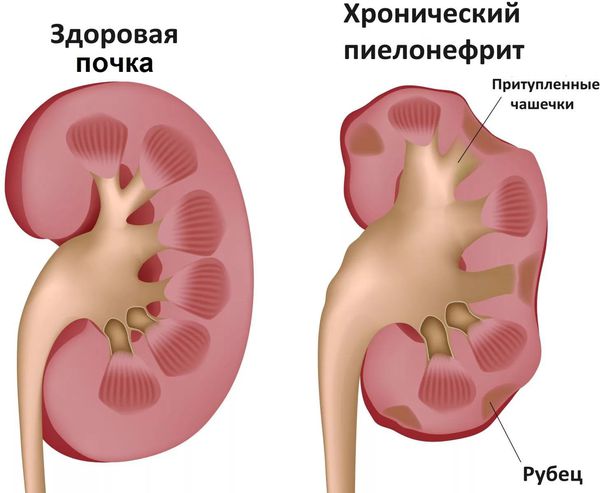
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
Что такое ОРВИ, ОРИ и ОРЗ?
Максимальная распространенность ОРИ в осенне-весенние, а также зимние месяцы чаще всего связана с переохлаждением, которое способствует развитию этих заболеваний. Группами высокого риска являются дети, люди преклонного возраста, беременные женщины, люди с хроническими болезнями сердца и лёгких.
Источником инфекции является заболевший человек. Передача инфекции происходит воздушно-капельным путем, а также через загрязненные руки или предметы, на которых находятся возбудители респираторных инфекций. Поэтому если в коллективе или семье кто-то один простыл, остальным тоже стоит поберечься.
Почему при простуде часто болит горло?
Роль фитопрепарата Тонзилгон Н при ОРЗ
Учитывая все свойства препарата Тонзилгон Н, его можно рекомендовать как в качестве самостоятельного лечения респираторных заболеваний верхних дыхательных путей, острого тонзиллофарингита, обострения хронического тонзиллита и фарингита у детей и взрослых, так и в составе комплексной терапии. Его лечебное и профилактическое воздействие на слизистую оболочку горла может быть полезным с целью предупреждения осложнений острых вирусных инфекций, особенно в непростых условиях пандемии COVID-19.
Что важно знать про Тонзилгон Н?
Как принимать Тонзилгон Н?
Применение Тонзилгона Н снижает вероятность осложнений ОРЗ и развития повторных простудных заболеваний. Препарат хорошо себя зарекомендовал и в лечении осложнившихся ОРВИ. Тонзилгон Н играет важную роль при лечении часто болеющих детей, посещающих дошкольные и школьные учреждения. Очень актуально его применение в осенне-весенний период, когда риск простудных заболеваний возрастает. Схема приёма препарата:
Как принимать детям
Как принимать взрослым
Противопоказаны детям до 2-х лет!
Дети от 2 до 5 лет – в острый период заболевания по 10 капель 5-6 раз в день, после уменьшения выраженности симптомов – по 10 капель 3 раза в день;
Дети от 6 до 11 лет – в острый период заболевания по 15 капель 5-6 раз в день, после уменьшения выраженности симптомов – по 15 капель 3 раза в день;
Дети старше 12 лет – в острый период заболевания по 25 капель 5-6 раз в день, после уменьшения выраженности симптомов – по 25 капель 3 раза в день.
В острый период заболевания по 25 капель 5-6 раз в день, после уменьшения выраженности симптомов – по 25 капель 3 раза в день.
Противопоказаны детям до 6-ти лет!
Дети от 6 до 11 лет – в острый период заболевания по 1 таблетке 5-6 раз в день, после уменьшения выраженности симптомов – по 1 таблетке 3 раза в день;
Дети старше 12 лет – в острый период заболевания по 2 таблетки 5-6 раз в день, после уменьшения выраженности симптомов – по 2 таблетке 3 раза в день.
В острый период заболевания по 2 таблетки 5-6 раз в день, после уменьшения выраженности симптомов – по 2 таблетке 3 раза в день.
Тонзилгон Н – это отличное средство от боли в горле и першения, которое к тому же позволяет предупредить осложнения при ОРЗ. Возьмите, чтобы не разболеться!
5. Острые респираторные инфекции и грипп. Профилактика.
6. О. А. Малявко. ОРИ. Что это такое?
7. Инструкция по медицинскому применению Тонзилгон Н для специалистов
Острые респираторные инфекции (ОРИ) по-прежнему занимают лидирующие позиции в структуре инфекционной патологии детского возраста. Основным этиологическим фактором ОРИ являются вирусы. Клинические симптомы ОРИ во многом схожи: повышение температуры тела, головная боль, гиперемия зева, насморк, кашель, конъюнктивит, увеличение регионарных лимфоузлов. Лечение пациентов с ОРИ должно быть комплексным и включать, при необходимости, противовирусные препараты. Идентификация конкретного вируса в настоящее время не является стандартной процедурой в повседневной клинической практике. Отдельные симптомы ОРИ могут быть выражены значительно, что требует назначения лекарственных препаратов. Лечение ОРВИ должно быть комплексным и включать: противовирусные этиотропные препараты; патогенетическую терапию; симптоматическую терапию; средства, усиливающие противовирусный и антибактериальный иммунный ответ; в случае развития бактериальных осложнений — антибактериальные средства. Поскольку ОРИ широко распространены и приводят к потере работоспособности, они относятся к социально значимым заболеваниям, требующим мер, обеспечивающих скорейшее выздоровление. Поэтому лекарственные средства, помогающие восстановить здоровье и работоспособность при ОРИ, приобретают соответствующую значимость. Однако в детском возрасте не все противовирусные препараты разрешены к применению, в частности, из-за возможного токсического действия. В этом случае целесообразно использовать препарат рекомбинантного интерферона альфа-2b в сочетании с высокоактивными антиоксидантами витаминами Е и С, клиническая эффективность и безопасность которого доказаны в многочисленных исследованиях.
Ключевые слова: острые респираторные инфекции, вирусы, дети, рекомбинантный интерферон альфа-2b.
Для цитирования: Николаева С.В., Хлыповка Ю.Н., Горелов А.В. Острые респираторные инфекции у детей: оптимизация тактики терапии. РМЖ. 2019;10:42-45.
Acute respiratory infections in children: optimizing treatment strategy
S.V. Nikolaeva 1 , Yu.N. Khlypovka 1,2 , A.V. Gorelov 2,3
1 Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow
2 Central Clinical Hospital and Polyclinic, Moscow
3 Sechenov University, Moscow
Acute respiratory infections (ARIs) still rank first among infectious diseases in children. Viruses are the most common causative agents of ARIs. Clinical symptoms of ARIs are similar, i.e., fever, headache, hyperemic pharynx, rhinitis, cough, conjunctivitis, and enlarged regional lymph nodes. Treatment for ARIs should be complex and include, if needed, antivirals. Current-ly, identification of a specific virus is not a standard procedure in routine clinical practice. Some symptoms of ARIs can be significant thus requiring additional drugs. Treatment for ARIs should include antivirals (etiological therapy), pathogenic and symptomatic therapy, medications to boost antiviral and antibacterial immune response, and antibiotics (if bacterial complications occur). Considering that ARIs are common disorders, drugs which reduce ARI duration and time to recover working capacity are socially important. However, not all antivirals can be used in children due to their potential toxicity. In these cases, recombinant interferon alfa-2b in combination with highly active antioxidants vitamins E and C is recommended. Numerous studies have demonstrated clinical efficacy and safety of this agent.
Keywords: acute respiratory infections, viruses, children, recombinant interferon alfa-2b.
For citation: Nikolaeva S.V., Khlypovka Yu.N., Gorelov A.V. Acute respiratory infections in children: optimizing treatment strategy. RMJ. 2019;10:42–45.
Статья посвящена вопросам оптимизации тактики терапии острых респираторных инфекций у детей
Актуальность
Основным этиологическим фактором ОРИ являются вирусы, немаловажную роль среди которых играют вирусы гриппа, риновирусы, респираторный синцитиальный вирус, аденовирусы, метапневмовирусы, коронавирусы, бокавирусы, а также вирусы парагриппа. Вирусы обладают выраженным тропизмом к эпителию слизистой оболочки дыхательных путей, что обусловливает высокую заболеваемость и быстрое распространение ОРИ. По нашим данным, на долю вирусных ОРИ в 2018–2019 гг. пришлось 87,5% всех случаев поражения дыхательных путей у детей. Доминирующим агентом являлся риновирус (в 14,8% случаев), бокавирус служил причиной ОРИ в 2% случаев, респираторно-синцитиальный вирус — в 9,1%. Грипп занимал одно из ведущих мест в этиологической структуре заболевших детей, его выявляли в 9,4% случаев. У 7,8% детей ОРИ имели сочетанный характер, при этом отмечались вирусно-вирусные и вирусно-бактериальные ассоциации (рис. 1).

В среднем дети переносят от 5 до 8 эпизодов ОРИ в год, большей частью — в легкой форме. Высокую частоту ОРИ можно объяснить значительным разнообразием возбудителей и высокой контагиозностью респираторных вирусов [2]. Помимо этого существует сложность идентификации возбудителей и способность микроорганизмов формировать устойчивость к лекарственным средствам. Все это способствует тому, что ОРИ вирусной этиологии часто носят массовый характер.
Особенности клиники ОРИ в зависимости от этиологии
Клинические симптомы ОРИ во многом схожи: повышение температуры, головная боль, гиперемия зева, насморк, кашель, конъюнктивит, увеличение регионарных лимфоузлов. Вместе с тем имеются некоторые особенности клинических проявлений, т. к. каждая группа респираторных вирусов имеет свои отличительные характеристики из-за преимущественной локализации поражения респираторного тракта (табл. 1). Так, при гриппе происходит поражение эпителия верхних (задняя стенка глотки), нижних (трахеобронхит) дыхательных путей, а также паренхимы легких (пневмония). При аденовирусной инфекции часто развиваются конъюнктивит, полиаденит, возможна гепатомегалия. При парагриппе у детей первых лет жизни чаще отмечается развитие обструктивного ларингита. Риновирус поражает эпителиальный покров носа с развитием ринита; в последние годы рассматривается связь перенесенной риновирусной инфекции с последующим развитием бронхиальной астмы. При респираторно-синцитиальной инфекции чаще развиваются бронхообструкция и бронхиолит [3, 4].
![Таблица 1. Основные клинические синдромы при гриппе и ОРВИ [5]](https://www.rmj.ru/upload/medialibrary/9df/42-2.jpg)
Идентификация конкретного вируса в настоящее время не является стандартной процедурой в повседневной клинической практике, и предположить, какова этиология этих инфекций, можно, учитывая сезон их возникновения, жалобы пациентов и данные физикального осмотра. Отдельные симптомы ОРИ могут быть выражены значительно, что требует применения лекарственных препаратов. Лечение ОРВИ должно быть комплексным и включать: противовирусные этиотропные препараты; патогенетическую терапию; симптоматическую терапию; средства, усиливающие противовирусный и антибактериальный иммунный ответ; в случае развития бактериальных осложнений — антибактериальные средства. В лечении ОРИ и гриппа используют широкий спектр противовирусных средств: 1) этиотропные препараты; 2) препараты интерферона; 3) индукторы интерферона; 4) гомеопатические препараты. Поскольку ОРИ — это широко распространенные заболевания с ежегодным охватом миллионов людей, любое лекарственное средство, ускоряющее выздоровление и восстановление работоспособности, чрезвычайно важно и приобретает социально значимый эффект.
Терапевтические возможности при ОРИ
В детском возрасте применение большинства противовирусных препаратов ограничено из-за их узкой специфичности, возможности вызывать побочные реакции, токсичности, возрастных ограничений. В этом случае у детей с ОРИ целесообразно применять лекарственные средства, не имеющие известных побочных действий, с доказанной эффективностью их применения у детей, в т. ч. детей раннего возраста. Таким препаратом, например, является рекомбинантный интерферон альфа-2b в сочетании с высокоактивными антиоксидантами витаминами Е и С (Виферон), успешное применение которого при гриппе и других ОРИ у детей доказано лечебной практикой. Препарат представлен в следующих лекарственных формах: свечи ректальные, мазь и гель для интраназального применения.
Одним из первых исследований по изучению эффективности препарата интерферона альфа-2b с антиоксидантами витаминами Е и С у детей при лечении ОРИ и гриппа было открытое сравнительное контролируемое рандомизированное исследование [6], проведенное в параллельных группах с участием 100 детей в возрасте от 4 мес. до 17 лет, госпитализированных в стационар по поводу ОРИ или гриппа. В группе детей, получавших препарат, наблюдались нормализация температуры тела, купирование интоксикации, исчезновение катаральных явлений и респираторного синдрома в среднем на 2 дня быстрее, чем в контрольной группе. Изучение показателей интерферонового статуса выявило способность препарата интерферона альфа-2b стимулировать активность иммунокомпетентных клеток к продукции α-ИФН и γ-ИФН и снижать уровень провоспалительных цитокинов (ИЛ-1β, ИЛ-8 и ФНО-α). Кроме того, на фоне приема препарата у большинства детей происходило восстановление исходно низкого в начале заболевания содержания sIgA в носовом секрете и сыворотке крови, а также статистически значимое снижение количества IgE в крови к моменту выздоровления (с 48,5±6,2 до 31,2±4,7 КЕ/л). Внутрибольничное инфицирование среди детей, получавших препарат, развивалось в среднем в 2 раза реже, чем в контрольной группе.
Эффективность различной противовирусной терапии (интерферон альфа-2b в суппозиториях ректальных и осельтамивир) изучали у 57 госпитализированных детей в возрасте от 6 мес. до 13 лет с гриппом и ОРИ в период пандемии 2009–2010 гг. [7]. Благодаря всасыванию через обильно кровоснабжаемую прямую кишку ректальные суппозитории оказывают быстрое действие, не перегружая желудок и печень. В первые сутки пребывания в стационаре дети были обследованы методом ПЦР на наличие вируса гриппа А/H1N1/sw, при этом данный вирус был выявлен у 28 (49,1%) детей. При анализе динамики клинических симптомов, вне зависимости от нозологической формы заболевания у детей, получавших препарат интерферона альфа-2b, была отмечена тенденция к уменьшению длительности кашля по сравнению с детьми, принимавшими осельтамивир (3,5±0,7 и 4,3±2,0 дня соответственно). Таким образом, применение рекомбинантного интерферона альфа-2b в терапии ОРИ и пандемического гриппа А/H1N1/sw эффективно, особенно у детей раннего возраста, что очень актуально в условиях возрастных ограничений многих противовирусных препаратов и в сезон массовой заболеваемости ОРИ и гриппом.
Еще в одном исследовании по изучению эффективности препарата интерферона альфа-2b в сочетании с витаминами Е и С приняли участие 277 детей [8], которых разделили на 3 группы по возрасту: I — от 1 года до 3 лет, II —
от 4 до 7 лет, III — от 8 до 14 лет. В каждой возрастной группе выделили 2 подгруппы. В основной подгруппе больные получали препарат интерферона альфа-2b в суппозиториях ректальных, в контрольной подгруппе — плацебо. Включение в терапию препарата оказывало положительное влияние на интерфероновый статус, корректировало пролиферацию цитотоксических клеток и естественных киллеров, способствовало повышению числа активированных Т-лимфоцитов и фагоцитов, а также усилению продукции IgA. Анализ интегрированных показателей выздоровления (балльный метод) показал, что у больных детей, получавших препарат интерферона альфа-2b в сочетании с антиоксидантным комплексом (витаминами Е и С), отмечалось более быстрое выздоровление.
При лечении ОРИ и гриппа целесообразно использование не только ректальных суппозиториев интерферона альфа-2b, но и местных лекарственных форм этого препарата (мазь, гель). И.Н. Захарова и соавт. провели сравнительное плацебо-контролируемое исследование клинико-иммунологической эффективности препарата интерферона альфа-2b в форме мази в комплексной терапии ОРИ у госпитализированных детей в возрасте от 1 года до 14 лет [9]. Препарат назначали интраназально 50 детям, вошедшим в основную группу, а в группе сравнения дети интраназально получали плацебо. В результате при применении мази с препаратом интерферона уменьшалась частота осложнений ОРИ (23,7 и 45% в группе сравнения соответственно), достоверно снижалась частота трансформации острого ринита в гнойный (7,9 и 20% в группе получавших плацебо, р≤0,01). Отмечена тенденция к сокращению длительности интоксикации, преобладанию критического варианта купирования лихорадки, уменьшению продолжительности и выраженности респираторного синдрома и сокращению сроков элиминации вирусов со слизистой оболочки носа. У детей, получавших препарат интерферона альфа-2b в форме мази, происходило увеличение индуцированной продукции α-интерферона в 2 раза, повышение уровня sIgА в смывах из носовой полости в ранние сроки заболевания, снижение уровня провоспалительного цитокина ИЛ-8. В группе сравнения таких изменений не выявлено.
Еще в одном клиническом исследовании по изучению терапевтической эффективности, безопасности и переносимости препарата интерферона альфа-2b в форме мази при лечении ОРИ и гриппа у детей приняли участие 100 пациентов в возрасте от 1 года до 9 лет 10 мес. [10]. Выявлено положительное влияние применения препарата на течение болезни: уменьшалась продолжительность катаральных симптомов, длительность сухого кашля, ускорялся переход сухого кашля во влажный, быстрее купировался токсикоз и нормализовалось общее состояние. Выявлен выраженный противовирусный эффект: происходила элиминация этиологически значимых вирусов в смывах из носоглотки у 91,6% детей, в то время как в группе контроля — только у 28%.
Еще одна форма препарата — гель — также эффективна в лечении гриппа и ОРИ. В открытом рандомизированном сравнительном клиническом исследовании, проведенном в 2011 г. [11] на базе отделения респираторных вирусных инфекций у детей ГУ НИИ гриппа РАМН, оценивали эффективность препарата интерферона альфа-2b геля у детей в возрасте от 4 мес. до 17 лет, госпитализированных в стационар с ОРИ. Методом случайной выборки были сформированы 2 группы по 50 человек. I группа получала препарат интерферона альфа-2b гель и симптоматическую терапию, а II (контрольная) группа получала только базисную симптоматическую терапию. Длительность терапии в обеих группах составила 7–10 дней. В этиологии заболевания, установленной у большинства детей основной (92%) и контрольной (82%) групп, доминировали вирусы гриппа и аденовирусы в виде моноинфекции или в сочетании, в ряде случаев обнаруживали более трех возбудителей. На фоне терапии препаратом интерферона альфа-2b гелем у детей наблюдалась статистически значимо более быстрая, чем в контрольной группе, нормализация температуры тела и купирование всех проявлений интоксикации и катарального синдрома. Было показано, что использование препарата интерферона альфа-2b в виде геля сокращает период присутствия вирусных антигенов в носоглотке пациентов. Так, уже через два дня после начала лечения у детей основной группы имело место статистически значимое сокращение числа повторного обнаружения вирусных антигенов в отличие от детей контрольной группы. Кроме того, в носовом секрете и в сыворотке крови у детей, получавших препарат интерферона альфа-2b, отмечалось повышение уровня секреторного IgA по сравнению с пациентами контрольной группы. Изучение показателей интерферонового статуса выявило умеренную способность геля к стимуляции выработки эндогенного интерферона (ИФН-α, ИФН-γ) к моменту выздоровления, что подтверждает иммуномодулирующее действие препарата. При изучении влияния препарата интерферона альфа-2b геля на динамику уровней провоспалительных цитокинов ИЛ-1β, ИЛ-8 и ФНО-α отмечена более быстрая их нормализация, повышение уровня ИЛ-1β практически не регистрировалось, тогда как в контрольной группе в 30% случаев выявлялось повышение уровня ИЛ-1β, сопровождавшееся более длительным течением заболевания. Кроме того, у большинства пациентов, получавших исследуемый препарат, наблюдались либо стабилизация, либо снижение уровня IgE по сравнению с исходным уровнем (с 53,3±6,5 до 37,3±4,9 КЕ/л) в отличие от детей контрольной группы.
Таким образом, применение препарата интерферона альфа-2b с антиоксидантами (витаминами Е и С) в комплексной терапии детей с ОРИ и гриппом приводит к более быстрому и выраженному купированию клинических проявлений заболевания, сокращению сроков выделения вирусных патогенов и более быстрой ликвидации иммунного дисбаланса, что позволяет рекомендовать интерферон альфа-2b для лечения ОРИ и гриппа у детей, в т. ч. детей раннего возраста.
Заключение
Таким образом, для каждой клинической ситуации и для каждого пациента в случае заболевания ОРИ или гриппом целесообразно использовать лекарственные препараты, действие которых направлено на уменьшение длительности заболевания и более легкое его течение. Причем необходимо учитывать все потенциальные риски и возможный исход, поскольку любое фармакологическое вмешательство оправдано только в том случае, если потенциальная польза превышает потенциальные риски применения препаратов. При принятии решения о назначении фармтерапии необходимо учитывать состояние больного, особенности болезни, риски потенциальных побочных эффектов лекарственных средств. В этом отношении препарат интерферона альфа-2b с витаминами Е и С отвечает требованиям эффективности и безопасности, а результаты исследований свидетельствуют о целесообразности его назначения при лечении ОРИ и гриппа у детей.
Авторы: Каннер Е.В. 1 , Горелов А.В. 1, 2 , Печкуров Д.В. 3 , Максимов М.Л. 4, 5, 6
1 ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия
2 ФГАОУ ВО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва
3 ФГБОУ ВО СамГМУ Минздрава России, Самара, Россия
4 ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
5 КГМА — филиал ФГБОУ ДПО РМАНПО Минздрава России, Казань, Россия
6 РНИМУ им. Н.И. Пирогова Минздрава России, Москва
Ключевые слова: острые респираторные инфекции, кишечные инфекции, вирусы, микст-инфекция
Для цитирования: Каннер Е.В., Горелов А.В., Печкуров Д.В., Максимов М.Л. Острые инфекции с сочетанным поражением дыхательной и пищеварительной систем: вызов современности. РМЖ. 2018;2(ll):84-89.
Acute infections with coexistent affection of the respiratory and digestive systems: the challenge of modernity
Kanner E.V. 1 , Gorelov A.V. 1,2 , Pechkurov D.V. 3 , Maksimov M.L. 4
1 Central Research Institute of Epidemiology of The Federal Service on Customers’ Rights Protection and Human Well-being Surveillance, Moscow
2 Sechenov University, Moscow
3 Samara State Medical University
4 Kazan State Medical Academy (branch of Russian Medical Academy of Сontinuous Postgraduate Education)
Acute respiratory (ARI) and acute enteric infections (AEI) rank first in the structure of morbidity and the economic losses in Russia and in the entire world. At the same time, the problem of the mortality of children from acute upper respiratory tract infections and their complications remains urgent.
The article presents current information on prevalence, epidemiology, clinical features, diagnosis of ARI.
Besides ARI pathogens which selectively affect the respiratory tract, recently attention has been paid to viruses that cause also the symptoms of the digestive system disorders, especially vomiting and diarrhea. On the other hand, at present, we know the AEI pathogens, which cause also the lesions of the respiratory tract. The article presents epidemiological and clinico-pathogenetic features concerning these ARI and AEI data.
Currently, the problem of diagnosis and treatment of coexistent infections in children remains very urgent. The diversity and discovery of new respiratory viruses, their variability, the rapid formation of strains resistant to antiviral agents and modifying adaptive immune responses in humans, lead to an increase in the frequency of viral mixed infections, which determines the need to develop and implement new diagnostic and treatment algorithms.
Key words: acute respiratory infections, enteric infections, viruses, mixed infection.
For citation: Kanner E.V., Gorelov A.V. Pechkurov D.V., Maksimov M.L. Acute infections with coexistent affection of the respiratory and digestive systems: the challenge of modernity // RMJ. 2018. № 2(II). P. 84–89.
Статья посвящена проблеме острых инфекций с сочетанным поражением дыхательной и пищеварительной систем. Приведены эпидемиологические и клинико-патогенетические особенности относительно данных респираторных и кишечных инфекций.
Введение
Возбудители и клиническая картина ори
Сочетанные инфекции
Антибиотико-ассоциированная диарея при ори
При ОРИ часто развивается диарея, которая связана с приемом лекарственных средств, прежде всего антибиотиков [17]. Антибиотико-ассоциированная диарея (ААД) может развиваться уже с первых дней приема антибактериального препарата и иметь тяжелое течение, особенно в тех случаях, когда ее этиологическим агентом являются токсинообразующие штаммы Clostridium difficile [89]. Развивается ААД, как правило, на фоне приема антибиотиков, в первые 3–5 дней, но в части случаев расстройство стула появляется в течение 1 сут после начала приема либо уже после их отмены, вплоть до 4 нед. [90, 91].
Частота ААД при приеме различных антибиотиков оценивается в 5–30%, а факторами, увеличивающими риск ее развития, являются применение антибиотиков, выводящихся с желчью, ранний (до 5 лет) или старший (более 65 лет) возраст, отягощенный преморбидный фон, особенно хронические заболевания ЖКТ, иммунная недостаточность, длительная госпитализация [92, 93]. Значительно увеличивает риск ААД одновременное или последовательное применение нескольких антибиотиков. Так, в одном из исследований показано, что при назначении комбинации амоксициллина и кларитромицина диарея развивалась у 36,8% детей [94].
Патогенетические механизмы ААД могут быть связаны как с нарушением биоценоза кишечника, так и непосредственно с побочными свойствами антибиотиков.
К первой группе относят воспаление стенки толстой кишки, вызванное воздействием токсинов Clostridium difficile, нарушение обмена желчных кислот, развитие вторичной панкреатической недостаточности, избыточную продукцию органических кислот, накопление в полости кишечника непереваренных осмотически активных компонентов, связанное с нарушением биоценоза кишечника, в т. ч. с избыточным бактериальным ростом в тонкой кишке [17, 94].
Ко второй группе относят мотилиноподобное действие макролидов, развитие билиарного сладж-синдрома на фоне приема цефтриаксона, токсическое действие тетрациклинов на слизистую оболочку кишечника.
Clostridium difficile являются определяющим фактором развития 15–20% случаев всех ААД, причем наиболее тяжелых ее форм, наличие этого микроорганизма повышает риск АДД в 3 раза [95, 96]. Эпидемиологическое значение имеют штаммы, продуцирующие токсины А и В. Энтеротоксин А повреждает слизистую оболочку кишки, инициируя развитие воспалительного процесса, и усиливает секрецию жидкости. Токсин В в 10 раз более токсичен, чем токсин А, и является фактором, необходимым для развития полной клинической картины заболевания, он активирует гликозилирование цитоплазматических белков энтероцитов, что приводит к морфологическим нарушениям, изменению клеточного давления, повышению проницаемости клеточной мембраны и гибели энтероцита [97, 98]. Наиболее тяжелой формой ААД, этиологически практически всегда связанной с клостридийной инфекцией, является псевдомембранозный колит.
Заключение
Таким образом, можно выделить 4 основных клинико-патогенетических варианта сочетанного поражения дыхательной и пищеварительной систем при остром инфекционном процессе:
развитие симптомов со стороны ЖКТ при ОРИ;
развитие симптомов со стороны ВДП при ОКИ, связанное с тропностью возбудителей к тканям обеих систем;
микст-инфицирование возбудителями респираторных и кишечных инфекций;
побочный эффект от лекарственной терапии ОРИ.
Очевидно, что при всех вариантах имеются как эпидемиологические, так и клинические особенности. В частности, это вопросы путей передачи возбудителя, способов профилактики, а в клиническом плане — комплексная оценка состояния больного с выделением ведущих клинических синдромов, оптимизация клинико-лабораторного обследования, рациональная терапия.
Читайте также:

