Паразит пульсирующие вакуоли бобовидный
Обновлено: 25.04.2024
Возбудитель малярии. Спорогония и шизогония
Возбудители малярии относятся к царству Animalia, подцарству Protozoa, типу Apicomplexa, классу Sporozoea, подклассу Coccidia, отряду Eucoccidiida, подотряду Haemosporina, роду Plasmodium. У человека в естественных условиях малярию вызывают 4 вида плазмодиев: P. vivax (Grassi et Feletti, 1890) Labbe, 1899 — возбудитель Р. vivaх-малярии, или трехдневной малярии; P. malariae (Laveran, 1881) Grassi et Feletti, 1890 — возбудитель четырехдневной малярии; P. falciparum (Laverania falcipara) Welch, 1897 — возбудитель тропической, или P. falciparum малярии; P. ovale Stephens, 1922 — возбудитель Р. ovale-малярии (типа трехдневной), отличающиеся по ряду экологических и биоморфологических параметров и клинико-эпидемиологической характеристике вызываемых ими заболеваний В пределах видов известны географические варианту расы и штаммы плазмодиев. В экспериментальных условиях возможно заражение человека оонозными видами плазмодиев обезьян (P. knowlesi, P. cynomolgi и др.).
При окраске по Романовскому — Giemsa у малярийных паразитов дифференцируют характерные для каждого вида ядро рубиново-красного цвета, цитоплазму голубого цвета, вакуоль и на некоторых стадиях развития — продукт паразитарного метаболизма гемоглобина - пигмент естественного золотисто-бурого цвета, что наряду с изменениями морфологии пораженных эритроцитов используется для идентификации возбудителей.
Шизогония. В организме человека малярийные паразиты последовательно проходят фазы тканевой (экзоэритроцитарной) и эритроцитарной шизогонии.
Тканевая шизогония протекает в гепатоцитах, в которые спорозоиты проникают из крови путем связывания циркумспорозоитных белков 2-го региона в качестве лигандов с гепарин-сульфатпротеогликанами и липопротеинами низкой плотности клеточной мембраны, выполняющих роль рецептора для паразитов. В гепатоцитах спорозоиты последовательно трансформируются в трофозоиты и шизонты, в результате деления последних образуются десятки тысяч (до 50 000 у P. falciparum) тканевых мерозоитов.

Эритроцитарная шизогония происходит циклически в эритроцитах различного возраста (Р vivax в незрелых и молодых эритроцитах, P. malariae — в старых, а Р. falciparum — в эритроцитах любого возраста). Поступившие из печени тканевые мерозоиты взаимодействуют с хемокинами — рецепторными белками эритроцитарной мембраны, в частности, P. falciparum с гликофоринами A (Aikawa M., Iseki М. и др , 1990), ретикулоцитсвязывающие протеины P. vivax — с белками системы Duffy — Fy" и Fyb(Miller L.H. и др.,1976), и, вызывая инвагинацию оболочки эритроцитов с образованием паразитофорной вакуоли, инвазируют эритроциты.
В них бесполые стадии паразитов развиваются (в течение 48 ч —P. vivax и P. falciparum, 50 ч —P. ovale и 72 ч — P. malariae) от стадии юного (кольцевидного, или ring-form) трофозоита до стадии зрелого шизонта с образованием после его деления эритроцитарных мерозоитов (от 6-8 у P. malariae до 32-40 у Р falciparum). Новое поколение эритроцитарных мерозоитов, взаимодействуя с комплементарными клеточными рецепторами, инвазируют новые эритроциты, где проходят очередной цикл эритроцитарной шизогонии.
Часть мерозоитов после проникновения в эритроциты трансформируется в них в незрелые половые стадии — микро- (мужские) и макро-(женские) гаметоциты (гаметоцитогония). При микроскопии крови больных P. vivax-,P. ovale- и четырехдневной малярией зрелые гаметоциты обнаруживаются уже в первые дни болезни и исчезают вскоре после прекращения эритроцитарной шизогонии. Напротив, гаметоциты P. falciparum созревают в течение 10-12 дней и сохраняются в периферической крови в течение 4-8 нед после исчезновения бесполых эритроцитарных стадий паразита.
Поэтому при микроскопии периферической крови больных неосложненной P.falciparum-малярией обнаруживаются лишь юные (кольцевидные) трофозоиты, а затем и гаметоциты. Промежуточные формы бесполых стадий этих плазмодиев обычно обнаруживаются в периферической крови при злокачественном, осложненном течении P.falciparum-малярии.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Бабезиоз (пироплазмоз, бабезиеллёз, babesiosis) - острое инфекционное заболевание человека и животных, характеризующееся интоксикацией, лихорадкой, развитием анемии и тяжелым прогрессирующим течением. Бабезиоз относится к трансмиссивным паразитарным зоонозным инфекциям. Заболевание у человека было впервые диагностировано в Югославии в 1957 году.
Болезни протекают с проявлениями лихорадки, анемии, желтухи, гемоглобинурии. Наибольшее ветеринарное значение имеют бабезиозы мелкого и крупного рогатого скота, а также собак. Возможно заболевание человека. Распространены на всех континентах, кроме Антарктики, в пределах ареалов переносчиков - нескольких видов пастбищных клещей. В России - в основном на северо-западе и юге Европейской части и в степных районах юга Сибири.
Из-за недостаточной изученности и различия мнений исследователей, часто бабезиоз отождествляют с пироплазмозом, что не вполне корректно из-за различий в этиологии возбудителей, а также клинической картины заболеваний. По Международной классификации болезней МКБ-10 бабезиоз человека имеет код B60.0.
Что провоцирует / Причины Бабезиоза:
Возбудитель бабезиоза относится к типу простейших, классу споровиков, семейству Babesiidae. Заболевание человека вызывают три вида бабезий: Babesia divergens, rodhaini - в Европе и Babesia micron в Америке. Бабезиоз животных вызывается также В. bovis и В. bigemina. Бабезии располагаются внутри пораженных эритроцитов в центре или по периферии клеток. При окраске по Граму имеют вид тонких колец диаметром 2-3 мкм или образований грушевидной формы диаметром 4-5 мкм.
В мировой литературе к настоящему времени описано всего около 100 случаев бабезиоза, большинство из которых закончилось летально. Манифестные формы заболевания развивались у лиц с резкими нарушениями иммунной системы, в частности после спленэктомии. Считается вероятной манифестация бабезиоза у ВИЧ-инфицированных. У людей с нормально функционирующей иммунной системой заболевание протекает бессимптомно, несмотря на наличие паразитемии, достигающей 1-2%.
Заболевание встречается в Европе (Скандинавские страны, Франция, ФРГ, Югославия, Польша) и в США (восточное побережье). Хозяином являются мыши-полевки и другие грызуны, собаки, кошки и крупный рогатый скот. Бабезиоз животных открыт в 1888 году В. Бабешем. Ежегодно только в Европе регистрируются десятки тысяч случаев заболевания домашних животных. Переносчик - широко распространенный пастбищный клещ Ixodes ricinus и аргасовые клещи. Возбудитель сохраняется в организме клещей пожизненно и может передаваться трансовариально. Заболевают туристы, сельхозяйственные рабочие, пастухи в период активности клещей (весенне-летний и летне-осенний сезоны). Возможна передача инфекции путем гемотрансфузий от инфицированных лиц, у которых имеется бессимптомная паразитемия.
Патогенез (что происходит?) во время Бабезиоза:
Патогенез бабезиоза изучен недостаточно.
Передаётся бабезиоз через укусы клещей почти всех родов семейства Ixodidae, наиболее известны как передатчики клещи родов Dermacentor, Rhipicephalus, Hyalomma. Передача происходит через слюну во время питания клеща.
Естественным резервуаром возбудителей в природе служат больные бабезиозом животные. Промежуточные резервуары - мелкие грызуны.
Переболевшие животные в течение 2- 3 лет невосприимчивы к повторному острому заражению. Во многих эндемичных районах заражено большинство или всё поголовье скота.
Симптомы Бабезиоза:
Продолжительность инкубационного периода при заражении Babesia divergens через клещей 10–15 суток, через кровь - 6–12 суток, при заражении овец Babesia ovis соответственно 8–12 и 5–7 суток. У больных животных резко повышается температура тела (до 40–41°C), нарушается работа сердца, учащается дыхание. Общее состояние угнетённое, запоры чередуются с поносами. Животные быстро худеют. Удои коров снижаются в 4–5 раз. Молоко становится жёлтым, иногда красноватым, горьким на вкус. На 2-3–й день болезни появляется кровавая моча. У овец часто наступает прерывание беременности. Продолжительность острого периода болезни 4–8 суток.
Летальность у крупного рогатого скота 40% и более, у овец и коз - до 80% от числа заболевших острой формой.
Бабезиоз у человека развивается в основном на фоне пониженного иммунного статуса (пожилые или перенёсшие тяжёлые операции, больные СПИДом). Случаи заболевания начали фиксировать лишь во второй половине 20–ого века, описано несколько десятков случаев заболевания. Высока вероятность недостаточного уровня диагностики этого заболевания у человека, для его повышения проводится значительная работа во многих странах. У человека с нормальной иммунной системой протекает бессимптомно, несмотря на высокую степень паразитемии (1–2%).
Осложнения. Бабезиоз закономерно осложняется острой почечной недостаточностью, острой почечно-печеночной и полиорганной недостаточностью. Присоединяющиеся неспецифические пневмонии ухудшают прогноз.
Диагностика Бабезиоза:
Клиническая диагностика затруднительна. Длительная лихорадка в сочетании с анемией, гепатомегалией при отсутствии эффекта от лечения с применением антибактериальных средств является основанием для лабораторных исследований на ба-безиоз. Особенно важен учет эпидемиологических данных (укусы клещей, пребывание в эндемичной местности) и выявление нарушений иммунного статуса у больного. Диагноз подтверждается паразитологиче-ски обнаружением возбудителя в мазке и толстой капле крови, а также в реакции непрямой иммунофлюоресценции. Диагностический титр при однократном исследовании не менее 1:256. Применяют также реакцию связывания комплемента.
При невысокой паразитемии иногда используют биологический метод, при котором кровь больного вводят спленэктомированным золотистым хомячкам. Спустя 2-4 нед у животных развивается заболевание и бабезий легко выявляются в мазке крови.
Дифференциальная диагностика проводится с тропической малярией, сепсисом, заболеваниями крови, ВИЧ-инфекцией, ГЛПС.
Лечение Бабезиоза:
Хороший лечебный эффект дают пироплазмил, беренил, гемоспоридин, акаприн, ихтарган, альбаргин, тиарген, наганин и др. Больным животным предоставляют полный покой (их нельзя перегонять), обеспечивают зелёными и сочными кормами.
Для тяжёлых форм бабезиоза у человека рекомендованы комбинации клиндамицина и хинина или азитромицина и атоваквона. В тяжёлых случаях необходимо переливание крови.
Прогноз. Без этиотропного лечения заболевание нередко (50-80% случаев) заканчивается летальным исходом. При своевременном начале антипаразитарной терапии прогноз благоприятный.
Профилактика Бабезиоза:
Специфическая профилактика не разработана.Уничтожение клещей и грызунов на пастбищах, обработка животных акарицидами. Для человека - применение противоклещевых препаратов.
К каким докторам следует обращаться если у Вас Бабезиоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Бабезиоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Что такое тениоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Тениоз (Taeniosis) — паразитарное заболевание человека, вызываемое половозрелой стадией ленточного гельминта (свиного цепня), который проникает в организм человека при употреблении плохо приготовленного мяса, паразитирует в тонком кишечнике и вызывает расстройства пищеварения. В некоторых случаях может осложняться цистицеркозом — паразитированием в тканях организма личинок свиного цепня, что приводит к серьёзным последствиям и даже смерти.
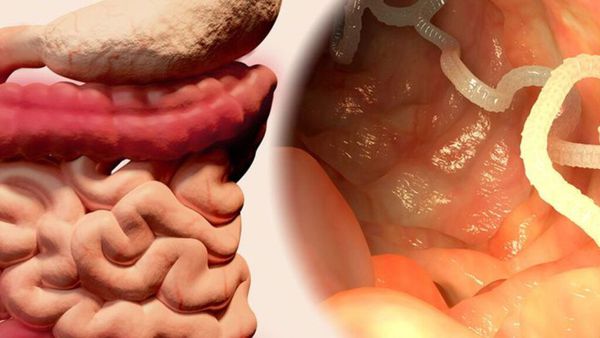
Возбудитель
- домен — эукариоты;
- царство — животные;
- тип — плоские черви;
- класс — ленточные черви;
- отряд — циклофиллиды;
- семейство — тенииды;
- род — Taenia;
- вид — свиной цепень (Taenia solium).
Свиной цепень (устаревшее название "cолитёр") — это плоский (ленточный) паразитический червь, длина которого в кишечнике человека достигает 3 метров, а по данным Ц ентра по контролю и профилактике заболеваний США (CDC) его длина может достигать 7 метров. Как правило, паразитирует только 1 червь. Паразит имеет головку, шейку и тело. Тело червя (стробила) состоит из члеников (п роглоттидов), их число может достигать 1000 . Головка (сколекс) размерами до 2 мм в диаметре имеет хоботок и 4 мышечные присоски (органы прикрепления), расположенные крестообразно. На хоботке есть крючья в количестве от 22 до 32, из-за этого есть второе название паразита — вооружённый цепень.
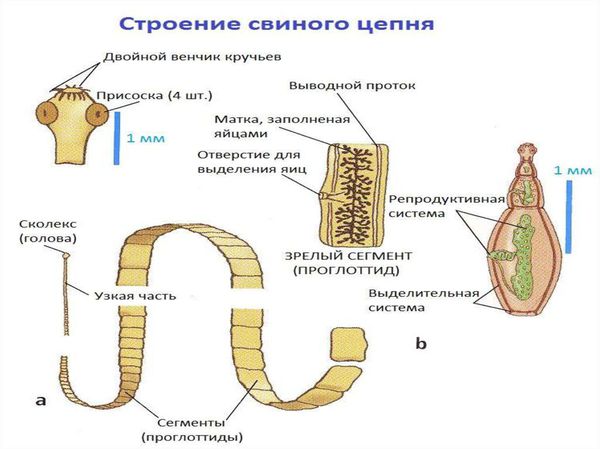
Яйца паразита попадают с калом человека в окружающую среду. Животные (свиньи, собаки, кошки и даже человек при несоблюдении гигиены) поедают яйца, зародыши проходят через кишечную стенку и разносятся кровью по всему организму, после чего оседают в тканях (в основном в соединительной ткани между мышцами). Через пару месяцев яйца превращаются в финны (цистицерки), которые живут до 5 лет, после чего они погибают и обызвествляются (накапливают минеральные вещества, соли кальция). Цистицерки имеют вид полупрозрачных беловатых пузырьков диаметром до 1,5 см, внутри видна мелкая сформированная головка.
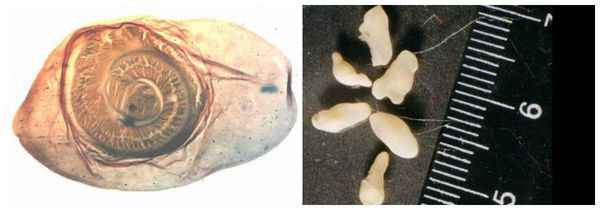
Для полноценного развития свиного цепня необходима смена хозяев за его жизнь. Человек является окончательным хозяином. В его кишечнике паразитирует взрослый гельминт, который развивается за 2 месяца из финны (личинки червя в тканях), съеденной с мясом. Паразит прикрепляется к стенке тонкого кишечника и растёт, поглощая пищу и постепенно наращивая членики (от шейки), которые по мере созревания отрываются и выходят в окружающую среду при дефекации. Паразит может жить в кишечнике десятки лет.
Человек может стать и промежуточным хозяином (при поедании яиц). В этом случае для паразита наступит "экологический тупик" — он не сможет развиться до половозрелой стадии и продолжить свой род, потому что мясо человека с финнами никто не ест.
Яйца выживают в окружающей среде в течение нескольких месяцев в зависимости от условий. Высыхание могут выдерживать в течение 10 месяцев, способны зимовать под снегом, в воде живут до 4 месяцев. При кипячении погибают практически мгновенно, при 65 °С сохраняют жизнеспособность в течение 3 минут, при 20-25 °С под воздействием прямых солнечных лучей сохраняются до 2 дней, если они закрыты травой — до полутора месяцев. Раствор хлорной извести 10-20 % убивает яйца за 5-6 часов. Цистицерки в мясе погибают при его замораживании при температуре -12 °С и поддержании в толще мяса температуры не ниже -10 °С в течение 10 дней [1] [2] [9] [10] .
Эпидемиология
Тениоз является одним из древнейших известных заболеваний. Первые упоминания встречаются ещё в 16 веке до нашей эры (Древний Египет), имеются записи Аристотеля и Гиппократа (финноз свиней). В настоящее время ВОЗ относит тениоз и цистицеркоз к группе забытых ("пренебрегаемых") болезней, т. е. тех, о которых мало говорят и обращают внимание развитые страны.
Распространение повсеместное, но наиболее поражены отдельные регионы: Индия, Африка, Южная Америка, Азия, Северный Китай, Восточная Европа, Белоруссия, Украина. Это регионы, где уровень дохода низкий или ниже среднего, где люди едят много плохо приготовленной свинины и недостаточно соблюдается гигиена. Здесь цистицеркоз является причиной эпилепсии в 30 % случаев, а в некоторых областях, где свиньи и люди живут вместе — до 70 %, по данным ВОЗ [3] . В РФ в среднем выявляется до 500 случаев в год [11] . Есть тенденция к повышенной заболеваемости сельских жителей и работников свиноводческих хозяйств.
Механизм передачи фекально-оральный, путь заражения пищевой. Источник инфекции и окончательный хозяин — заражённый человек, выделяющий с фекалиями яйца гельминта. Промежуточные хозяева — иногда человек, но чаще животные, которые поедают корм, загрязнённый фекалиями человека: свиньи (отсюда происходит название вида), кабаны, обезьяны, собаки, кошки.
Факторы передачи:
- При тениозе — недостаточно термически обработанное мясо свиней или диких кабанов. Наиболее опасно мясо, не прошедшее ветеринарный контроль. В этом случае человек заражается, поедая финны, т. е. зародыши червя, с инфицированным мясом.

- При цистицеркозе — загрязнённые яйцами пища и объекты внешней среды при несоблюдении людьми правил гигиены. Фактором передачи также может быть аутоинвазия, когда у человека с паразитом в кишечнике из-за нарушения перистальтики ЖКТ яйца из кишечника попадают в желудок. Т. е. яйца свиного цепня заразны и опасны для человека сразу, как только покидают организм с каловыми массами. Поэтому риск заражения цистицеркозом есть для любого человека, особенно если пренебрегать правилами гигиены и правилами обработки пищевых продуктов (тщательное мытьё) [1][3][5][7][11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тениоза
Множество случаев заражения и болезни проходит бессимптомно или малосимптомно. Жалобы таких больных обычно незначительны и связаны в основном с расстройствами пищеварения. Примерно через 1-1,5 месяца от момента заражения (а может и раньше) может наблюдаться лёгкое недомогание, головокружение, слабость, нарушения сна, умеренные головные боли, раздражительность, сниженный или повышенный аппетит, тошнота, дискомфорт и несильные боли в разных отделах живота. Развиваются запоры, чередующиеся с диареей, возможен анальный зуд, больной может умеренно худеть.
Характерной особенностью является периодическое (раз в несколько месяцев) выделение с калом оторвавшихся члеников паразита начиная с 2-3 месяцев паразитирования и так десятки лет. Их хорошо видно невооружённым глазом. Могут быть симптомы гипохромной анемии (недостатка железа): бледность кожи и слизистых, быстрая утомляемость при физической нагрузке, шум в ушах, обмороки, чувство мурашек по коже. Развивается гиповитаминоз В1 (тёмно-красный сухой язык со сглаженными сосочками). В результате отравления организма продуктами жизнедеятельности паразита, а также из-за расстройства пищеварения повышается склонность к необъяснимым высыпаниям токсико-аллергического характера на коже.

Тениоз у беременных
У беременных заболевание может протекать более тяжело, что обусловлено характерными физиологическими процессами в организме женщины этого периода. Наиболее часто наблюдаются расстройства пищеварения (запоры, диарея), тошнота, рвота, снижение гемоглобина, зуд кожи, перианальный зуд. Может быть плохой набор веса у плода. Вследствие более частого нарушения желудочно-кишечной перистальтики (моторики) повышается риск заброса яиц паразита в желудок и развития цистицеркоза [1] [4] [6] [10] .
Патогенез тениоза
Во время паразитирования свиной цепень повреждает слизистую при помощи крючьев и присосок, что вызывает расстройство пищеварения и нарушает моторику кишечника. Кроме того, гельминт потребляет много важных для человека питательных веществ, микроэлементов и отравляет организм продуктами своей жизнедеятельности, что приводит к токсико-аллергическому отравлению.
При заглатывании яиц паразита извне или при рефлюксной болезни, когда нарушается моторика кишечника и яйца из кишки попадают в желудок, развивается цистицеркоз. В различных органах и тканях развиваются соединительнотканные капсулы, содержащие зародыш — цистицерк. Вокруг наблюдаются воспалительные изменения в виде аллергической реакции и дистрофически-атрофические изменения из-за механического давления на окружающую ткань.
При локализации в головном мозге вокруг капсулы наблюдается воспаление мелких сосудов и инфильтрация окружающей ткани плазматическими клетками, что вызывает расстройство движения спинномозговой жидкости (ликвора), отёк мозговой ткани, развитие менингита и энцефалита. При паразитировании в оболочках мозга у его основания возможно развитие рацемозной (ветвистой) формы цистицеркоза до 25 см в длину.
С течением времени (до 5 лет) цистицерк претерпевает дегенеративные изменения — происходит его набухание и разложение (расплавление), что сопровождается усилением токсического и местного воспалительного воздействия. Исходом гибели личиночной формы паразита является кальцификация и местное рубцевание. Специфичных симптомов при этом процессе нет, после полной гибели цистицерков болезнь заканчивается, если, они не находятся в жизненно важных органах [1] [5] [6] [9] .
Классификация и стадии развития тениоза
По Международной классификации болезней 10-го пересмотра (МКБ 10):
- Тениоз:
- B68.0 Инвазия, вызванная Taenia solium.
- B68.9 Тениоз неуточнённый (при подозрении на болезнь, но отсутствии лабораторного подтверждения).
- Цистицеркоз:
- B69.0 Цистицеркоз центральной нервной системы (судороги, эпилепсия, необъяснимая рвота).
- B69.1 Цистицеркоз глаза (нарушения зрения, слепота).
- B69.8 Цистицеркоз других локализаций.
- B69.9 Цистицеркоз неуточнённый [1][2] .
Осложнения тениоза
Острый аппендицит. В правой половине живота снизу постепенно нарастают боли, появляется тошнота, характерен субфебрилитет (температура тела от 37,1 до 38,0 °С). В анализе крови наблюдается нейтрофильный лейкоцитоз со сдвигом влево — повышенный уровень нейтрофилов с преобладанием незрелых форм, которые не могут в полной мере осуществлять защитную функцию.
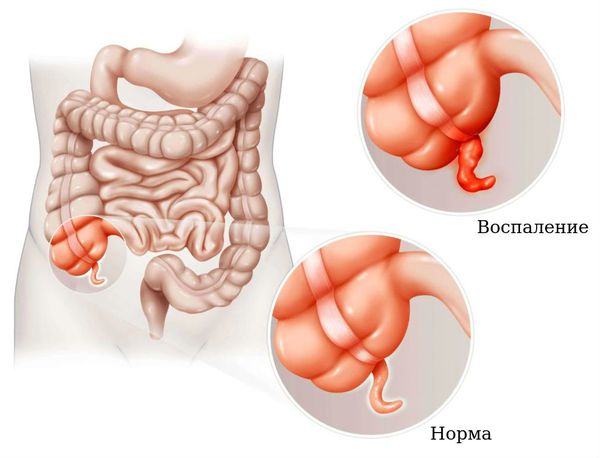
Панкреатит ( воспаление поджелудочной железы) . Характеризуется тошнотой, рвотой, опоясывающими болями в животе.
Кишечная непроходимость. Симптомы — с хваткообразные боли в животе без связи с приёмом пищи, запоры, метеоризм, вздутый живот, учащение пульса, рвота, бледность кожи.
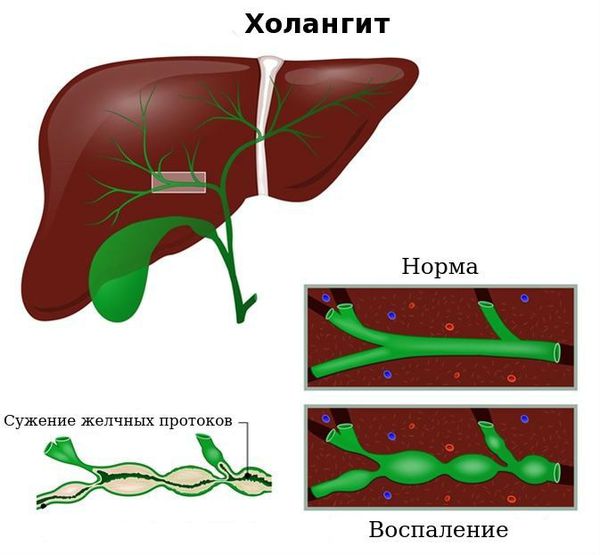
Холангит ( воспаление жёлчных протоков) . Субфебрильная или фебрильная лихорадка, выраженные боли в правом подреберье, озноб, повышенная потливость, тошнота и рвота, желтуха и кожный зуд.
Гипохромная анемия. Бледность кожи и слизистых оболочек, повышенная утомляемость, чувство мурашек и покалывания, головокружения, шум в ушах, обмороки.
Цистицеркоз. Может быть осложнением тениоза, а может быть отдельным заболеванием. В основном симптоматика проявляется при поражении центральной нервной системы (ЦНС) — головного и спинного мозга и глаз. В зависимости от локализации возникают головные боли различной интенсивности, рвота, эпилептические припадки, нарушения речи, расстройства личности, бред и галлюцинации, деменция. При поражении глаз могут наблюдаться воспалительно-дистрофические процессы в различных отделах глаз — рецидивирующие конъюнктивиты, увеиты, отслоение сетчатки, атрофия глазного яблока, что может привести к слепоте. При поражении сердца могут возникать нарушения ритма. При поражении мышц и подкожной клетчатки иногда может наблюдаться некоторая болезненность при ощупывании и приподнятость этого участка в виде подкожного плотного опухолевидного бугорка [1] [5] [5] [8] .
Диагностика тениоза
Тениоз или цистицеркоз может быть заподозрен на основании следующих признаков:
- эпиданамнез — проживание на территории развитого свиноводства, употребление плохо приготовленной свинины, низкий социально-экономический уровень страны или региона;
- расстройства пищеварения;
- астено-невротические проявления — слабость, повышенная утомляемость, эмоциональная нестабильность, раздражительность, повышенная потливость;
- выход с калом неподвижных члеников паразита;
- развитие неврологической симптоматики (эпилепсия), патологии органов зрения.
Дифференциальная диагностика
Основывается на данных анамнеза, типичном виде члеников паразита и их микроскопическом исследовании.
Лабораторная диагностика
Клинический анализ крови — изменений может не быть, иногда наблюдаются гипохромная анемия, умеренное повышение эозинофилов, повышение скорости оседания эритроцитов (СОЭ), редко выявляется небольшое повышение лейкоцитов за счёт сегментоядерных клеток (наиболее большой группы иммунных клеток).
Общий анализ мочи — как правило, без отклонений.
Биохимический анализ крови — возможны отклонения при развитии осложнений:
- При холангитах — повышение маркеров нарушения выработки или оттока желчи: АСТ, ГГТ, ЩФ, общего билирубина.
- При панкреатитах — повышение амилазы.
- При поражении сердца — повышение ЛГД и КФК-МВ.
Серологические специфические исследования:
- Иммуноферментный анализ (ИФА) антител IgG — в основном применяются с целью диагностики внекишечного поражения — цистицеркоза, результаты могут быть ложноположительными;
- Иммунный блоттинг — более точный метод лабораторного исследования сыворотки крови на присутствие антител , который применяют для подтверждения результатов ИФА. Этот метод позволяет снизить число ложных результатов, но в РФ он недоступен.
ПЦР кала — выявление антигенов свиного цепня. Это достаточно чувствительный метод, однако может дать ложноотрицательный результат ввиду ограниченного количества материала в кале.
Копроовоскопия — микроскопическое изучение кала с целью обнаружения яиц и зрелых члеников паразита. По яйцам невозможно установить точный диагноз, т. к. они очень похожи на яйца других представителей этого рода, проводится не менее трёх раз в разные дни. Для определения вида паразита необходимо исследование члеников.
Инструментальная диагностика
Компьютерная (КТ) и магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ), прямая офтальмоскопия — применяются для выявления цистицеркоза. КТ лучше выявляет кальцификаты цистицерков (особенно небольшие). МРТ больше подходит для обнаружения цистицерков в некоторых трудновизуализируемых местах мозга, также МРТ указывает на местные окружающие изменения (отёк) и возможную гибель паразита.
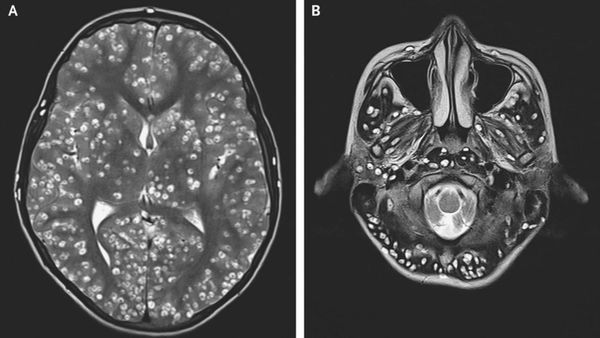
Исследования спинномозговой жидкости при поражении цистицерками ЦНС (лимфоцитарный плеоцитоз, увеличение уровня эозинофилов, белка).
Биопсия — морфологическое исследование биоптатов при оперативном вмешательстве [1] [3] [6] [10] .
Лечение тениоза
Госпитализации подлежат больные с тяжёлыми сопутствующими заболеваниями, а также больные с цистицеркозом ЦНС и глаз. Остальные больные могут лечиться амбулаторно.
В качестве этиотропной терапии (направленной на уничтожение возбудителя) применяется Празиквантел и Никлозамид. Есть данные об эффективности Альбеназола, но они ограничены. Продолжительность лечения — 3 дня.
При лечении цистицеркоза выбор способа уничтожения паразита зависит от его локализации и количества. При локализации под кожей и в тканях (кроме ЦНС и глаз) лечение, как правило, не проводят, так как риск последствий от приёма препарата выше пользы от лечения. Однако, если наличие паразита ведёт к каким-то физическим и эстетическим недостаткам, лечение назначается.
При локализации цистицерков в ЦНС и глазах лечение проводят только в условиях неврологического стационара, применяются Празиквантел и Альбендазол в сочетании с глюкокортикостероидами (т. к. есть риск местного воспаления и повреждения нервной системы и глаз).
В качестве мер патогенетической и симптоматической терапии при тениозе могут назначаться средства нормализации моторики кишечника (прокинетики) и микрофлоры кишечника (пре- и пробиотики).
При цистицеркозе головного мозга применяют противосудорожные препараты.
Возможно хирургическое лечение (удаление цистицерков при поражении головного и спинного мозга).
Контроль излеченности тениоза:
- визуальный — осмотры кала (о выздоровлении говорит отсутствие периодического отделения члеников червя);
- 4 отрицательных анализа кала на яйца гельминтов с интервалом в 1 месяц [2][4][5][8] .
Прогноз. Профилактика
При изолированном тениозе прогноз благоприятный. При развитии осложнений, особенно цистицеркозе ЦНС и глаз, прогноз серьёзный: возможно развитие тяжёлых стойких поражений (эпилепсия, слепота) и летальный исход.
Что такое бластоцистоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Бластоцистоз — это заболевание человека, вызываемое простейшим одноклеточным микроорганизмом Blastocystis, который колонизирует желудочно-кишечный тракт и при определённых условиях вызывает срыв функционирования кишечника (запоры или диарея, дискомфорт и боли в животе). Также Blastocystis повышает частоту развития иммунодепрессии, проблемной кожи и патологии суставов. Паразит проникает в организм посредством фекально-орального механизма. Чаще всего болезнь протекает в форме неактивного носительства.
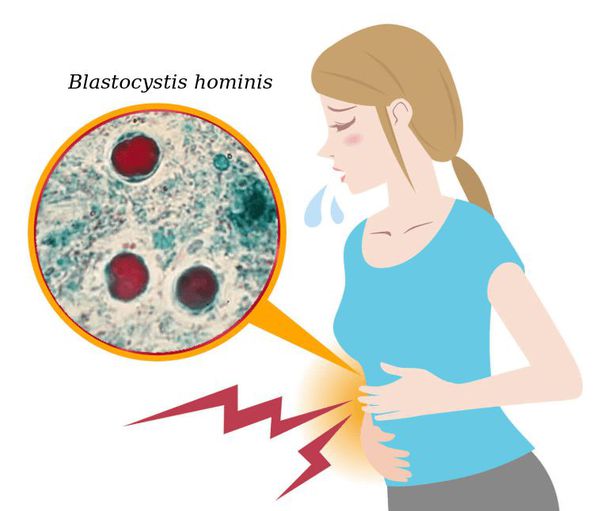
Этиология
- домен — Eukaryota;
- тип — cтраменопилы (также входят водоросли, водяная плесень и диатомовые водоросли);
- учебный класс — Blastocystae;
- порядок — Blastocystida;
- семья — Blastocystidae;
- род — Blastocystis;
- вид — Blastocystis hominis (рекомендуется использовать общий термин — Blastocystis sp).
Впервые эти простейшие были описаны А. Алексеевым (А. Alexieff) в 1911 году, а уже в 1912 году Е. Брумпт (Е. Brumpt) выделил и описал основные признаки бластоцисты в материале человека.
Бластоцисты — очень разнообразные по генетическим вариациям простейшие одноклеточные. Они выявляются в кишечнике как у человека, так и у множества животных (свиней, приматов, собак, птиц, тараканов и др.), т. е. не являются строго специфичными к хозяину. Отсюда рекомендуемое наименование — Blastocystis sp. (species subtype n., где n — число, указывающее субтип простейшего ). До сих пор ведутся дискуссии по поводу патогенности их для человека, однако в экспериментах на мышах заражение бластоцистами вызывало у животных воспаление кишечника, выраженное нарушение его работы и преждевременную смерть, а у высших приматов — хроническую диарею [16] .
Для людей характерно нахождение подтипа ST (при генетическом типировании). Всего 9 видов (ST1-ST9), наиболее распространены ST1, ST2, ST3 и ST4, причём они могут сосуществовать в организме одного хозяина в разных сочетаниях. На сегодняшний день конкретная патогенность разных подтипов для человека не выяснена, однако есть предположения, что заболевание вызывают лишь некоторые подтипы паразита, тогда как другие в основном приводят лишь к носительству.
Жизненный цикл Blastocystis до конца не изучен. Размножаются микроорганизмы бинарным делением. Тело покрыто специальной мембраной, с которой соприкасается цитоплазма и органеллы. Паразиты могут находиться в кишечнике от недели до нескольких лет.
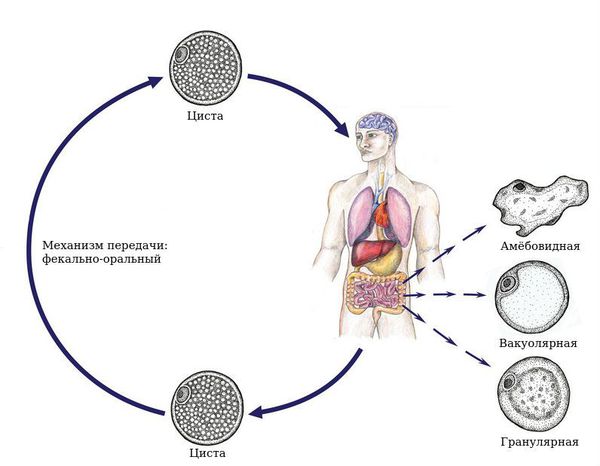
Бластоцисты имеют 4 формы жизни:
- Вакуолярная форма. В культуре у бессимптомных носителей бластоцисты выявляются в форме круглого или овального образования размерами 5-50 (редко больше) мкм. Основную часть тела занимает большая центральная вакуоль (вероятно, предназначена для хранения), окружённая тонким кольцом цитоплазмы. В цитоплазме могут находиться от 1 до 6 ядер.
- Гранулярная форма. В просвете кишечника выявляются тонкостенные простейшие, напоминающие вакуолярную форму, но с наличием в вакуоли и цитоплазме гранул различной формы (участвуют в химических процессах поддержания жизнедеятельности и размножении).
- Авакуолярная (амёбовидная) форма. Выявляется в культуре у больных кишечными расстройствами. Амёбовидные бластоцисты в кишечнике адгезированы (прикреплены) к эпителию и неподвижны.
- Цисты. Они меньше по размеру и имеют толстую многослойную стенку, выявляются в культуре (кале). Данная форма лишена центральной вакуоли, имеет несколько небольших вакуолей с отложениями пищи и несколько ядер. Это самая устойчивая во внешней среде форма.
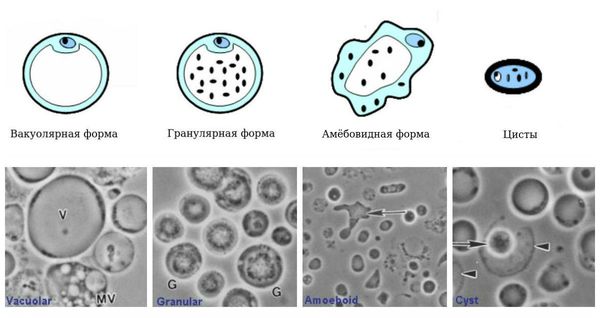
Паразиты к ультивируются на питательных средах, причём образуют множество нетипичных форм (промежуточные стадии развития).
Бластоцисты достаточно быстро погибают при действии бытовых дезинфектантов, кипячении и замораживании. В окружающей среде при 4 °C могут сохранять жизнеспособность до 2 месяцев, при 25 °C — до 1 месяца, длительно не погибают в дистиллированной воде [1] [2] [6] [12] .
Эпидемиология
Бластоцисты распространены повсеместно, это один из самых часто встречающихся паразитов в мире (заражены, вероятно, не менее 1 млрд. человек), распространённость подтипов пока изучается. В некоторых регионах, особенно в тропиках, ими инфицировано до 100 % населения, в США — около 23 % популяции. Заболеваемость выше в тех регионах, где присутствует антисанитария и не уделяется должного внимания соблюдению правил личной гигиены. Чаще болезнь выявляется среди людей, которые контактируют с животными и имеют сопутствующую патологию ЖКТ или хронический вирусный гепатит. Во многих случаях они выявляются в сочетании с другими патогенами ЖКТ (лямблиями, возбудителями острых кишечных инфекций и др.).
Механизм передачи — фекально-оральный, пути — водный (через загрязнённую воду), пищевой (через заражённую пищу) и контактно-бытовой (при несоблюдении правил гигиены, возможно распространение насекомыми, например мухами и тараканами).
Риск распространения в семье, где соблюдают правила гигиены, минимален. В странах, где проводят централизованное обеззараживание водопроводной воды, вода из под крана безопасна (т. е. бластоцисты в ней не содержатся) [1] [7] [8] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы бластоцистоза
Во множестве случаев выявления бластоцист у людей симптомы не проявляются или их нельзя напрямую связать с паразитом (по крайней мере, на сегодняшнем уровне развития медицины). Возможно, люди (и врачи в том числе) оказались "ослеплены" фактами исчезновения и уменьшения количества некоторых паразитарных заболеваний (например, малярии и дракункулёза), что создало неверное представление о победе над паразитами. Однако постоянное увеличение числа больных с патологией кишечника неустановленной этиологии, иммунодефицитами и кожными заболеваниями может быть вызвано распространением именно тех микроорганизмов, которые раньше считались непатогенными или условно-патогенными.
Чаще всего при манифестной форме заболевания (когда болезнь начинает проявляться) больные указывают на следующие признаки:
- дискомфорт и боли в животе;
- неустойчивый стул, диарея, запор, изменение консистенции стула, его цвета и запаха;
- метеоризм;
- тошнота;
- перианальный зуд, иногда зуд кожи;
- повышенная утомляемость, снижение работоспособности;
- снижение массы тела (похудание);
- необъяснимые высыпания на коже;
- дискомфорт в суставах;
- частые простудные заболевания;
- повышенная нервная возбудимость, плохой сон;
Есть публикации, описывающие связь бластоцист с воспалительными заболеваниями кишечника (ВЗК). Дело в том, что ВЗК связаны с нарушением барьерной функции эпителия, а у пациентов с бластоцистозом повышена кишечная проницаемость [16] . Это позволило предположить, что паразиты могут повреждать стенку кишечника [15] .
Есть некоторые предпосылки, указывающие на более частое развитие манифестных форм болезни, в основном это:
- генетическая предрасположенность (связанная с повышенной секрецией цитокинов);
- возраст (чем старше человек, тем больше вероятность симптоматики);
- более патогенные подтипы бластоцист.
Бластоцистоз у беременных
Каких-то обособленных проявлений инфекции у беременных не наблюдается. Возможно более раннее начало и тяжесть токсикоза, чаще развиваются функциональные нарушения работы желудочно-кишечного тракта. Возможное влияние на плод ограничивается повышенным риском гипотрофии ( недостаточной массы тела) , анемии, отставании по срокам развития, после рождения может быть отмечена склонность к аллергизации и патологиям кожи (атопический дерматит, псориаз) [3] [4] [7] [13] .
Патогенез бластоцистоза
Бластоцисты могут нарушать расположение и функционирование актиновых филаментов эпителиальных клеток кишечника (нитей из специальных белков, находящихся в цитоплазме клеток, их основная функция — сократительная). Таким образом они влияют на барьерную функцию кишечной стенки, что приводит к диарее, нарушению процессов пищеварения и обмена биологически активных веществ.
Выявлена способность бластоцист стимулировать выработку провоспалительных цитокинов клетками толстого кишечника (ИЛ-8, гранулоцитарно-макрофагальный колониестимулирующий фактор), которые играют роль в развитии ревматоидного артрита.
Классификация и стадии развития бластоцистоза
Единой официально принятой классификации бластоцистоза не существует, обобщённо можно представить следующую градацию:
По клинической форме:
- Манифестная (с симптомами):
- типичная (с проявлениями желудочно-кишечных расстройств);
- атипичная (с поражениями кожи и суставов).
- Субклиническая (проявления болезни минимальны или выражаются только лабораторными изменениями).
- Бессимптомная ("неактивное" паразитоносительство).
В Международной классификации болезней 10-го пересмотра (МКБ-10) о бластоцистозе нет информации. Однако заболевание можно отнести к группе А07 — Другие протозойные кишечные болезни.
Осложнения бластоцистоза
- Белково-энергетическая недостаточность (гипо- и авитаминоз, снижение веса, анемия и др.).
- Развитие дисбиотического состояния кишечника (стойкое нарушение количества, состава и функционирования нормальной флоры кишечника).
- Артрит — дискомфорт и боли в суставах. — зудящие обширные высыпания на теле.
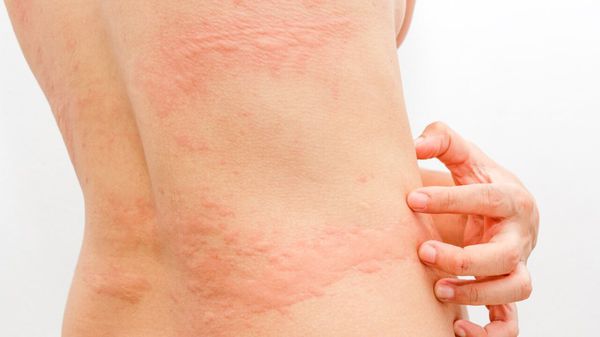
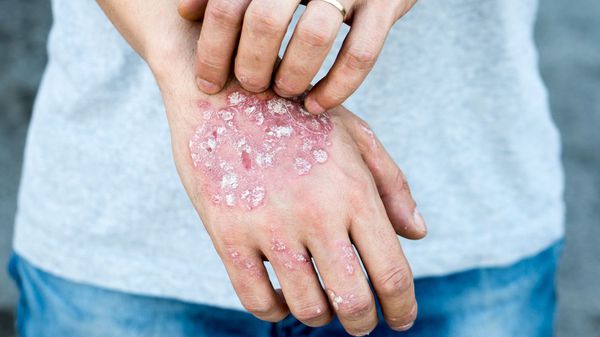
- Появление и обострение генетически обусловленных заболеваний кожи (атопический дерматит, псориаз и др.). В данном случае бластоцисты выступают как провоцирующий фактор [3][4][12][14] .
Диагностика бластоцистоза
Для верной диагностики важно целенаправленно определить бластоцисты в биологическом материале. Врач принимает решение, являются ли именно они причиной симптомов у конкретного человека: часто симптомы обнаруживаются в ассоциации с другими патогенами или имеется сопутствующая патология неинфекционного характера.
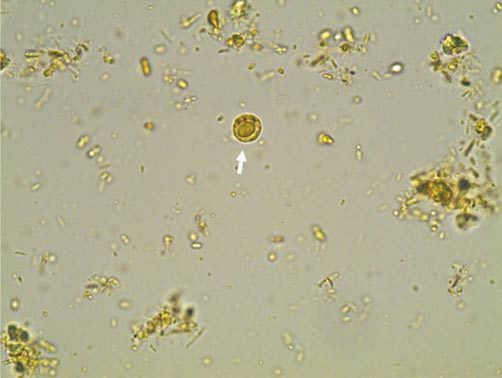
- ПЦР диагностика (выявление бластоцист в кале путём молекулярно-генетической детекции). Достаточно надёжный и чувствительный метод, за одно исследование выявляемость составляет 88 %.
- Посев кала (культивирование бластоцист на средах). Надёжный метод выявления, однако сложен в реализации и коммерчески невыгоден [1][7][12][14] .
Дифференциальная диагностика
- Паразитарные заболевания другой этиологии (лямблиоз, аскаридоз, энтеробиоз, дифиллоботриоз и др.).
- Кишечные инфекции (сальмонеллёз, дизентерия, энтеровирусная, ротавирусная и др.).
- Синдром раздражённого кишечника (при полном отсутствии этиологического фактора кроме питания и стресса).
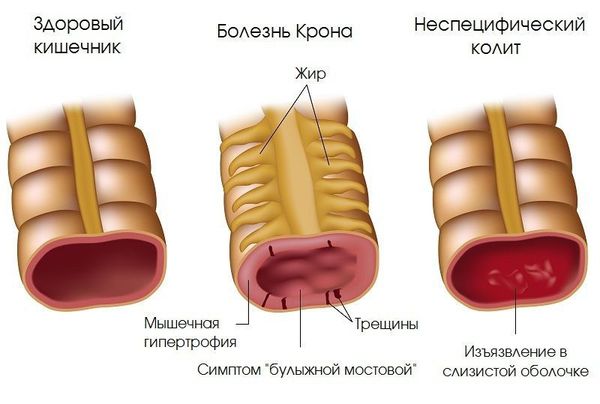
- Воспалительные заболевания кишечника неинфекцонной природы (болезнь Крона, язвенный колит).
- Заболевания желудка и верхнего отдела кишечника гастроэнтерологического характера (гастрит, дуоденит). (сборное понятие, характеризующееся неустойчивостью стула, дискомфортом в животе различного характера, снижением веса и другими симптомами) [1][4][12][14] .
Лечение бластоцистоза
Терапия бессимптомного носительства в каком-либо медицинском вмешательстве не нуждается. Не стоит заниматься лечением и тем более самолечением при отсутствии симптоматики и сомнении в роли данного микроорганизма в болезни. Нет гарантии, что применение препаратов благотворно скажется на здоровье кишечной экологической системы и организма в целом и не ухудшит проявления заболевания.
При развитии симптомов, в патогенезе которых нельзя исключить роль бластоцист, и подтверждении паразитирования их в кишечнике проводятся следующие мероприятия:
- диета с ограничением сладкого, газообразующего и мучного (улучшает микроклимат кишечника, в какой-то мере лишает бластоцист энергетических запасов, снижает метеоризм);
- противопротозойная терапия. Применяются препараты нитроимидазольной группы, ингибиторов дигидрофолат-редуктазы и некоторые пробиотические дрожжи;
- применение пробиотических препаратов (лактобактерии, бифидобактерии и энтерококки);
- повышение иммунитета кишечника. Применение иммуномодулирующих средств и прямое восполнение дефицита IgA в просвете кишечника.
На сегодняшний день не существует какого-либо препарата или стратегии лечения, позволяющих со 100 % вероятностью избавиться от бластоцист [5] [7] [12] [13] .
Прогноз. Профилактика
При сохранном иммунитете прогноз благоприятный (даже при развитии клинически выраженного заболевания), при иммунодефиците (особенно СПИДе) прогноз серьёзный.
Меры профилактики неспецифичны, их можно разделить на общественно-значимые (социальные) и индивидуальные.
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз: симптомы, подкожный и внутренний дирофиляриоз у человека, лечение и профилактика
Дирофиляриоз — один из гельминтозов, ранее считавшихся исключительно зооспецифическим и до недавнего времени бытовало мнение, что этому заболеванию подвержены исключительно животные. В первую очередь — собаки. Но в последние годы все чаще стали регистрироваться случаи заражения людей.
Дирофиляриоз (Dirofilariasis) — относится к ларвальным гельминтозам. То есть, при этом заболевании паразитирует не взрослая особь нематоды, а ее личинка, не достигшая половой зрелости. Разносчиками заразы являются комары, поэтому наиболее часто этот гельминт встречается в теплом климате: от Австралии, Южной Америки и Африки до Юга России и Средней Азии. На протяжении последних лет наибольшее количество заболевших дирофиляриозом регистрировалось в Иране и Греции. Но в последние годы все чаще регистрируют эту болезнь и в умеренном климате.
Так, на территории Российской Федерации на протяжении нескольких лет выявляют по 35-40 случаев дирофиляриоза ежегодно. Причем география заражения весьма обширна — от теплого Ростова, умеренных климатических зон Тулы и Рязани, до морозной Сибири. На самом же деле уровень заболеваемости может быть значительно выше. Поскольку этот вид гельминтоза долго считался присущим только животным, то медики его не изучали, и на сегодняшний день о нем мало знают и не сразу могут поставить верный диагноз.
Причины возникновения дирофиляриоза
Как происходит заражение дирофиляриозом?
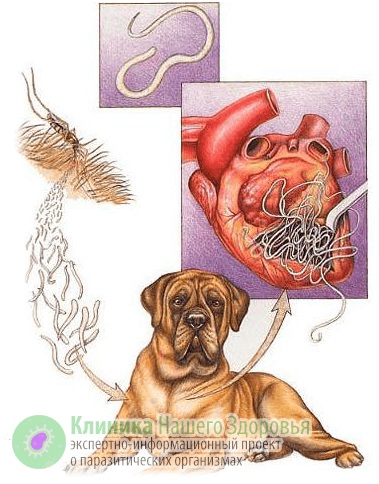
Механизм заражения у людей — трансгемный, то есть инфицирование происходит через кровь. Передается болезнь, зачастую, через укусы комаров. Реже, через укусы блох, слепней и других видов кровососущих насекомых. А источником заразы, как это ни прискорбно, выступают наши домашние животные. В первую очередь собаки, изредка кошки. По данным ветслужбы до 30% собак, живущих в городах, страдают от упомянутой инвазии. В сельской местности этот показатель еще выше. В организме животного взрослые дирофилярии паразитируют в сердце, легких, бронхах и крупных кровеносных сосудах. Самки выделяют в кровь тысячи личинок-микрофилярий, которые имеют микроскопический размер — до 0,3 мм в длину. Именно поэтому они с кровотоком и лимфотоком разносятся по всему организму.
Микрофилярии так микроскопичны, что с кровью и лимфой попадают не только во все органы и ткани человека или животного, но даже преодолевают плацетнарный барьер и внутриутробно инфицируют плод. С кровью животного микрофилярия попадает к промежуточному хозяину — комару. Насекомое, в свою очередь, кусает инвазированное животное, личинки попадают в его брюшную полость, но часть из них остается в хоботке комара. Когда насекомое кусает следующую жертву — часть паразитов из хоботка попадает в кровоток следующего хозяина. Так дифиляриоз передается от животного к животному и к человеку.
У людей тотальная восприимчивость к дирофилриозу – то есть, если человека кусает инфицированный комар, то он заразится со 100% вероятностью. Но в наибольшей зоне риска заражения дирофиляриозом находятся некоторые категории людей, среди которых:
- заводчики собак и кошек;
- люди, проживающие у открытых водоемов;
- те, кто часто бывает на природе — охотники, туристы, огородники, рыбаки.
Этапы развития дирофиляриий
Когда комар (реже другое кровососущее насекомое) заглатывает личинку нематоды с кровью, та около суток остается у него в кишечнике. Затем микрофилярии мигрируют в обратном направлении — к хоботку комара, где дозревают до инвазивной стадии. В этот период, комар, кусает жертву и заражает ее дирофиляриозом.
У нового хозяина около трех месяцев личинки остаются в месте комариного укуса: в коже или в подкожной клетчатке. Именно тут микрофилярии линяет и уже более жизнеспособными попадают в кровоток и разносятся по организму. Паразитировать микрофилярия может около трех лет.
До половозрелости дирофилярия развивается только в организме животных. Человеческий организм для нее тупиковый вариант, так как большинство личинок все же гибнут в крови людей. Это значит, что человек не может быть источник заражения.
Воздействие дирофилярий на человека
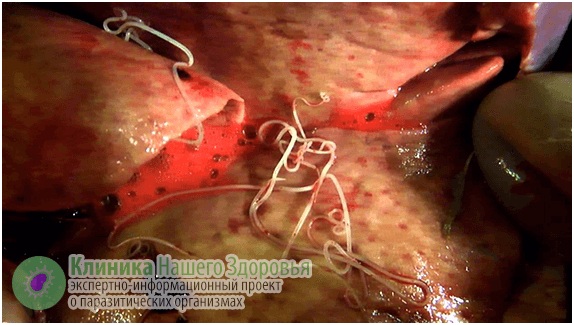
Главная опасность дирофиляриоза — первичные реакции на месте внедрения микрофилярии. Может возникнуть сильная аллергическая реакция. Кроме того, кожа воспаляется, образуются уплотнения (шишки) довольно большого диаметра. Внутри этих уплотнений находится серозная жидкость и/или гной, внутри этого содержимого и обитает какое-то время дирофилярия. Часто паразит погибает, тогда уплотнение постепенно может само рассосаться. Но чаще все же требуется хирургическое вмешательство.
Виды дирофиляриоза
Инвазионное заболевание вызывает червь-паразит. Личинки нитевидной нематоды, вызывающие болезнь, бывают нескольких разновидностей, и поэтому заражение ими приводит к разным формам заболевания.
Dirofilaria repens и Dirofilaria immitis — основные виды, поражающие собак и реже кошек. Именно эти разновидности гельминта являются самыми распространенными среди заболевших людей, ведь в подавляющем большинстве случаев дирофиляриоз у человека появляется при укусе комара-переносчика, контактировавшего до этого с данными животными.
- Dirofilaria repens вызывает подкожную разновидность дирофиляриоза.
- Dirofilaria immitis — висцеральную.
В России и странах ближнего зарубежья встречается в основном подкожный дифиляриоз. Висцеральный дирофиляриоз распространен в жарких странах Азии, Японии, Индии, США, Африке, Канаде, Вьетнаме, Австралии, на юге Европы.
Симптомы и места распространения дирофиляриоза
Скрытая форма дирофиляриоза у человека длится от 1 до 12 месяцев. Основным симптомом является появление под кожей или слизистой, болезненного уплотнения, с покраснением и зудом на месте внедрения. При этом гельминт под кожей может перемещаться (со скоростью до 15 мм в сутки), что может быть заметно для человека, как по ощущениям, так и визуально. Часто, заметив на теле уплотнение похожее на опухоль, пациенты обращаются к хирургу, а тот решает, что это липома, опухоль, фиброма, атерома и т.п., а затем уже в ходе операции обнаруживает гельминта.
У дирофилярий есть любимые места на теле человека — это органы зрения, ноги и руки, шея, лицо, грудь, мошонка. Могут появиться такие симптомы, как слабость, пассивность, тошнота, нервозность, бессонница, повышенная температура, боли в голове и в области поражения паразитом. В 50 % случаев обычно поражаются органы зрения. Человек жалуется на ощущение чего-то ползающего в глазу, у него наблюдается покраснение век и глаз, блефароспазм. При перемещении гельминта возникает боль, слезотечение и зуд. Иногда через конъюнктиву виден сам гельминт.
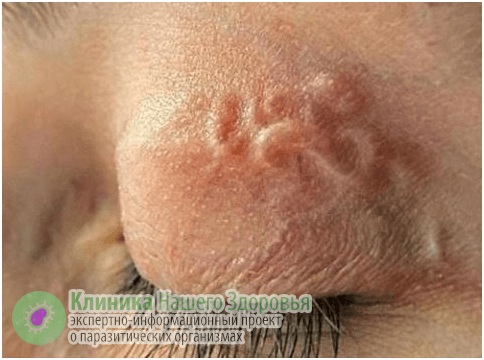
При нахождении дирофилярии в глазу вокруг нее образуется гранулема, что вызывает развитие экзофтальма и диплопии. Поражение глаз приводит к ослаблению зрения. Человек способен увидеть мигрирующего паразита. Наблюдения показали, что его перемещения усиливается под воздействием тепла.
Дифиляриоз обычно носит хронический характер, с рецидивами, характеризующимися периодами вспышек и затихания заболевания. Если вовремя не заняться лечением, вероятны воспаления тканей, и возникновение абсцесса.
Симптомы внутреннего дирофиляриоза
При этой разновидности паразитом поражаются легкие. Личинка живет в левом желудочке сердца и легочных артериях, образуя при этом фиброзную капсулу. Обычно болезнь протекает бессимптомно, реже вызывает боль в груди, кашель и кашель с кровью.
Заболевание часто выявляется случайно, например, при рентгене грудной клетки (видны узелки размером 1-2 см) или при оперировании легких.
Диагностика дирофиляриоза у человека
Диагностика заболевания представляет определенную сложность, так как её симптоматика схожа со многими другими заболеваниями, поэтому врачами часто ставится ложный диагноз и своевременное лечение затягивается. Основными жалобами пациентов являются появление мигрирующих подкожных узлов, ощущения перемещения паразита.
Диагноз дирофиляриоза можно подтвердить, сдав следующие анализы:
- анализ крови;
- после удаления паразита хирургом, проводится его макроскопическое исследование;
- проведение исследования на наличие серологической реакции, позволяющей обнаружить антиген паразита;
- аппаратная диагностика (УЗИ узлов, рентгеновские исследования, эхокардиография и электрокардиография).
Кроме того, перед постановкой диагноза специалист проводит анализ условий проживания больного, времени года, его деятельности. Факторами риска являются наличие домашних и бездомных собак и кошек, комаров, выезд в лес, на рыбалку, на дачу или в сад.
Риск заболевания дирофиляриозом особенно увеличивается в период высокой активности комаров. В связи с чем важны профилактические меры, производимые санитарными службами по ликвидации насекомых на территории водоемов. Известно, что заболевание носит сезонный характер, поэтому основное количество заболевших фиксируется весной и летом. Пики заболеваемости приходятся на периоды июнь-июль и октябрь-ноябрь.
Диагностика дирофиляриоза у животных
Для профилактики заболевания домашним животным необходимо регулярно давать противоглистные препараты. Признаками заболевания паразитами служат различные высыпания, уплотнения, ранки, опухоли на коже.
Больше всего при поражении страдает сердечно-сосудистая система животного. Поведение его становится пассивным, теряется аппетит, отмечается температура, кашель. Собака может прихрамывать и страдать от судорог.
Лечение дирофиляриоза
Форма болезни диктует методы лечения. Обычно у человека паразитирует одна неполовозрелая особь. Основной метод избавления от паразита — хирургический. Чтобы исключить перемещение паразита применяют дитразин. Редко применяется терапия медикаментами с использованием ивермектина или диэтилкарбамазина. Дополнительно при лечении используются успокаивающие и антигистаминные лекарства, нестероидные противовоспалительные средства, глюкокортикостероиды.
При глазном дирофиляриозе основным методом лечения будет удаление гельминта с помощью операции и последующие назначение дезинфицирующих и противовоспалительных препаратов для глаз, иногда также прописываются капли дексаметазона для уменьшения воспаления. Обязательно назначаются антигистаминные средства.
Профилактика дирофиляриоза
В России 4-30% (в зависимости от географии их проживания) домашних и уличных собак являются хозяевами-переносчиками микрофилярий. Самый большой процент зараженных животных в Греции и Иране- 25-60%.
Профилактика заболевания включает в себя истребление комаров и ограничение контакта с ними животных и человека, своевременное выявление дирофилярий животных и их лечение, борьба с бродячими животными, противоглистная профилактика у домашних питомцев.
Так как очагами дирофиляриоза являются водоемы около жилых районов, очевидна эффективность мер, применяемых санитарными органами по борьбе с кровососущими насекомыми. К тому же необходима борьба с комарами в подвалах жилых домов, ведь здесь эти паразиты могут с комфортом обитать весь год. Из подвалов жилых домов комары и другие насекомые попадают по вентиляционной системе в квартиры.
В лесу и около водоемов необходимо использовать репелленты и защищать участки тела с помощью одежды. Животным кроме репеллентов могут быть одеты специальные ошейники. По возможности старайтесь отказаться от прогулок в вечернее и ночное время суток.
Человек сам в ответе за собственное здоровье, а также за здоровье своих детей, родных и близких, поэтому отправляясь в отпуск в теплые страны, будьте бдительны! Легче предотвратить болезнь, соблюдая профилактические меры, чем лечить ее последствия!
Читайте также:

