Профессор по болезни лайма
Обновлено: 08.05.2024
Об авторах
Валентин Викторович Власов — академик РАН, доктор химических наук, профессор, директор Института химической биологии и фундаментальной медицины СО РАН. Лауреат Государственной премии РФ (1999). Автор и соавтор более 200 научных работ и девяти патентов.
Нина Викторовна Тикунова — доктор биологических наук, зав. лабораторией молекулярной микробиологии ИХБиФМ СО РАН (Новосибирск). Выпускница НГУ (1984).
Клещевой боррелиоз, или болезнь Лайма, — это переносимое иксодовыми клещами мультисистемное инфекционное заболевание с самыми разными проявлениями: кожными, суставными, неврологическими, кардиологическими и т. д. Первые симптомы возникают в течение нескольких дней или недель после укуса клеща, а поздние могут проявиться через месяцы и годы после заражения. При этом как симптомы, так и само течение болезни у разных людей могут значительно варьировать.
В месте укуса зараженного боррелиями клеща на коже появляется красное кольцо — первичная кольцевая мигрирующая эритема, результат воспалительной реакции на проникших в организм бактерий. Впоследствии на разных участках тела могут появиться множественные эритемы. Фото: James Gathany. Public Domain
В месте укуса инфицированного клеща через несколько дней может образоваться покраснение, которое расширяется в виде кольца и мигрирует по телу. Это так называемая мигрирующая эритема — яркое свидетельство локального размножения и распространения возбудителей инфекции, бактерий спирохет. Однако такое характерное покраснение развивается далеко не у всех заболевших, поэтому отсутствие эритемы не означает меньший риск развития болезни у человека, укушенного клещом. При этом 30–40% таких больных даже не замечают укус клеща, который стал причиной болезни.
В любом случае постановка клинического диагноза в ряде случаев невозможна без лабораторного подтверждения. Однако применяющиеся сегодня иммуноферментные тесты для диагностики боррелиоза несовершенны. Стандартный иммуноферментный тест регистрирует не самих боррелий, а антитела, вырабатываемые против них организмом, которые появляются лишь спустя 3–4 недели после заражения. Поэтому такие тесты часто оказываются ложноотрицательными, в первую очередь у пациентов, иммунная система которых не дала сильного иммунного ответа. Эти тест-системы нередко дают и ложноположительные результаты. Более трудоемкие анализы, основанные на определении нескольких бактериальных белков, также не дают абсолютно достоверных результатов.
Таким образом, лабораторные тесты могут подтвердить диагноз, но отрицательный результат не может считаться доказательством отсутствия боррелиоза. Поэтому врач должен проанализировать всю картину заболевания у конкретного пациента. Сделать это непросто, так как, к примеру, симптомы поражения головного мозга при боррелиозе похожи на симптомы нескольких нейродегенеративных заболеваний. А такие признаки, как слабость и головная боль, могут сопутствовать самым разным болезням, и не только инфекционным.
Считается, что у людей с нормально функционирующей иммунной системой заражение боррелиями вызывает активный иммунный ответ, так что бактерии могут погибнуть даже без стандартной для этого заболевания терапии. Для лечения болезни Лайма сегодня применяют антибиотики, наилучшие результаты дают цефтриаксон и доксициклин. Современная медицина предусматривает профилактическое применение антибиотиков для людей с высокой вероятностью заражения (укушенных клещом, с мигрирующей эритемой и т. п.) и двух-трехнедельный курс антибиотикотерапии при развитии заболевания.
Род Borrelia относится к спирохетам, ближняя родственница боррелий — бледная трепонема, возбудитель сифилиса. По внешнему виду боррелия напоминает длинную и тонкую закрученную спираль. Клетки бактерии имеют длину около 15–25 и толщину 0,2–0,3 мкм. Изображение: Janice Haney Carr, Public Domain
Несмотря на все эти меры, у некоторых больных болезнь переходит в хроническую форму, при которой не помогают даже повторные курсы антибиотиков. И здесь возникает трудность, связанная с определением причин этого болезненного состояния. Недостаточность знаний о механизмах повреждения организма в результате инфицирования боррелиями, об устойчивости бактерий к лекарствам, а также ненадежность современных методов клинической диагностики привели к появлению разных, полярных точек зрения на эту проблему.
Вакцины пока нет
Болезнь или синдром?
О проблеме клещевого боррелиоза спорят не только доктора — нет единства и среди ученых.
Согласно одной из точек зрения, с помощью стандартной антибиотикотерапии не удается уничтожить всех возбудителей болезни в организме пациентов со слабой иммунной системой. Это мнение подтверждается экспериментами на лабораторных животных: живые боррелии обнаруживались после лечения антибиотиками в организме инфицированных лабораторных мышей и обезьян. Результаты некоторых исследований говорят о том, что колонии боррелий, возможно, продолжают жить в органах и тканях в составе так называемых биопленок — сообществ микроорганизмов, заключенных в продуцируемый ими полимерный матрикс. В таком виде боррелии становятся практически недоступными для лекарств и клеток иммунной системы.
Согласно другой точке зрения, после курса антибиотикотерапии в организме не остается живых боррелий. Однако за время болезни бактерии успевают вызвать нарушения в работе иммунной системы, которые проявляются еще долгое время в виде аутоиммунных поражений. Сильными иммуногенами являются, к примеру, пептидогликаны клеточной стенки бактерий, которые могут долго сохраняться в организме. Долгосрочные токсические эффекты могут вызывать и остатки биопленок с погибшими боррелиями. Все эти бактериальные компоненты провоцируют воспалительные процессы, затрагивающие различные органы и ткани, что приводит, например, к артриту. Подобное болезненное состояние назвали пост-Лайм синдромом (Blaut-Jurkowska, Jurkowski, 2016).
Кстати сказать, ряд специалистов считает, что хроническая болезнь Лайма развивается в случае, когда пациент поражается одновременно боррелиями и другими патогенами, переносимыми клещами (например, риккетсиями). Клещи очень часто переносят одновременно возбудителей разных инфекций, и некоторые из них вызывают симптомы, клинически трудно различимые.
На ранней стадии заболевания клещевым боррелиозом люди могут испытывать самые разнообразные простудоподобные симптомы: лихорадку, усталость, нарушения сна, увеличение лимфатических узлов. В дальнейшем, при отсутствии лечения, могут отекать и болеть суставы, особенно коленные. Возникают неврологические проблемы (энцефалит, менингит, временный паралич лицевых мышц), а также нарушения функций мускулатуры, миозиты.
На поздних стадиях заболевания симптомы сильно варьируют. У некоторых больных появляются нарушения сердечного ритма, наблюдаются воспаления глаз, печени, появляется сильная слабость. Среди неврологических осложнений — тяжелая депрессия, нарушения памяти, бессонница, частая головная боль, непереносимость света или звуков, галлюцинации, энцефаломиелит и т. п.
Скрестили шпаги
С такой позицией не согласны тысячи людей в США, годами страдающие от тяжелых заболеваний, которые они связывают с последствиями клещевых инфекций. Хроническая болезнь Лайма впервые была отмечена в США еще 45 лет назад: по некоторым оценкам, число таких больных сегодня достигает 400 тыс. человек. Эти люди совместно с некоторыми врачами организовали Международное общество борьбы с болезнью Лайма и ассоциированными заболеваниями, которое предлагает применять агрессивную антибиотикотерапию при подозрении на то, что наблюдаемые болезненные симптомы вызваны боррелиозной инфекцией.
Защитники официальной точки зрения считают, что сама хроническая болезнь Лайма выдумана недобросовестными врачами, эксплуатирующими отчаянное состояние пациентов с неопределенным диагнозом. По их мнению, те пациенты, у которых современные методы диагностики не выявляют боррелий, нуждаются не в дополнительном лечении, а в помощи психиатра. В результате люди, считающие себя хроническими больными, вынуждены обращаться к врачам, несогласным с позицией медицинских властей, и лечиться за свой счет.
Как рукой снимет
Истина где-то посередине?
Таежный клещ Ixodes persulcatus — самый распространенный клещ на территории России: его ареал простирается от северо-западных районов до Дальнего Востока. Взрослые особи таежных клещей активизируются ранней весной и остаются активными до середины лета. Инфицирование людей может происходить в результате присасывания не только самок (справа), но и самцов, которые присасываются на непродолжительное время, и, в редких случаях, нимф, что может оставаться незамеченным. Фото В. Якименко (Омский НИИ природно-очаговых инфекций)
К примеру, недавно были получены экспериментальные доказательства, что пациенты с пост-Лайм синдромом страдают не какими-то психологическими расстройствами, а вполне конкретными поражениями головного мозга. В их крови, а также в восьми отделах мозга было обнаружено повышенное содержание белка, служащего маркером воспалительного процесса. При этом в течение полугода после курса антибиотикотерапии эти люди ощущали сильную слабость, неспособность концентрировать внимание; страдали нарушениями памяти и когнитивных функций (Coughlin, Yang, Rebman et al., 2018). Из-за воспалительных процессов и повреждений, связанных с боррелиозной инфекцией, подобные неврологические симптомы могут сохраняться неделями и месяцами даже после длительного начального курса антибиотиков.
Однако в редких случаях хронического боррелиоза дополнительная антибиотикотерапия все же оказывалась эффективной. Вероятно, у некоторых пациентов в организме после стандартного либо запоздалого или неполного курса лечения действительно могут сохраняться живые боррелии, т. е. речь идет именно о хронической инфекции. Напомним, что лабораторная диагностика боррелиоза сегодня ненадежна. Кроме того, в случае хронического боррелиоза инфекционные агенты могут находиться в основном внутри нейронов, т. е. за гематоэнцефалическим барьером. А диагностические системы обладают низкой чувствительностью и непригодны для использования у пациентов, у которых количество бактерий в крови невелико.
Так что все зависит от ситуации, и в некоторых случаях речь может идти о реальном хроническом инфекционном заболевании, а в некоторых — о развитии пост-Лайм синдрома после перенесенной болезни.
Боррелиоз — причина нейродегенеративных заболеваний?
Группа американских исследователей выдвинула гипотезу о связи между заражением боррелиозом и развитием нейродегенеративных заболеваний. Их натолкнуло на эту мысль сходство симптомов, наблюдаемых на поздних стадиях заболевания болезнью Лайма, с симптомами, характерными для болезни Альцгеймера, болезни Паркинсона и даже аутизма (MacDonald, 2006; Miklossy, 2008, 2015). В пользу этой гипотезы говорит и тот факт, что боррелии, как и их близкие родственники трепонемы — возбудители сифилиса, способны проникать в мозг и приводить к поражениям, характеризующимся как нейроборрелиоз (Lapenta, 2018).
Боррелии были действительно обнаружены в тонких срезах мозга пациентов, умерших от нейродегенеративных заболеваний. По мнению авторов этой работы, биопленки боррелий находились внутри амилоидных бляшек, аналогичных тем, что наблюдаются у пациентов с болезнью Альцгеймера (Miklossy, 2016). Было выдвинуто предположение, что именно иммунный ответ на эти биопленки и приводит к развитию болезни Альцгеймера, при этом человек может быть инфицирован трепонемами или боррелиями задолго до поражения мозга. Однако убедительных подтверждений эти предположения не получили.
Исследования в Национальных институтах здоровья США не выявили маркеров боррелиоза у таких больных. Но главным аргументом стал анализ распространения болезней по территории страны, так как болезнь Лайма, в отличие от нейродегенеративных болезней, встречается лишь в нескольких штатах на Восточном побережье США (Forrester, Kugeler, Perea et al., 2015). Не было получено убедительных данных и о связи боррелиоза с другими нейродегенеративными заболеваниями.
Биосенсор — для клеща, ПЦР — для людей
Одна из главных проблем с клещевым боррелиозом связана с его диагностикой на ранних стадиях развития болезни. Ведь чем раньше можно начать лечение, тем больше будет шансов избежать перехода болезни в хроническую форму.
Сегодня существует прямой метод обнаружения боррелий в крови на ранней стадии развития инфекции. Это ПЦР-диагностика, детекция бактериальной ДНК с помощью полимеразной цепной реакции. Однако простые варианты этого метода недостаточно чувствительны, а высокочувствительные, основанные на комбинации ПЦР и масс-спектрометрии, слишком сложны и дороги для применения в клинике. Недавно американская компания Ceres Nanosciences разработала еще один прямой метод обнаружения боррелий в организме. Для этого используются специальные наночастицы, на которые осаждаются бактериальные молекулы-антигены из больших объемов мочи пациента. После такого концентрирования антигены могут определяться с помощью обычного иммунного анализа (Magni, Espina, Shah et al., 2015).
Команда студентов Московского государственного университета имени М. В. Ломоносова совместно со специалистами из Института молекулярной биологии имени В. А. Энгельгардта РАН (Москва) и других исследовательских организаций приступила к разработке экспресс-диагностики зараженности боррелиозом самого переносчика болезни — иксодового клеща.
До сих пор клеща, снятого с тела, приносят в специализированную лабораторию, где инфекционный агент детектируется с помощью ПЦР или иммуноферментного анализа. Анализ занимает несколько часов и может быть выполнен только в условиях лаборатории. Принцип действия нового биосенсора основан на поиске ДНК боррелий в образце с помощью молекулярных генно-инженерных конструкций, созданных на базе системы, сконструированной из компонентов известного молекулярного комплекса для редактирования генома CRISPR/Cas.
В состав этой бинарной системы входят две молекулы РНК, комплементарные двум соседним последовательностям в бактериальной ДНК. Эти РНК несут два белка, которые являются составными частями фермента бета-лактамазы. Если в исследуемом образце есть ДНК боррелий, РНК свяжутся с ней, и белковые субъединицы сблизятся, сформировав комплекс с ферментативной активностью, в результате чего в присутствии определенного субстрата в растворе будет синтезироваться красящее вещество. Окрашивание раствора можно зарегистрировать с помощью простейшего портативного спектрофотометра.
На сегодня ситуация с хроническим боррелиозом остается тревожной. Слишком много нерешенных вопросов, связанных с диагностикой и рекомендациями по терапии пациентов, заболевших этой клещевой инфекцией.
Один из наиболее спорных вопросов: надо ли спешить с применением антибиотиков после укуса клеща. Среди официальных рекомендаций есть и такая: если клещ присасывался менее чем на сутки, опасности инфекции практически нет. Но все дело в том, что заболевшие боррелиозом порой вообще не помнят контакта с клещом — заразить могут и нимфы, которых можно просто не заметить, и самцы, которые наносят лишь кратковременные укусы. При этом большинство врачей в США и европейских странах считают, что если характерные симптомы заболевания в первые дни после заражения отсутствуют, то и антибиотикотерапию проводить не следует. С этим трудно согласиться, учитывая, что развитие инфекции может привести к долговременным нарушениям работы многих систем организма.
Ответы на все эти вопросы мы получим лишь тогда, когда ученые разберутся со сложными загадками коварной бактерии. До этих пор шарлатаны могут обирать пациентов, а страховые компании — уклоняться от выплат больным. Но для проведения полноценных научных исследований клещевых инфекций, разработки эффективных средств диагностики и терапии требуется достаточное финансирование.
В США сами больные совместными усилиями пытаются через Конгресс повлиять на ситуацию с финансированием работ по изучению болезни Лайма. Подобное движение в свое время возникло из-за эпидемии СПИДа, и в результате были приняты действенные меры по организации интенсивных исследований ВИЧ. И сегодня эта болезнь уже не является смертельным приговором. Если приложить аналогичные усилия к изучению клещевого боррелиоза, то очень скоро он уже не будет представлять такую угрозу для нашего здоровья, как сейчас.
Болезнь Лайма (клещевой боррелиоз) впервые была описана в 1975 году в городе Олд-Лайм, Коннектикут, откуда и получила свое название. В 1982 году Вилли Бургдорфер открыл причину этого заболевания - им оказалась бактерия рода боррелия типа спирохет. Эта бактерия была названа его именем - Borrelia burgdorferi. То, что менее известно, это что Вилли Бургдорфер имел прямое отношение к созданию этой болезни в качестве бактериологического оружия.
Ниже представлены некоторые выдержки из книги Bitten: The Secret History of Lyme Disease and Biological Weapons, которая была опубликована в мае 2019-го. Автор, Kris Newby - научный писатель из Стэнфордского медицинского факультета. Она и ее муж несколько лет страдали болезнью Лайма.

Вилли Бургдорфер
Вилли Бургдорфер родился в 1925 году в Базеле, и получил докторскую степень в швейцарском институте тропической медицины, где он изучал зоологию, паразитологию и бактериологию. Его академическим наставником был профессор Рудольф Гейги, который и основал этот институт в 1943 году. Семья Гейги основала в 18 веке химическую компанию Geigy AG, которая впоследствии стала фармацевтической. В наши дни она называется Новартис.
После окончания учебы Гейги предложил Бургдорферу и другому студенту две позиции для постдокторантуры. Первая была в Сардинии, и включала в себя тестирование нового инсектицида под названием ДДТ, который разработала компания Гейги. Вторая позиция была в Лаборатории Скалистых гор в штате Монтана. Оба студента предпочитали, разумеется, теплое местечко в Сардинии, с его пляжами и итальянской едой, а не американскую глухомань, и Гейги подкинул монетку. Вилли проиграл.
В 1951 году он приехал в Хамильтон, Монтана, где в конце 19 века была обнаружена лихорадка Скалистых гор, после чего там был основана лаборатория с тем же названием. Лаборатория, среди прочего, разрабатывала и производила вакцины от лихорадки скалистых гор, энцефаломиелита, желтой лихорадки и других болезней, которые передаются от животных.
Один из проектов Вилли заключался в разработке более эффективных способов искусственного кормления клещей потенциальными биологическими агентами. Он делал это путем принудительного кормления их через стеклянные трубки, содержащие болезнетворные бактерии и вирусы, такие как туляремия, тиф, бешенство, ку-лихорадка и другие.

Насильственное кормление клещей возбудителями болезней
У этого безумства была цель. В большинстве случаев микробы из одного региона не могут развиваться внутри клещей из другого региона, потому что микробам и клещам требуется много поколений для развития взаимовыгодных отношений, когда один вид не убивает другой. Когда Вилли находил совместимую пару, она добавлялась в список потенциального биологического оружия. Разработчики оружия искали клеща, который не вызовет подозрений вражеской страны, но в случае их нашествия, жители этой страны не имели бы естественного иммунитета против вызываемой клещем болезни.
В середине 50-х годов Вилли проводил много времени в армейской лаборатории биологического оружия в Форт-Детрик, Мэриленд, где он познакомился с Джеймсом Оливером. Оливер работал над программой по сбрасыванию зараженных клещей из самолетов. Вместе с Вилли они размышляли над методами увеличения скорости размножения клещей, чтобы программа не отставала от военных потребностей. Однако они так и не смогли заставить клещей откладывать больше яиц. [1]

Вилли Бургдорфер работает с африканскими клещами

Разработка Вилли Бургдорфера, позволяющая кормить голодных клещей лабораторными мышами

Блоха с комками бактерий чумы, которые блокируют ей пищевод

Неконтролируемые выпуски клещей, 1966–1969
Вилли рассказывал, что агенты ФБР допрашивали его два раза насчет пропажи биологического оружия. Может ли вспышка на Лонг-Айленде быть связана с биологическим выбросом иностранной державы? Как бы невероятно это ни казалось, Вилли был бы главной мишенью для советских шпионских вербовщиков. У него был легкий доступ к биологическому оружию, он мог часто путешествовать в Европу, не вызывая подозрений, он говорил на трех языках, и у него были финансовые проблемы, которые могли быть использованы иностранной державой. Кроме того, у него была большая сумма денег, спрятанная на банковском счете, о котором его три наследника ничего не знали.
Автор книги также сняла документальный фильм о болезни Лайма Under Our Skin (2008), и его продолжение - Under Our Skin 2: Emergence (2014). В фильмах обсуждается вопрос хронической формы болезни Лайма, которая не признается ортодоксальной медициной. Врачи, которые выписывают антибиотики хроническим больным и вылечивают их, подвергаются гонениям и некоторые из них теряют лицензию. Имеются также свидетельства того, что болезнь Лайма передается половым путем и внутриутробно.
Для этого фильма она сделала запрос FOIA (закон о свободе информации), из которого выявилось, что большинство авторов руководств по диагностике и лечению Лайма 2006 года имели прямые или косвенные коммерческие интересы, связанные с болезнью Лайма. Давая определение болезни и одобряя тесты или вакцины, патентами на которые они обладали, они и их учреждения заработали больше денег.
Теперь, однако, признание Вилли добавило еще одну причину, по которой CDC приуменьшает количество случаев болезни Лайма. Возможно, правительственные чиновники знали, что болезнь вызывается не только боррелией, но и другим патогеном, возможно биологическим оружием, и хотят это скрыть.
В 1983 году, когда Вилли ополаскивал поддоны кроличьих клеток, моча инфицированных болезнью Лайма кроликов брызнула ему в глаза. Несколько недель спустя он обнаружил на теле пять кольцевидных эритем (первый симптом болезни Лайма). Несмотря на это, антитела к Лайму у него не обнаружили. Через 3 года он вышел на пенсию. В ноябре 2014 года Вилли умер от осложнений болезни Паркинсона.
Армия США провела тысячи экспериментов по изучению использования клещей и клещевых заболеваний в качестве биологического оружия, и в некоторых случаях эти биологические микроорганизмы остались в окружающей среде. Правительство должно рассекретить детали полевых испытаний биологического оружия, чтобы мы могли начать восстанавливать ущерб, который эти патогенные микроорганизмы наносят людям и животным.
Откуда взялся этот адский коктейль клещевых болезней? Если вы верите Вилли Бургдорферу - а я верю - это был умышленный выброс или авария, эксперимент с непреднамеренными последствиями для окружающей среды. Тем не менее, после пяти лет исследований я не смогла найти поддающиеся проверке документы, подтверждающие инцидент на Лонг-Айленде. Я не знаю, почему Вилли отказался полностью раскрыть детали до своей смерти.
Прошло пятьдесят лет с тех пор, как началась таинственная вспышка клещевых заболеваний, и для ее устранения потребуются чрезвычайные усилия. Наша медицинская система по-прежнему не хочет диагностировать и лечить болезнь Лайма и сопутствующие инфекции. С тех пор, как болезнь Лайма была обнаружена, не было введено существенно новых протоколов диагностики или лечения. Исследования клещевых заболеваний не получают достаточного финансирования. Если эта вспышка была вызвана аварией, мы должны о ней знать. Если это был враждебный акт со стороны другого государства, то он показывает, насколько мы не готовы к будущим атакам.
П оражение глаз при болезни Лайма считается достаточно редким явлением. Болезнь Лайма - мультисистемное инфекционное заболевание, вызываемое спирохетой Borrelia burgdorfery. Известно три группы боррелий: собственно B. burgdorfery, B. garinii, B. afzelii. В Европе боррелиоз может быть вызван любой из указанных спирохет. Спектр клинических проявлений болезни, называемой также боррелиозом Лайма, варьирует от явлений эритемы мигранс до артритов, неврологических и кардиологических расстройств. Первый случай внутриглазного боррелиоза был описан в 1985 г.
В 11% случаев на стадии ранней диссеминации инфекции у больных обнаруживаются явления конъюнктивита, однако на этой стадии больные редко попадают к окулисту. К ранним проявлениям относят также такие нейроофтальмологические расстройства, как парез окуломоторных нервов и неврит зрительного нерва, что связано с проникновением спирохет через гематоэнцефалический барьер уже через неделю после инфицирования. На поздних стадиях (через месяцы и годы после начала заболевания) развиваются кератиты и внутриглазные воспалительные поражения. При биомикроскопическом исследовании выявляются весьма необычные признаки, например, рубцовые инфильтраты роговицы, атипические парспланиты, витрииты по типу паутины, выраженные отеки диска зрительного нерва, изменения, подобные пигментному ретиниту. Многие изменения напоминают таковые при сифилитических поражениях глаза.
Глазной боррелиоз распознается крайне редко вследствие позднего появления симптомов и частых случаев серонегативной реакции ELISA.
Можно заподозрить боррелиоз в случае необычной клинической картины внутриглазного воспалительного процесса, но точный диагноз ставится с помощью иммуноблоттинга или путем обнаружения ДНК боррелии. Скрининг всех больных увеитом на предмет выявления боррелиозной этиологии процесса нецелесообразен. При кератитах возможно успешное применение антибиотиков per os, но при наличии пареза окуломоторных нервов и внутриглазных воспалительных изменений требуется назначение антибиотиков внутривенно. Обычно используют цефтриаксон (2 г/сут) или цефотаксим (6 г/сут). Передозировка цефтриаксона может привести к развитию осложнений со стороны желчевыделительной системы.
Karma A, Mikkila H. Ocular manifestations and treatment of Lyme disease. Current Opinion in Ophthalmology 1996;7(111):7-12.
НОВЫЕ ВОЗМОЖНОСТИ В ЛЕЧЕНИИ РЕТИНОБЛАСТОМЫ
И. Лоскутов
I. Loskutov
П рогноз для зрения и жизни больных с ретинобластомой значительно улучшился в последние десятилетия вследствие раннего выявления заболевания и совершенствования методов лечения. Сто лет назад ретинобластома почти всегда приводила к гибели больного. Ведение больного с ретинобластомой должно быть комплексным. Первой и главной целью лечения было и остается сохранение жизни больного, в известной степени вторичным оказывается вопрос сохранения глаза и зрения. Основными методами лечения данной опухоли являются: энуклеация глазного яблока, облучение, лазерное воздействие, криоаппликации, термотерапия, химиотерапия, хеморедукция, хемотермотерапия и экзентерация орбиты.
Проведение энуклеации показано при развитой стадии заболевания, а также при инвазии опухоли в зрительный нерв, хориоидею или орбиту. При вторичной глаукоме, вовлечении плоской части цилиарного тела или передней камеры также производится удаление глазного яблока.
Ретинобластома относится к опухолям, чувствительным к воздействию ионизирующего излучения. Результаты такого лечения во многом зависят от размеров и локализации опухоли, а также возникновения осложнений вследствие облучения (например, ретинопатии). Аргоновая или ксеноновая лазерная фотокоагуляция может быть успешно применена при лечении опухолей маленького размера, расположенных в заднем полюсе. Криотерапия используется для лечения маленьких опухолей, расположенных периферично к экватору.Термотерапия - метод воздействия на опухолевую ткань ультразвуком, микроволновым или инфракрасным излучением. Целью термотерапии является достижение температурного воздействия от 42 до 47 ° С, что ниже порога коагуляции. Комбинация термотерапии и химиотерапии определяется как хемотермотерапия, которая наиболее эффективна при опухолях, расположенных в заднем полюсе глазного яблока.
Хеморедукция - метод уменьшения объема опухолевой ткани для лучшей фокусировки последующего терапевтического воздействия, что делает его менее опасным.
Если заболевание распознано лишь в развитой стадии, на что указывает вовлечение тканей орбиты, то для спасения жизни больного необходимо проведение экзентерации орбиты с последующим курсом химиотерапии и облучения.
Shields C, Shields J, Potter P. New treatment modalities for retinoblastoma. Current Opinion in Ophthalmology 1996;7(111):20-6.

03.03.1997 НЕВРОЛОГИЯ
МЫШЕЧНЫЕ НАРУШЕНИЯ ПРИ ГОЛОВНОЙ БОЛИ НАПРЯЖЕНИЯ ВЛИЯНИЕ ИНСУЛЬТА И ЕГО ПРОФИЛАКТИКИ НА КАЧ.
Для цитирования: Антелава О.А., Ушакова М.А., Ананьева Л.П. и др. Клиническая манифестация нейроинфекции при болезни Лайма на фоне иммуносупрессивной терапии. РМЖ. 2014;7:558.
Лайм-боррелиоз (ЛБ), или болезнь Лайма (Lyme disease), Лаймовский боррелиоз, или иксодовый клещевой боррелиоз – это инфекционное природно-очаговое трансмиссивное мультисистемное инфекционное полиорганное воспалительное заболевание, вызываемое спирохетами рода Borrelia, переносчиками которых являются иксодовые клещи. ЛБ характеризуется стадийностью, склонностью к хронизации и рецидивирующему течению [1].
Особое место в клинической картине болезни занимает поражение нервной системы, или нейроборрелиоз, частота выявления которого зависит от географической зоны, наблюдается в России у 10–60% больных [5]. Колебание в частоте его развития связано с особенностью геновидов боррелии и недостаточной изученностью проблемы в ряде регионов. Наиболее высокая частота поражения нервной системы наблюдается на Северо-Западе и в Центре России – 43–64%.
Широкий спектр клинических симптомов и синдромов при нейроборрелиозе объясняется способностью Воrreliа burgdorferi поражать все отделы нервной системы на любой стадии болезни [6, 7]. При нейроборрелиозе описаны:
- сенестонейропатии, нейропатии и радикулопатии;
- поражения черепно-мозговых нервов (ЧМН): моно(поли)неврит (лицевого, языкоглоточного, блуждающего нервов, зрительного, слухового нервов);
- синдром Банавартца (менингорадикулоневрит);
- периферические невриты, плексит. У 1/3 больных выявляется периферический судорожный синдром (тремор кистей рук и судороги в мышцах голеней);
- миелит;
- миелорадикулоневрит;
- лимфоцитарный менингит;
- очаговый или диффузный энцефалит;
- пароксизмальные расстройства сознания;
- эпилептические припадки, церебральный васкулит;
- прогрессирующий энцефаломиелит.
Хронический боррелиоз, или III стадия ЛБ, развивается у 10% больных через 6 мес. – 2 года после острого периода [8]. Наиболее изученными в этом периоде являются хронические неврологические синдромы, напоминающие по срокам развития третичный период нейросифилиса, названные хроническим нейроборрелиозом. При этом развиваются хронический энцефаломиелит, спастический парапарез, некоторые расстройства памяти, деменция, хроническая аксональная полирадикулопатия. Эта стадия характеризуется чередованием ремиссий и рецидивов, однако в некоторых случаях болезнь имеет непрерывно рецидивирующий характер.
Частота развития хронических форм нейроборрелиоза, по данным разных авторов, составляет от 4 до 20% всех больных ЛБ. Однако имеются данные о том, что реальный показатель может быть значительно выше и после перенесенной безэритематозной формы заболевания достигать 85% [9–11]. Считается, что диагностика этих форм заболевания затруднена в связи с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [12].
Для хронической нейроинфекции наиболее характерно постепенное поражение нервной системы с развитием патологического процесса, имитирующим другие нозологические формы, в частности рассеянный склероз, рассеянный энцефаломиелит. Большинство больных c хронической нейроинфекцией не указывают на предшествующую мигрирующую эритему или укус клеща. Полагают, что укусы самцов и незрелых особей клещей часто проходят незаметно для людей [13]. Кроме того, могут встречаться безэритематозные формы ЛБ в 2–20% случаев [14–15]. Известно, что в 6–8% случаев возможно субклиническое течение боррелиозной инфекции, при этом отсутствуют клинические проявления болезни. Отсутствие симптомов болезни не исключает развития в последующем II и III стадий заболевания. Все это является фактором риска развития хронической нейроинфекции, т. к. обусловливает отсроченную диагностику [16–18]. Латентный период инфекции при позднем нейроборрелиозе может составлять от 1,5 до 17 лет. Столь длительное латентное течение заболевания связывают с возможным переходом боррелии в неактивные L-формы с последующей их активацией [19–21].
Впервые хронический боррелиозный энцефаломиелит был описан R. Ackermann et al. в 1985 г. [23]. Позже была изучена группа из 44 больных, у которых встречались преимущественно церебральные проявления, напоминающие мультифокальный энцефалит, или спинальные симптомы. В настоящее время частота выявления энцефаломиелита при ЛБ невысока и составляет в среднем 4–5% от всех случаев нейроборрелиоза. Хроническое течение ЛБ в России изучено мало, что связано с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [24].
В литературе выделяют разные варианты течения нейроинфекции при хроническом ЛБ, включая прогрессирующий энцефаломиелит, хроническую радикулополиневропатию, хронический лимфоцитарный менингит, церебральный васкулит, энцефалопатию и др. Прогрессирующий энцефаломиелит при ЛБ нередко имитирует рассеянный склероз [25, 26]. Согласно наблюдению ряда исследователей, при хроническом ЛБ процесс носит генерализованный характер поражения нервной системы, несмотря на то, что клинически определяется изолированное поражение какого-либо нерва [27, 28]. Пo данным магнитно-резонансной томографии (МРТ) отмечаются поражения очагового характера преимущественно белого вещества головного мозга [29], которые могут определяться после длительного латентного периода.
Ведущие симптомы прогрессирующего боррелиозного энцефаломиелита – это спастические пара- и тетрапарезы, атаксия, дисфункция тазовых органов, когнитивные расстройства в виде снижения памяти и концентрации внимания. Больше чем у 50% больных ЛБ с поражением ЦНС наблюдаются сопутствующее поражение корешков и периферических нервов, множественные парезы черепных нервов, преимущественно вестибулокохлеарного.
Диагностические критерии хронической нейроинфекции включают:
- Наличие признаков поражения ЦНС при боррелиозе после перенесенных I и II стадий заболевания.
- Развитие неврологической симптоматики позднее 6 мес. от появления мигрирующей эритемы и/или факта присасывания клеща или сохранение симптоматики на протяжении более 6 мес.
- Обнаружение умеренных или высокоположительных титров антител к Borrelia burgdorferi в сыворотке крови больного при двукратном обследовании.
- Исключение другой этиологии патологического процесса, протекающего в нервной системе, который мог явиться причиной развития имеющейся у больного клинической симптоматики.
Поражение нервной системы на поздних стадиях ЛБ у 40% больных бывает изолированным и почти в 60% сочетается с экстраневрональными проявлениями ЛБ [6, 30]. Наиболее часто отмечаются поражения опорно-двигательного аппарата в виде артралгии, миалгии и других проявлений. В связи с развитием ревматических синдромов до 30% больных с ЛБ ежегодно обращаются к ревматологам.
Особая сложность диагностики наблюдается при отсроченном развитии поражения нервной системы, когда трудно определить связь развития поражения нервной системы с фактом присасывания клеща, особенно в случае безэритематозных форм. Также позитивность по антителам к Borrelia burgdorferi в ликворе выявляется только у 18% больных ЛБ [31–35].
В патогенезе хронического нейроборрелиоза играют роль проникновение инфекции и лимфоцитов в ткани нервной системы, чему способствуют активация или повреждение эндотелиальных клеток, нарастание уровня растворимой формы одной из основных клеточных молекул адгезии – ICAM-1, металлопротеиназы-9 [32]. В ряде исследований имеются доказательства развития аутоиммунных процессов в виде обнаружения антител, направленных против протеинов Borrelia burgdorferi и белков нервной ткани, вызывающих воспаление и демиелинизацию [33]. Высказывается предположение о возможном участии боррелии в инициации аутоиммунного процесса в результате активации миелин-специфичных Т-клеток и обнаружения аутореактивных антител к миелину и компонентам миелина при ЛБ [34]. По мере прогрессирования заболевания расширяется спектр антител ко многим белкам боррелии, что может приводить к перекрестному реагированию иммунной системы с антигенами боррелии и макроорганизма. Ведущая роль в этом отводится длительной персистенции возбудителя в тканях и его внутриклеточному расположению [35].
Комплексная оценка эпидемиологических, клинико-лабораторных и инструментальных данных, отражающих поражения нервной системы при хроническом ЛБ, демонстрирует отличие клинической картины хронической нейроинфекции в России от таковой в Европе в виде более частого поражения периферической нервной системы (радикулополиневропатии) и энцефалопатии, а также отсутствия сочетания полиневропатии с хроническим атрофическим акродерматитом.
Факторами риска развития хронического нейроборрелиоза названы: множественные присасывания клещей, отсутствие у больных мигрирующей эритемы на месте присасывания клеща в острый период ЛБ, раннее развитие признаков диссеминации, отсроченный и неполный курс лечения в острый период заболевания.
Спектр редких проявлений хронического нейроборрелиоза включает изолированное поражение черепных нервов, множественные мононевропатии, церебральный васкулит, синдромы паркинсонизма и бокового амиотрофического склероза, описан миастеноподобный синдром как проявление хронического ЛБ [36].
Представляют клинический интерес особенности течения хронической микст-инфекции ЛБ с клещевым энцефалитом и эрлихиозом, анаплазмозом. Так, в единичных случаях возможно хроническое течение клещевой микст-инфекции с характерными клинико-лабораторными проявлениями данных заболеваний. Показано, что в единичных случаях возможно хроническое течение клещевого энцефалита и ЛБ с типичными клиническими проявлениями последних. В случае возможной хронической микст-инфекции ЛБ и эрлихиоза по сравнению с изолированным течением ЛБ преобладает системность проявлений в сочетании с общеинфекционным синдромом и изменением лабораторных показателей крови (лейкопения, повышение уровня трансаминаз).
Диагностика и течение ЛБ в целом и нейроборрелиоза в частности при ревматических заболеваниях осложняется некоторым атипизмом клинический картины и скоростью прогрессирования ее проявлений, связанных со скомпрометированностью иммунной системы этой группы пациентов на фоне терапии высокими дозами глюкокортикоидов (ГК) и цитостатиками.
Клинический случай
Пациент Г., 1972 г. р. Анамнез болезни: считает себя больным с июля 2013 г., когда без объективной причины возникли повышение температуры до 37,4°С, параорбитальный отек, первые признаки мышечной слабости, утомляемость, боли в области правого тазобедренного сустава. При обследовании (июль 2013 г.) в общем анализе крови: гемоглобин – 148 г/л, скорость оседания эритроцитов (СОЭ) – 8 мм/ч, лейкопения – 2,82х109 (норма 4,0–9,0), тромбоцитопения, аспартатаминотрансфераза (АСТ) – 49 Ед/л (норма до 35 Ед/л), аланинаминотрансфераза (АЛТ) – 26,2 Ед/л, показатели креатинфосфокиназы (КФК) не исследовали. Белковые фракции: альбумины – 57,3%, (норма 55,7–66,1%), α1 – 6,3% (норма 2,9–11,8%), α2 – 9,1% (норма 7,1–11,8%), β1 – 5,5% (норма 4,7–7,2%), β2 – 5,9% (норма 3,2–6,5%), γ – 15,9% (норма 11,1–18,8%). Общий анализ мочи – без особенностей.
С августа 2013 г. – нарастание параорбитального отека, эритема на лице, груди (в зоне декольте), шее, лихорадка, общая слабость, утомляемость, появление признаков мышечной слабости преимущественно нижних конечностей. При обследовании в сентябре 2013 г. впервые выявлено повышение КФК до 841 Ед/л, лактатдегидрогеназы (ЛДГ) – до 657 Ед/л, креатинина – до 118 мкмоль/л (61–115), сохранялись тромбоцитопения (150х109) и лейкопения (2,8х109).
С учетом наличия в клинической картине параорбитального отека, эритемы на лице и в зоне декольте, проксимальной мышечной слабости, миопатических изменений по данным игольчатой электромиографии, повышения уровня КФК у больного диагностирован дерматомиозит (ДМ), начата терапия ГК в дозе 40 мг/сут, на фоне которой отмечены нормализация температуры тела и уменьшение отека вокруг глаз, снижение уровня КФК, АСТ, АЛТ, нормализации уровня лейкоцитов и тромбоцитов. Однако через 2 нед., на фоне быстрого снижения ГК, при достижении дозы преднизолона 30 мг/сут вновь отмечались возобновление лихорадки, усиление выраженности параорбитального отека, появление и нарастание признаков язвенно-некротического васкулита параорбитальной области (рис. 1 а, б). В связи с обострением заболевания и нарастанием признаков язвенно-некротического васкулита параорбитальной области было назначено повышение дозы ГК до 60 мг/сут, к терапии добавлен циклофосфамид 1000 мг в сочетании с метилпреднизолоном 500 мг в/в капельно 1 р./мес.
За период наблюдения пациенту проведен онкопоиск, включающий КТ грудной клетки, консультации специалистов, в т. ч. уролога – патологии не выявлено. Тогда же (до начала терапии циклофосфамидом в октябре 2013 г.) больному впервые выполнена МРТ головного мозга, каких-либо изменений не выявлено.
На фоне вышеуказанной терапии наблюдались: нормализация температуры тела, заживление язвенно-некротических изменений (рис. 2), нарастание мышечной силы, снижение КФК – 145 Ед/л, ЛДГ– 256 Ел/л, АСТ – 26 Ед/л, АЛТ – 35 Ед/л. Показатели гемоглобина и СОЭ, как и в начале заболевания, сохранялись в пределах нормы.
В январе 2014 г. проведена повторная МРТ головного мозга, при которой выявлено появление множественных инфильтративных очагов в кортикальном слое лобных областей, левой теменной области, супраорбитальный области, признаков отека мозга, нарушение гемодинамики (рис. 4 а–г).
Обращали на себя внимание высокие титры к Borrelia burgdorferi: IgМ – 45,0 Ед/мл (норма 12–17), IgG – 78,7 Ед/мл (до 15), однако исследование спинномозговой жидкости показало отрицательный результат.
Зараженность эрлихиозом и анаплазмозом исключена в лабораторном обследовании.
Таким образом, с учетом неоднократно подтвержденной в динамике позитивности по антителам к Borrelia burgdorferi при проведении как иммуноферментного анализа, так и методики иммуночипа, МРТ- и клинической картины очагового демиелинизирующего поражения ЦНС, факта пребывания пациента в течение более чем 2-х лет в эндемичном районе (в центре европейской части России) и после исключения других причин патологического процесса, протекающего в нервной системе, который мог бы явиться причиной развития имеющейся клинической симптоматики, у больного был диагностирован ЛБ III стадии с поражением нервной системы по типу нейроборрелиоза, наиболее вероятно в виде энцефаломиелита.
Полученные результаты обследования потребовали коррекции лечения: циклофосфамид был отменен, начато снижение дозы ГК и подключение антибактериальной терапии: цефтриаксон 4,0 г/сут в/в капельно № 30, а также ипидакрин 20 х 2 р./сут – 1 мес., тиоктовая кислота 600 мг/сут – 1 мес., витамин Е 400 мг/сут.
В настоящее время на фоне вышеуказанной антибактериальной терапии, приема преднизолона 40 мг/сут (снижение дозы продолжает) и отмены циклофосфамида отмечена стабилизация клинической картины, некоторое уменьшение выраженности амимии и признаков полинейропатии нижних конечностей.
Диагностическая и терапевтическая особенность ведения пациента обусловлена сложностью проведения дифференциальной диагностики. Так, с одной стороны, присутствие в клинической картине выраженного язвенно-некротического васкулита, энантемы, лихорадки, неоднократно выявляемых до лечения ГК лейкопении, тромбоцитопении, требовали исключения прежде всего системной красной волчанки, а также системного васкулита, однако отрицательные результаты анти-ДНК, антинуклеарного фактора, Sm, р-АNCA в иммунологическом анализе крови не позволили с уверенностью говорить об обсуждаемых диагнозах. С другой стороны, с учетом множественного прогрессирующего поражения головного мозга в круг дифференциального диагноза были включены рассеянный склероз и прогрессирующая мультифокальная лейкоэнцефалопатия. Последняя является прогрессирующим демиелинизирующим заболеванием ЦНС, вызываемым реактивацией латентно существующего JC-вируса семейства Papovaviridae, рода Polyomavirus и проявляющимся на фоне иммуносупрессии: СПИД, лимфомиелопролиферативные заболевания, злокачественные опухоли, трансплантация органов и аутоиммунные воспалительные заболевания [37]. При анализе клинико-лабораторной картины, данных анамнеза вопрос диагноза был решен в пользу ЛБ, о чем свидетельствовали картина МРТ-изменений (консультация по поводу результатов МРТ головного мозга в Центре неврологии, г. Москва), наличие высоких титров классов IgG и IgМ к Borrelia burgdorferi, а также клинически-положительная динамика неврологического статуса на фоне антибактериальной терапии.
Остается актуальным вопрос причинно-следственного диагноза. Можно ли рассматривать дебют ДМ как самостоятельный, с последующей манифестацией нейроинфекции на фоне иммуносупрессивной терапии? Или латентно протекающий ЛБ послужил триггером для ревматического заболевания?
Так, на сегодняшний день наиболее вероятным остается диагноз ДМ (параорбитальный отек, эритема в зоне декольте, на шее, язвенно-некротический васкулит, проксимальная мышечная слабость, первично-мышечные электромиографические изменения, повышение КФК).
Клещевой иксодовый боррелиоз (болезнь Лайма) III стадия: нейроборрелиоз, изменения ЦНС (по данным МРТ – очаговые изменения в кортикальном слое лобных областей, левой теменной области, супраорбитальной области), поражение ЧМН, периферическая полинейропатия; миопатический синдром, высокая серопозитивность по антителам к боррелиям классов IgG и IgМ.
Описанный случай интересен не только как клиническое наблюдение – манифестация латентно протекающего ранее ЛБ в виде быстропрогрессирующей нейроинфекции на фоне иммуносупрессивной терапии. Представляют интерес также широта дифференциально-диагностического поиска, осложненного некоторым атипизмом дебюта и течения ДМ, и начало наблюдения авторами за больным уже на фоне лечения ГК.
Что такое болезнь Лайма? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Болезнь Лайма (иксодовый клещевой боррелиоз) — опасное инфекционное трансмиссивное заболевание острого или хронического течения, вызываемое бактериями рода Borrelia, которые поражают кожу, суставы, сердце и нервную систему. Клинически характеризуется полиморфизмом проявлений и без лечения приводит к стойкому нарушению жизнедеятельности и инвалидизации человека.
Возбудитель боррелиоза
род — Borrelia (тип Спирохет)
виды — более 10, из них наиболее этиологически значимые Borrelia burgdorferi (наиболее распространён), Borrelia azelii, Borrelia garinii.
Грамм-отрицательны. Культивируются в видоизменённой среде Kelly (селективная среда BSK-KS). Любит жидкие многокомпонентные среды. Жгутиконосцы. Небольшого диаметра, что позволяет им обходить большинство бытовых бактериальных фильтров. Borrelia burgdorferi состоит из плазмоцилиндра, покрытого клеточной мембраной, имеющей в составе термостабильный ЛПС. Температурный оптимум — 33-37°С. Сходствует со штопорообразной извитой спиралью. Вид завитков неравномерный, вращательные движения медленные.
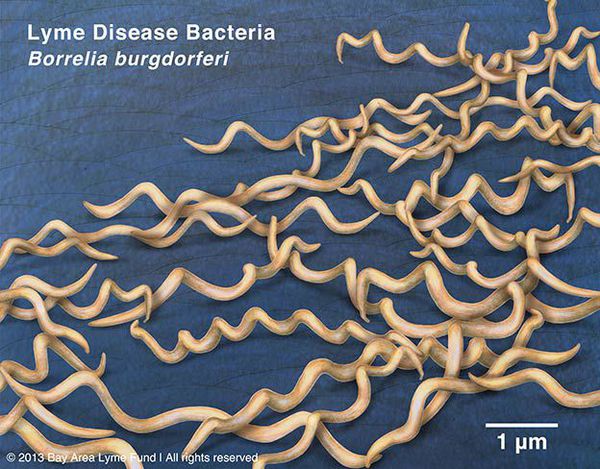
Группы антигенов: поверхностные Osp A, Osp B, Osp С (обуславливают различия штаммов). Этиологические агенты генетически гетерогенны (то есть комплекс Borrelia burgdorferi sensu lato — вызывает группу этиологически самостоятельных иксодовых боррелиозов).
Хорошо красятся анилиновыми красителями. Неплохо выдерживают низкие температуры. Фенол, формалин, спирт и другие обеззараживающие вещества, а также ультрафиолетовое излучение вызывают быструю гибель. Является внутриклеточным паразитом. [2] [3] [5]
Эпидемиология
Природно-очаговое заболевание. Источник инфекции — различные животные (олени, грызуны, волки, домашние и дикие собаки, еноты, овцы, птицы, крупный и мелкий рогатый скот и другие). Переносчики — иксодовые клещи (таёжный и лесной): Ixodes demine (США), Ixodes ricinus и Ixodes persulcatus (Россия и Европа).

Род Ixodes — это темно-коричневый клещ с твёрдым, чуть больше булавочной головки телом, похож на корочку на ссадине или кусочек грязи. В тканях животных возбудитель присутствует в очень небольшом количестве (сложно обнаружить). Исходя из географии заболевания боррелии расселяются с мигрирующими птицами, прикрепившись к ним. Возможен симбиоз нескольких видов боррелий в одном клеще. Возбудитель передаётся среди клещей трансовариальным способом, то есть от самки к потомству. Живут дклещи о 2 лет, часто находятся на кустарниках не выше одного метра от земли. Перезимовать способны только самки, самцы погибают после спаривания. В эндемичных районах заражённость клещей достигает 70%, в остальных регионах — от 10%. Высокая частота инфицированности клеща не является постулатом высокой заболеваемости людей после укуса, так как лишь у немногих клещей боррелии находятся в слюнных железах. Сосание крови осуществляется длительное время и боррелии поступают в ткани не сразу, поэтому ранее удаление клеща существенно снижает риск передачи.
Заразен ли боррелиоз
Механизмы передачи инфекции:
- трансмиссивный (инокуляция — при укусе; очень редка контаминация — при втирании остатков клеща в рану);
- вертикальный (трансплацентарно — от матери к плоду);
- алиментарный путь (через молоко больного животного).
Между людьми боррелиоз не распространяется (исключая вертикальный механизм). Через грудное молоко, слюну и половые жидкости боррелиоз не передаётся.
Распространённость
География распространения достаточно широкая: США, Прибалтика, лесная Европа, Северо-Запад и Центр России, Предуралье, Урал, Западная Сибирь, Дальний Восток.
Сезонность весенне-летняя и осенняя (то есть во время тепла, когда клещи активны). Иммунитет нестерильный. Повторные заболевания возможны через 5-7 лет. [1] [4]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Лайма
Инкубационный период в различных источниках колеблется от 1 до 50 дней (в практической деятельности следует придерживаться срока 1-30 дней).
Синдромы заболевания:
- общей инфекционной интоксикации;
- эритемы (покраснение кожи);
- артрита;
- регионарной лимфаденопатии (увеличение лимфоузлов);
- поражения нервной системы;
- поражения сердечно-сосудистой системы;
- гепатолиенальный (увеличение печени и селезёнки).
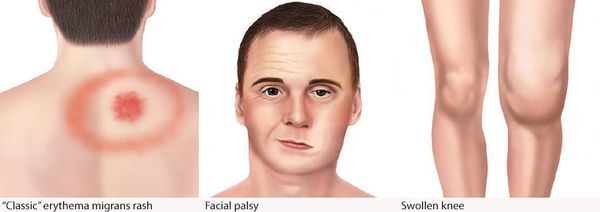
Периоды развития заболевания имеют достаточно условный характер, в основном ограничены лишь временными рамками:
- ранний (локализованная и диссеминированная стадии);
- поздний;
- резидуальный.
Локализованная стадия раннего периода
Начинается остро или подостро с невысокой лихорадки (субфебрильная температура тела — 37,1-38°C), головной боли, слабости, дискомфорта в мышцах и суставах. Редко бывает тошнота и рвота. Катар (воспаление) верхних дыхательных путей возникает очень редко, иногда бывает регионарная лимфаденопатия, гепатолиенальный синдром.
Самым ярким признаком данной фазы болезни (однако не всегда!) является выход на поверхности кожи мигрирующей кольцевидной эритемы (патогномоничный признак заболевания). Вначале в месте локализации укуса клеща возникает первичный аффект (покраснение 2-4 мм красноватого цвета), затем появляется пятно или папула интенсивного розово-красного цвета, в продолжении нескольких суток распространяющаяся во все стороны на много сантиметров в диаметре. Края пятна становятся чётко очерченными, ярко-красными, чуть возвышающимися над уровнем неизменённой кожи. Чаще в центре пятно медленно бледнеет, становится цианотичным (синеет), и образование приобретает характерный вид кольцевидной эритемы овальной или округлой формы.

В месте локализации эритемы не исключается зуд, слабая болезненность. При отсутствии антибиотикотерапии эритема визуализируется в течение нескольких дней, при их отсутствии может держаться до двух месяцев и более. В исходе — слабая непродолжительная пигментация, шелушение. У части больных появляется несколько эритем меньшего диаметра (обычно в более поздний период).
Диссеминированная стадия раннего периода
Эта стадия начинается на 4-6 неделе болезни (при отсутствии профилактической и лечебной терапии предшествующего периода). В этот период происходит угасание предшествующей симптоматики (синдрома общей инфекционной интоксикации, лихорадки и эритемы). Выявляются неврологические нарушения:
- мягкотекущий энцефалит,
- мононевропатии,
- серозные менингиты,
- энцефаломиелит с радикулоневритическими реакциями,
- лимфоцитарный менингорадикулоневрит, характеризующийся болями в месте укуса, сильными корешковыми болями с нарушением чувствительности и двигательной функции шейного и грудного отделов спинного мозга — так называемый синдром Бэннуорта, включающий триаду: корешковые боли, периферический парез (чаще лицевого и отводящего нервов) и лимфоцитарную клеточную реакцию с содержанием клеток от 10 до 1200 в мм3) при выполнении люмбальной пункции.
Возможно поражение сердечно-сосудистой системы — кардиалгии, сердцебиения, повышение артериального давления, миокардиты, AV-блокады (нарушения передачи нервного импульса в проводящей системе сердца).
Иногда бывают поражения кожи (уртикарные и другие высыпания). Может наблюдаться боррелиозная лимфоцитома (доброкачественный лимфаденоз кожи) — синюшно-красный кожный инфильтрат с лимфоретикулярной пролиферацией, преимущественно располагающийся на мочке уха или соске груди. Редко возникают поражения глаз в виде конъюнктивита, хориоидита, ирита.

Не исключаются лёгкие гепатиты, нарушение работы почек.
Поражения суставов в виде реактивного артрита (в основном крупные суставы) в виде болей и ограничения подвижности, без внешних изменений, длительностью от недели до трёх месяцев. При отсутствии лечения болезнь Лайма переходит в хроническую форму.
Поздний период лаймборрелиоза

Боррелиоз у беременных
Заражение женщины во время беременности (и до неё при отсутствии лечения) повышает риск гибели плода и выкидыша. Возможно внутриутробное поражение плода с развитием энцефалита и кардита, однако величина риска этого остаётся неясна.
Отличия боррелиоза у детей
Болезнь Лайма у детей чаще всего развивается в возрасте от 3 до 10 лет. При этом часто появляется мигрирующая эритема (покраснение кожи), расположенная в верхней половине тела. Интоксикация, как правило, сильнее, чем у взрослых. Могут увеличиваться лимфатические узлы возле места укуса клеща. Без лечения до 20 % случаев болезни Лайма переходит в хроническую форму.
Дифференциальный диагноз:
- в первую фазу — лихорадочные состояния с экзантемой, клещевой энцефалит, рожистое воспаление, эризипелоид, целлюлит;
- во вторую стадию — серозные менингиты другой этиологии, клещевой энцефалит, ревмокардит;
- в третью стадию — ревматизм и сходные заболевания, ревматоидный артрит, болезнь Рейтера. [3][6]
Отличия от клещевого энцефалита
При клещевом энцефалите присутствует выраженная лихорадка, общемозговая и неврологическая симптоматика, при боррелиозе — поражения кожи, суставов и сердца.
Патогенез болезни Лайма
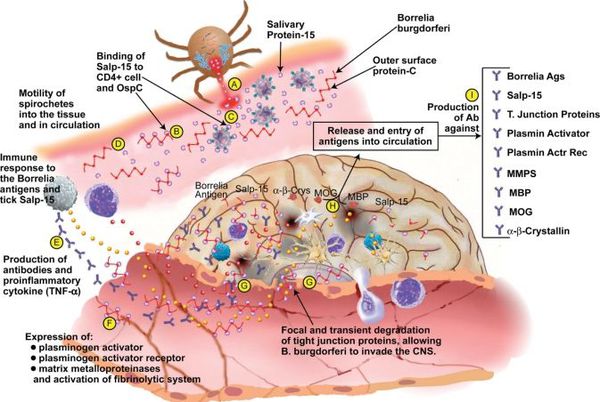
В случае прогрессирования боррелиоза (отсутствия лечения) происходит дальнейшее размножение боррелий, расширение спектра антител к антигенам спирохет и их длительная выработка (хронизация инфекции). Появляются циркулирующие иммунные комплексы, усиление продукции T-хелперов, лимфоплазматические инфильтраты (уплотнения ткани) в органах.
Ведущую роль в патогенезе артритов несут липополисахариды, стимулирующие синтез ИЛ-1 клетками моноцитарно-макрофагального ряда, Т- и В-лимфоцитов, простагландинов и коллагеназы синовиальной тканью (то есть происходит активация воспаления в полости суставов). Циркулирующие иммунные комплексы накапливаются в органах, привлекают нейтрофилы, которые вырабатывают медиаторы воспаления, вызывая воспалительные и дистрофические изменения в тканях. Возбудитель может сохраняться в организме десятилетия, поддерживая иммунопатологический процесс. [2] [3] [6]
Классификация и стадии развития болезни Лайма
1. По форме:
- манифестная;
- латентная (симптомы отсутствуют, только лабораторные изменения);
2. По течению:
- острое (до трёх месяцев)
- подострое (от трёх до шести месяцев);
- хроническое (более шести месяцев) — непрерывное и рецидивирующее.
3. По периодам:
- ранний (острая и диссеминированная стадии);
- поздний;
- резидуальные явления.
4. По клиническим признакам (при остром и подостром течении):
5. По преимущественному поражению какой-либо системы:
- нервной системы;
- опорно-двигательного аппарата;
- кожных покровов;
- сердечно-сосудистой системы;
- комбинированные.
6. По степени тяжести:
Осложнения болезни Лайма
Осложнения не характерны, но существуют резидуальные (остаточные) явления заболевания — стойкие, необратимые изменения органического характера (кожи, суставов, сердца, нервной системы при отсутствии явного воспалительного процесса и зачастую самого возбудителя). Они возникают не во время разгара болезни, а спустя длительное время (годы) и снижают работоспособность человека, вплоть до инвалидности. К ним относятся деформирующие артриты с органическими изменениями суставов, истончение кожи, нарушение мнестических функций, памяти, снижение работоспособности.
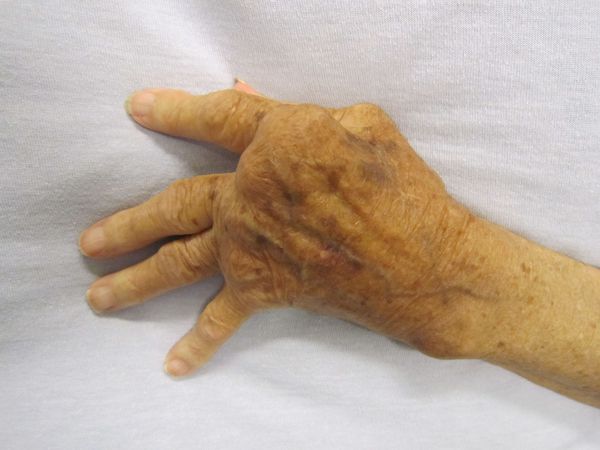
Диагностика болезни Лайма
К какому врачу обращаться при подозрении на боррелиоз
При укусе клеща и подозрении на клещевой боррелиоз необходимо обратиться к инфекционисту.
Какие исследования может назначить врач
- общеклинический анализ крови с лейкоцитарной формулой (нейтрофильный лейкоцитоз, повышение СОЭ);
- биохимический анализ крови (повышение островоспалительных белков, РФ, сиаловых кислот);
- серологические тесты (ИФА классов IgM и IgG, при сомнительных данных выполнение иммуноблоттинга. ПЦР крови, синовиальной жидкости, ликвора).
- МРТ ГМ (признаки атрофии коры головного мозга, дилатации желудочковой системы, воспалительные изменения, арахноидит).
В практической деятельности следует подходить к диагностике комплексно, учитывая совокупность данных, а не только результаты одного вида исследований. Например, в случаях, когда у пациентов при регулярных исследованиях неоднократно выявляются изолированные повышенные титры IgM (даже при подтверждении иммуноблоттингом) при отсутствии IgG, то это следует расценивать как ложноположительный результат. Причинами этого явления могут быть системные аутоиммунные заболевания, онкология, иные инфекционные заболевания, туберкулёз и другие, зачастую причины остаются невыясненными. [1] [4]
Через какое время после укуса клеща сдавать анализ на боррелиоз
Анализы следует сдавать сразу после укуса клеща и повторно три недели спустя.
Лечение болезни Лайма
Может проводиться как в инфекционном отделении больницы (при тяжёлом процессе), так и в амбулаторных условиях.
Показана диета № 15 по Певзнеру (общий стол). Режим отделения.
Медикаментозное лечение. Антибактериальная терапия
Наиболее важным и эффективным является применение этиотропной терапии (устраняющей причину) в как можно более ранние сроки от момента укуса клеща. Является достаточно дискутабельным вопрос о применении антибактериальной терапии в ранние сроки (до пяти дней от момента укуса) у необследованных лиц (или до момента получения результатов обследования клеща). Однако с практической точки зрения, учитывая возможность полиэтиологического характера возможного заражения человека (клещевой боррелиоз, моноцитарный эрлихиоз, гранулоцитарный анаплазмоз и другое) и серьёзные прогнозы при развитии системного клещевого боррелиоза, данное превентивное (профилактическое) лечение вполне обосновано. Применяются препараты широкого спектра действия, например, тетрациклинового, цефалоспоринового и пенициллинового рядов.
При развитии поздних стадий системного клещевого боррелиоза эффективность антибиотикотерапии существенно снижается (однако показания сохраняются), так как основное значение приобретают процессы аутоиммунных поражений при малоинтенсивном инфекционном процессе. Курсы лечения длительные (до одного месяца и более), в совокупности с препаратами улучшения доставки антибиотиков в ткани, десенсибилизирующей, противовоспалительной, антиоксидантной терапией.
В случае развития гипериммунного аутопроцесса (патологически усиленного иммунитета) назначаются средства, снижающие реактивность иммунной системы.
После перенесённого заболевания устанавливается диспансерное наблюдение за человеком до двух лет с периодическими осмотрами и серологическим обследованием. [1] [5]
Пробиотики
При лечение антибактериальными препаратами следует принимать пробиотические средства.
Дезинтоксикационная терапия
Выраженная интоксикация при болезни Лайма встречается редко, поэтому дезинтоксикационная терапия обычно не требуется.
Симптоматическое лечение
Для уменьшения симптомов боррелиоза могут применяться нестероидные противовоспалительные средства и противоаллергические препараты.
Общеукрепляющая терапия и физиотерапия
При лечении хронических форм боррелиоза можно применять средства общеукрепляющей терапии: витамины и иммуностимуляторы. Также могут назначаться физиотерапевтические процедуры: электрофорез, УФ-облучение, магнитотерапия, УВЧ, парафиновые аппликации, массаж, ЛФК. Эти методы популярны в России, однако исследований, подтверждающих их эффективность при восстановлении после болезни Лайма, недостаточно.
Прогноз. Профилактика
Неспецифическая профилактика — использование защитной плотной одежды при посещении лесопарковой зоны, отпугивающих клещей репеллентов, периодические осмотры кожных покровов (раз в два часа). Централизованная обработка лесных и парковых угодий акарицидными средствами. При обнаружении присосавшегося клеща незамедлительно обратиться в травматологическое отделение для удаления клеща и отправки его на обследование и параллельно обратиться к врачу-инфекционисту для наблюдения, обследования и получения рекомендаций по профилактической терапии.
Специфическая — профилактическое использование антибиотиков в ранние сроки после укуса клеща по назначению врача. [4] [5]
Создаётся ли иммунитет после перенесённого боррелиоза
Повторно заболеть можно через 5-7 лет, в некоторых случаях раньше.
Существует ли прививка от боррелиоза
Вакцины от болезни Лайма сейчас нет. Компании Valneva, Pfizer и MassBiologics разработали вакцины-кандидаты, которые проходят клинические испытания [7] .
Читайте также:

