Реферат диагностика токсоплазмоза у
Обновлено: 05.05.2024

Токсоплазмоз – протозойная инфекция, характеризующаяся поражением нервной, лимфоидной системы, печени, селезенки, скелетных мышц, миокарда, глаз.
Заболевание имеет достаточно широкую распространенность среди людей и животных.
В большинстве случаев наблюдается бессимптомное паразитоносительство или же заболевание протекает хронически без характерных симптомов.
По некоторым данным, среди населения встречается от 10 до 30% клинически здоровых носителей токсоплазм. В некоторых же случаях может наступить обострение хронического токсоплазмоза с воспалительными процессами и поражением нервной ткани, глаз, сердечной мышцы, сосудистой системы.
Опасно заражение токсоплазмозом женщин во время беременности. Из организма матери через плаценту токсоплазмы могут проникнуть в организм плода и вызвать его гибель. В других случаях могут рождаться мертвые или нежизнеспособные дети с различными уродствами. Иногда у детей наблюдается острый врожденный токсоплазмоз, характеризующийся высокой температурой, отеком, сыпью. Результатом врожденного токсоплазмоза может быть отставание в умственном развитии вплоть до идиотии.
I. Токсоплазма-возбудитель токсоплазмоза
Тип: Простейшие (Protozoa)
Класс: Споровики (Sporozoa)
Отряд: Кокцидий (Coccidia)
Представитель: Toxoplazma gondii
Токсоплазмы имеют сложный цикл развития, который происходит в организме окончательного и промежуточного хозяина.
По своей форме токсоплазмы напоминают дольку апельсина или полумесяц. Они изогнуты, один конец их заострен, другой более округлый, с размерами 4-7х2-5 мкм. В центре находится крупное рыхлое ядро.
На заостренном конце токсоплазмы при исследовании под электронным микроскопом обнаруживается коноид – образование, похожее на присоску. Коноид служит для фиксации паразита на поверхности клетки при проникновении в нее. Далее вращательным движением паразит внедряется в клетку хозяина. Для эндозоида характерно бесполое размножение путем деления. В результате многократных делений в цитоплазме клетки хозяина накапливается большое число токсоплазм, растягивающих наружную мембрану клетки. Формируется скопление токсоплазм под клеточной мембраной, называемое псевдоцистой. После разрушения пораженной клетки токсоплазмы внедряются в новую. При хроническом токсоплазмоме помимо псевдоцист формируются и настоящие цисты. Цисты в клетках хозяев могут сохранять жизнеспособность на протяжении нескольких лет.
Для поддержания вида токсоплазме необходимо осуществлять половое размножение. Оно происходит в организме окончательного хозяина – хищников семейства кошачьих. При этом в эпителии тонкой кишки из одних эндозоидов образуются макрогаметы, а из других – микрогаметы. После копуляции гамет возникает зигота, покрывающаяся плотной оболочкой. Такая форма называется ооцистой. Ооцисты выделяются во внешнюю среду с испражнениями кошки. Они очень стойки к неблагоприятным условиям и в почве могут сохраняться годами.
II. Пути заражения
Человек может заражаться токсоплазмозом от животных при снятии шкуры, разделке туши, алиментарным или воздушно-капельным путем.
Наиболее распространенный способ инфицирования – уход за больным животным и уборка его испражнений. Домашние животные способны переносить токсоплазмоз на шерсти. Заразиться токсоплазмозом так же можно при употреблении в пищу инфицированных продуктов, мяса. После попадания в кишечник цисты, происходит распространение паразита с током крови по всему организму.
Стоит отметить, что заразиться токсоплазмозом при контакте с человеком невозможно. Передача токсоплазмоза от человека к человеку осуществляется только трансплацентарно, при заражении плода от больной матери.
III.Профилактика токсоплазмоза
Для профилактики токсоплазмоза большое значение имеет оздоровление природных очагов, лечение домашних животных, ограничение контакта с кошками, соблюдение правил личной гигиены, термическая обработка пищевых продуктов, особенно мяса. Следует избегать загрязнения почвы испражнениями кошек в районе расположения детских игровых площадок, песочниц. Домашних кошек не рекомендуется кормить сырым мясом. Следует обследовать их на токсоплазмоз и, в случае обнаружения заболевания, лечить.
Для предупреждения врожденного токсоплазмоза необходимо всех беременных женщин, впервые обратившихся в женскую консультацию, обследовать с помощью внутрикожной пробы с токсоплазмином. Беременные с положительными иммунологическими реакциями, т.е. иммунные, в дальнейшем наблюдении и тем более в этиотропном лечении не нуждаются. Беременные с отрицательными иммунологическими реакциями (неиммунные) относятся к группе риска, так как могут заразиться токсоплазмозом в ходе настоящей беременности. Они подлежат повторному иммунологическому обследованию во втором и третьем триместрах беременности. Сохранение отрицательных иммунологических проб свидетельствует об отсутствии заражения.
Заключение
Токсоплазмоз – заболевание, вызываемое микроскопическим паразитом, называемым Toxoplasma gondii. Существует две группы риска по заражению токсоплазмозом: беременные женщины и лица с иммунодефицитами. По результатам статистического исследования (США), каждый год приблизительно 3000 детей рождаются инфицированными токсоплазмозом.
Токсоплазмоз является одним из самых распространенных паразитарных заболеваний у человека. В Южной Америке, в странах Африки болезнь поразила более 90 процентов жителей. В США и Западной Европе количество инфицированных варьируется в пределах от 25 до 50 процентов.
По статистике в России токсоплазмозом заражен каждый третий человек. Несмотря на тот факт, что болезнь поражает большое количество жителей, часто она никак не проявляет себя. Более того, многие люди даже не догадываются о том, что являются носителями токсоплазмоза: симптомы заболевания списываются на уже существующие болячки, и обращение к врачу происходит в редких случаях. При тяжелых формах инфекция поражает нервную систему, глаза, селезенку, мышцы сердца и даже печень.
Список источников информации:
Грачева, Л.И. Проблема токсоплазмоза / Л.И. Грачева // 1999
2. Биология: учебник в 2-х т. / под ред. В.Н. Ярыгин. – Москва: ГЭОТАР-Медиа, 2013.
3. Пехов А.П. Биология: медицинская биология, генетика и паразитология: учебник/ А.П. Пехов. – М.: ГЭОТАР-Медиа, 2010. – 656 с.

Введение: Токсоплазмоз - врожденное или приобретенное паразитарное заболевание с длительным, нередко хроническим течением, характеризующееся весьма частым поражением ЦНС, глаз, печени, селезенки и других органов и систем. Заболевание распространяется среди людей и теплокровных животных.
На территории нашей страны, по неполным данным, инфицировано около 30% населения. Однако среди инфицированных манифестные формы болезни встречаются редко - не более 1% всего населения (Казанцев А.П., 1985). Большинство случаев первичного поражения токсоплазмозом приходится на детский возраст. Возбудитель токсоплазмоза открыт в 1908 г. французскими исследователями Ш. Николем и Л. Мансе, обнаружившими его у грызунов. В 1923 г. чешский исследователь Янку обнаружил токсоплазмы в глазу умершего ребенка. Первый случай врожденного токсоплазмоза описан в 1939 году. токсоплазмоз паразитарный внутриутробный диагностика.
Токсоплазмы имеют сложный цикл развития, который происходит в организме окончательного и промежуточного хозяина. Окончательным хозяином является домашняя кошка и дикие представители семейства кошачьих (рысь, ягуар и др.), в организме которых (эпителиальные клетки кишечника) токсоплазмы проделывают бесполый (шизогонический) и половой (гаметогонический) циклы развития, завершающиеся образованием ооцист. Последние выделяются кошками с фекалиями в окружающую среду, где они могут сохраняться в течение 2 и более лет. Ооцисты часто обнаруживаются в почве, песке и других местах, посещаемых кошками.
Промежуточным хозяином токсоплазм являются многие виды теплокровных, птиц, а также человек. В организме промежуточного хозяина токсоплазмы размножаются только бесполым путем. Первоначально процесс характеризуется бурным внутриклеточным размножением токсоплазм (эндозоитов) в пораженных органах и тканях (печень, плацента, ЦНС и др.), сопровождающимся разрушением клеток и формированием воспалительной реакции. Этот процесс лежит в основе острой фазы токсоплазмозной инфекции у человека. В дальнейшем, под воздействием формирующегося иммунитета, большинство эндозоитов погибает, а оставшиеся постепенно трансформируются в цисты, которые имеют плотную оболочку и приспособлены к длительному паразитированию в организме хозяина. Цисты могут локализоваться во всех органах и тканях (мышцах, головном мозге, сердце, глазах, печени и др.). При этом воспалительная реакция отсутствует.
Заражение человека обычно происходит либо ооцистами (спорозоиты), попавшими в почву с фекалиями кошек, либо цистозоитами, содержащимися в тканях других промежуточных хозяев, что обычно происходит при употреблении в пишу недостаточно термически обработанного мяса инфицированных домашних и диких животных.
Устойчивость токсоплазм во внешней среде зависит от стадии жизненного цикла паразита. Вегетативные формы (эндозоиты) погибают вне организма через несколько часов. Они очень чувствительны к нагреванию, высушиванию, замораживанию и т.д. Цисты и, особенно, ооцисты высокоустойчивы во внешней среде. В мясе при температуре 4-6°С цисты сохраняются в течение месяца, в ткани мозга - более 2 мес. В почве ооцисты могут сохраняться более года. Цисты и ооцисты устойчивы также и к воздействию всех лекарственных препаратов.
Накопленные данные подтверждают концепцию о том, что токсоплазмы могут передаваться плоду в утробе матери, когда женщина инфицируется в период текущей беременности. И хотя в подобных случаях беременность чаще заканчивается рождением нормального незараженного ребенка, может иметь место спонтанный аборт, мертворожденность, преждевременные роды или рождение в срок зараженного ребенка. Врожденная инфекция развивается приблизительно у 30% детей, рожденных от матерей, инфицированных в период беременности. У детей, родившихся от матерей, инфицированных в I триместре, врожденный токсоплазмоз встречается наименее часто (около 17%), но болезнь протекает достаточно тяжело; у детей, родившихся от матерей, заразившихся в III триместре, врожденная инфекция отмечается чаще (около 65%), но протекает бессимптомно. Степень риска заражения плода не зависит от того, протекает ли инфекция у матери с клиническими симптомами или без таковых.
Передача инфекции при переливании крови или лейкоцитов или трасплантации органов:
Токсоплазмы могут передаваться при переливании крови или лейкоцитов. Возбудитель был выделен из лейкоцитов лиц без клинических признаков токсоплазмоза, причем описаны случаи стойкой паразитемии на протяжении 1 года после заражения у практически здоровых людей. Заслуживает особенного внимания высокая частота выделения паразитов из крови больных с хроническим миелоидным лейкозом и высокими титрами антител против токсоплазм. В цельной крови, стабилизированной цитратом натрия, и крови, хранящейся при +4°С, паразиты выживают до 50 дней. Больные с иммунодефицитом, требующие многократных переливаний крови, находятся в группе особого риска передачи инвазии этим способом. Передача токсоплазм может происходить при трансплантации сердца от доноров с острой инфекцией.
При приобретенном генерализованном токсоплазмозе изменения обнаруживаются во всех органах и тканях, но преимущественно в печени, головном мозге, лимфатических узлах и миокарде. При этом в головном мозге отмечаются воспалительные изменения очагового характера, вплоть до некрозов и кальцификатов, иногда встречаются изменения характерные для энцефалита и менингоэнцефалита. Возможны признаки гидроцефалии. В печени обнаруживается картина холестатического гепатита с мелкими очагами некроза и клеточной инфильтрацией, формирующей токсоплазмозные гранулемы, которые состоят из эпителиоидных клеток, макрофагов, плазматических клеток, лимфоцитов и эозинофилов. Аналогичного характера инфильтраты могут быть в легких, почках, лимфатических узлах и других органах. Поражение глаза характеризуется очаговыми некрозами, продуктивным воспалением сетчатки и сосудистой оболочки. Во внутренних органах обнаруживаются геморрагии, полнокровие и отек.
При врожденном токсоплазмозе основные морфологические изменения обнаруживаются в мозге. Возможно недоразвитие полушарий головного мозга с явлениями микроцефалии, поражение эпендимы, возникновение спаечного процесса с явлениями гидроцефалии. Характерна макрофагальная реакция с фагоцитированными токсоплазмами, встречаются дистрофические изменения. Возможно развитие тромбоваскулитов с появлением очагов асептического некроза с последующим их рассасыванием и образованием множественных полостей - кист. Может наблюдаться обызвествление очагов воспаления с образованием рассеянных кальцификатов.
В печени обнаруживается картина интерстициального гепатита с мелкими участками некрозов и перипортальной инфильтрацией, иногда выявляются очаги экстрамедулярного кроветворения. Селезенка обычно увеличена, с гиперплазией пульпы и обширной клеточной инфильтрацией. Характерна дилатация полостей сердца, отек легких, набухание лимфатических узлов. Типичны кровоизлияния и мелкие рассеянные очаги некроза во всех внутренних органах.
Диагноз ставится на основании комплексного обследования больного с обязательным осмотром глазного дна, ЭКГ, ЭЭГ, рентгенографии черепа, пораженных мышц, а также специальных методов исследования. Из клинических симптомов диагностическое значение имеют длительный субфебрилитет, лимфаденопатия, увеличение печени и селезенки, поражение глаз и обнаружение на обзорных рентгенограммах черепа кальцификатов в головном мозге.
Из лабораторных методов абсолютное диагностическое значение имеет обнаружение токсоплазм в окрашенных мазках крови, центрифугате ликвора, в мазках пунктата или биоптата лимфатических узлов, миндалин и гистологических срезах тканей органов трупов. Однако этот метод диагностики не получил распространения из-за трудности обнаружения малочисленных токсоплазм, к тому же расположенных внутриклеточно, кратковременности паразитемии и трудоемкости исследований.
В клинической практике наибольшее значение имеют методы иммунологической диагностики токсоплазмоза. Для обнаружения специфических антител используют РСК, РНИФ, РПГА, РЭМА, ИФА и др. Обнаружение в сыворотке крови про-тивотоксоплазменных антител с высокой достоверностью указывает на инфицированность ток-соплазмами, но не обязательно о заболевании токсоплазмозом, так как серологические реакции положительны у 20-30% населения. Поэтому для лабораторного подтверждения токсоплазмоза необходимо обнаружение нарастания титра антител в динамике заболевания или выявление в высоком титре специфических антител класса IgM (анти-ТОХО IgM) в иммуноферментном анализе.
Для диагностики токсоплазмоза предложена кожная аллергическая проба с токсоплазмином. Она становится положительной на 4-5 неделе после заражения и остается положительной нередко в течение всей жизни, что снижает ее диагностическое значение.
Результаты серологичских реакций при токсоплазмозе бывают достаточно информативными и позволяют не только своевременно диагностировать токсоплазмоз, но и судить о времени заражения и стадии патологического процесса.
При этом острый активно протекающий токсоплазмоз можно диагностировать на основании обнаружения в сыворотке крови анти-ТОХО IgM при отрицательной кожной пробе (положительны также РСК, РИФ, РИГА). Хронический токсоплазмоз - при выявлении анти-ТОХО IgG и стойко положительной кожной пробе.
При обнаружении анти-ТОХО IgG в низких титрах, отрицательных анти-ТОХО IgM и слабо положительной кожной пробе можно думать о реконвалесцентном процессе с последующим выздоровлением.
Вывод: Токсоплазмоз - это паразитарное заболевание, характеризующееся поражением нервной системы, глаз, скелетной мускулатуры и мышцы сердца, а также увеличением лимфоузлов, печени и селезенки. Склонно к хроническому течению.
Заражение человека происходит при контакте с кошачьими испражнениями, с землей и песком, загрязненными ими, а также при опробовании мясного фарша или употреблении недостаточно проваренного мяса. Баранина и свинина часто содержат токсоплазмы (10 - 25%). Контакт с собаками, сельскохозяйственными животными к заражению людей не приводит. Больной человек для окружающих не заразен.
Передача токсоплазм возможна при пересадке органов инфицированных доноров, и при внутриутробном заражении плода от матери через плаценту.
Диагноз подтверждается исследованиями крови - выявление специфических антител в крови. Наиболее чувствительным и специфическим методом диагностики токсоплазмоза является иммуноферментный анализ (ИФА), т.е. выявление антител классов IgM и IgG к токсоплазмам.
Обследованию на токсоплазмоз подлежат:
в обязательном порядке все беременные женщины в максимально ранние сроки беременности (в идеале - до нее);
женщины, страдающие бесплодием и невынашиванием беременности (выкидыши в сроке до 12 недель).
Источники:
Грачёва Л.И. и др. Эпидемиология, клиника, диагностика и лечение токсоплазмоза. Москва, 1996 г.
Руководство по инфекционным болезням под ред. проф. Ю.В. Лобзина СПб, 1996 г.

ТОКСОПЛАЗМОЗ. ПРИЧИНЫ, СИМПТОМЫ, ДИАГНОСТИКА И ЛЕЧЕНИЕ
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
Введение. Токсоплазмоз – врожденное или приобретенное паразитарное заболевание с длительным, нередко хроническим течением, характеризующееся весьма частым поражением ЦНС, глаз, печени, селезенки и других органов и систем. Заболевание широко распространено как среди людей, так и среди теплокровных животных, включая птиц. На территории нашей страны, по неполным данным, инфицировано около 30% населения. Однако среди инфицированных манифестные формы болезни встречаются редко – не более 1% всего населения. Большинство случаев первичного поражения токсоплазмозом приходится на детский возраст.
Заболевание, вызываемое облигатным внутриклеточным паразитом Toxoplasma gondii, характеризующееся преимущественно латентным течением. При наличии иммунного дисбаланса (иммунодефицита) может протекать с поражениями ЦНС, органов ретикулоэндотелиальной системы, поперечно-полосатой мускулатуры различной степени выраженности, вплоть до летальных исходов.
Биология и жизненный цикл. Токсоплазма относится к классу споровиков (на переднем конце таких паразитов расположен комплекс, обеспечивающий их проникновение внутрь клеток хозяина).
Имеют очень сложный жизненный цикл, в нем выделяется половой и бесполый процессы (с формированием и слиянием половых клеток – гамет), в организме окончательного хозяина из семейства кошачьих (домашние и дикие кошачьи).
Токсоплазма существует в виде 3 форм: тахизоит – быстро размножающая внутриклеточная форма, брадизоит – медленно размножающаяся внутриклеточная форма и ооциста. В результате полового размножения формируется спора – ооциста. В ооцисте путем деления формируется несколько спорозоитов, служащих для заражения других хозяев.
Человек заражается 3 путями:
при попадании в организм ооцист, с пищей или водой;
трансплацентарно происходит заражение плода, если мать заражается токсоплазмозом во время беременности;
при употреблении недостаточно термически обработанного или сырого мяса животных или птиц, зараженных токсоплазмозом и содержащих брадизоиды.
Способы инфицирования токсоплазмой. Алиментарный путь. Заражение наступает при употреблении в пищу инфицированных продуктов животного происхождения (например, мясо, молоко, яйца), не прошедших должным образом термическую обработку. Согласно результатам проведенных исследований, особенно много токсоплазм может находиться в мясе свиньи и барана. Вертикальный путь. Данный путь передачи еще называют трансплацентарным, так как передача токсоплазм происходит через плаценту от матери к плоду. Трансплацентарный путь передачи токсоплазмоза является наиболее опасным, так как во время беременности внедрение инфекции может спровоцировать у будущего ребенка серьезные патологические изменения (например, умственная отсталость, эпилепсия, внутричерепное давление, слепота). Инфицирование ребенка на ранней стадии беременности (первый триместр) нередко приводит к гибели плода. Фекально-оральный путь. Результаты проведенных исследований доказали, что инфицированные токсоплазмами кошки за две недели способны выделять в окружающую среду порядка двух миллиардов ооцист, которые считаются заразными в течение двух лет. Передача токсоплазм осуществляется при заглатывании пыли вместе с паразитами в тех местах, где испражнялась инфицированная кошка (например, песочница, огород, сад). Также инфекцию можно занести через рот с помощью загрязненных рук после контакта с больной кошкой, на шерсти которой обычно сохраняются частички ее испражнений.
Симптомы. Различают врождённый и приобретённый токсоплазмоз.
Врожденный токсоплазмоз. Особую опасность представляет вероятность внутриутробного заражения плода. Токсоплазма способна проникать через плаценту и вызывать болезнь у еще не родившегося ребенка. Но это возможно только в том случае, когда мать заражается токсоплазмозом во время беременности. В случае если она заразилась еще до беременности, будущему ребенку ничего не угрожает.
При врожденном токсоплазмозе поражение органов очень значительно. Так, возможны врожденные уродства глазного яблока, вплоть до развития слепоты, недоразвитие головного и спинного мозга. Тяжесть поражения плода тесно связана со сроками беременности - чем моложе плод, тем тяжелее болезнь.
В результате врождённого токсоплазмоза плод либо погибает в результате возникновения уродств, несовместимых с жизнью, либо рождается с симптомами острого врождённого токсоплазмоза - интоксикацией, лихорадкой, желтушностью, поражениями печени, селезёнки, лимфатических узлов и центральной нервной системы (энцефаломиелит).
Но токсоплазмоз может поражать плод только один раз, все последующие беременности будут надежно защищены образовавшимися у матери антителами.
Приобретённый токсоплазмоз нередко протекает в латентной (скрытой) форме; острая форма может напоминать тиф или энцефалит, нередки поражения глаз. Длится острая стадия примерно 7 дней. Острый токсоплазмоз начинается с высокой температуры, головной боли, судорог, рвоты. Увеличивается печень и селезенка, могут присоединиться воспаление легких и параличи.
Наиболее частой является хроническая форма заболевания, с длительным повышением температуры до 37,2-37,8 градусов, головными болями, увеличением печени, селезёнки, лимфатических узлов; мышечными и суставными болями. Возможно и носительство инфекции.
Хроническая форма и носительство нередко переходят в острую форму на фоне стресса, беременности, снижения иммунитета различной природы. На выраженность проявлений токсоплазмоза существенно влияет общее состояние здоровья, иммунный статус. У лиц с иммунодефицитом (включая СПИД) заболевание протекает крайне тяжело, часто со смертельным исходом.
Диагностика. Дифференциальная диагностика. Токсоплазмоз следует дифференцировать с инфекционным мононуклеозом, доброкачественным лимфоретикулезом, туберкулезом, бруцеллезом, листериозом, микоплазмозом, хламидиозом, цитомегалией, герпесом и рядом других бактериальных, вирусных и паразитарных инфекций. Следует исключить онкологические и системные заболевания (например: лимфогранулематоз, ревматизм и т.д.).
Лабораторная диагностика. Для лабораторной диагностики токсоплазмоза чаще всего применяют серологические методы: реакцию связывания комплемента (РСК), реакцию непрямой иммунофлюоресценции (РНИФ), иммуноферментный анализ (ИФА). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM.
Формирование диагноза. При формировании развернутого диагноза токсоплазмоза следует указывать:
форму токсоплазмоза (приобретенный, врожденный);
характер течения процесса (острый, подострый, хронический, инаппарантный);
органную или системную патологию;
Лечение. Выбор тактики лечения зависит от формы и характера течения заболевания, выраженности клинической симптоматики, тяжести течения, наличия осложнений и преобладающих органно-системных поражений.
Абсолютными показаниями к назначению лечения являются острый и подострый токсоплазмоз. Лечение хронического токсоплазмоза проводится в зависимости от выраженности клинической симптоматики, характера преобладающих поражений. Требует лечения и инаппарантный токсоплазмоз, выявленный у беременных женщин.
Возможно применение комбинированных препаратов; Потесептила (триметоприм + сульфадимезин), Бисептола (триметоприм + сульфаметоксазол), которые назначаются по 1 таблетке 2 раза в день в течение 10 дней (цикл), в количестве 2–3 циклов (курс). При непереносимости указанных препаратов при пероральном приеме возможно назначение внутривенно или капельно Бисептола: по 10 мл в день, в течение 5 дней (курс). В перерывах между циклами (курсами) этиотропной терапии назначается фолиевая кислота, в среднем до 0,01 г в сутки.
В случае выявления иммунодефицитного состояния совместно с этиотропной терапией назначаются иммунотропные средства: Ликопид, Циклоферон, Витамедин-М, а также натуральные гормоны тимуса телят и их синтетические аналоги: Тактивин, Тимамин, Тимоген, Декарис.
В комплексной терапии используют и препараты системной энзимотерапии (СЭТ), в частности Вобэнзим и Флогэнзим. Для сохранения микробиоценоза кишечника рекомендовано назначение про- и пребиотиков.
Лечение и дальнейшее диспансерное наблюдение за больными должно проводиться у специалистов в зависимости от характера преобладающей патологии— врачей-инфекционистов, врачей-невропатологов, врачей-окулистов, акушеров-гинекологов и др. Госпитализация осуществляется в стационар соответствующего профиля (инфекционный, неврологический, офтальмологический, акушерско-гинекологический, детский и т.д.). Это обусловлено особенностями органной патологии, спецификой обследования и назначением дополнительных средств лечения.
Профилактика. Профилактика токсоплазмоза включает: употребление в пищу только хорошо термически обработанных мясных продуктов; исключение привычки дегустации сырого мясного фарша или сырого мяса; употребление в пищу чисто вымытых овощей, зелени и фруктов (с земли); тщательное мытье рук после обработки сырого мяса, сырых мясных продуктов, после работы в саду, огороде, у детей – после игры на детской площадке, особенно в песочнице; борьбу с беспризорными кошками; лечение больных токсоплазмозом домашних кошек, предупреждение заражения последних. Специфическая профилактика токсоплазмоза не разработана.
Заключение: На сегодняшний день это заболевание не достаточно изучено, и требует большого внимания. Практически в каждом доме имеются кошки и собаки, первые же в свою очередь являются абсолютным источником заражения.
Источники:
Засухин Д.Н, Калякин В.Е, Акиншина Г.Т. Современные представления о цикле развития токсоплазм. Паразитология , 1971, №4, 5, с. 302 - 309; в кн.: Токсоплазмоз животных под ред. И.Г. Галузо. Алма-Ата, 1965 – C. 25- 30
Андреева Е.A. Врожденный токсоплазмоз / Е.А. Андреева // Эпидемиология и инфекционные болезни. – 2006. – № 1. – С. 49-52.
А. П. Казанцев /. Токсоплазмоз – Ленинград: Медицина: Ленингр. отд-ние, 1985. – 168 с.
Агринский Н.И. и А.Ф. Кухто. Токсоплазмоз - В кн.: Малоизученные заразные болезни животных. (Под. ред. Ф. М. Орлова. М, 1959.
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
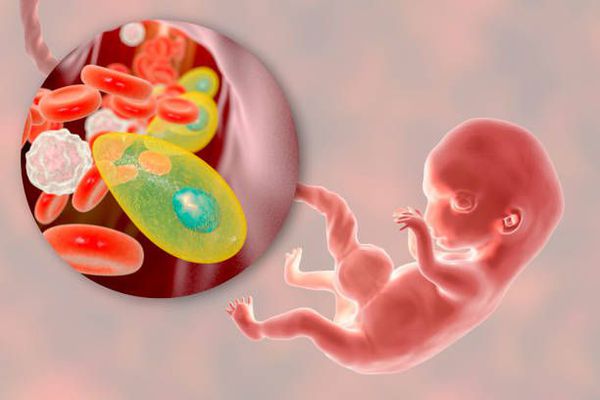
Этиология
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
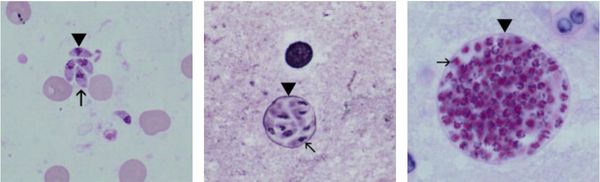
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
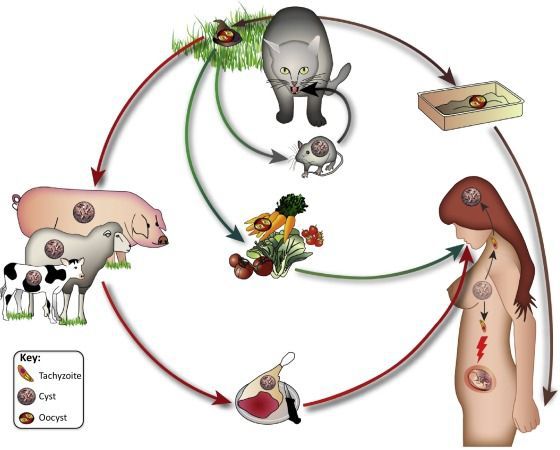
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
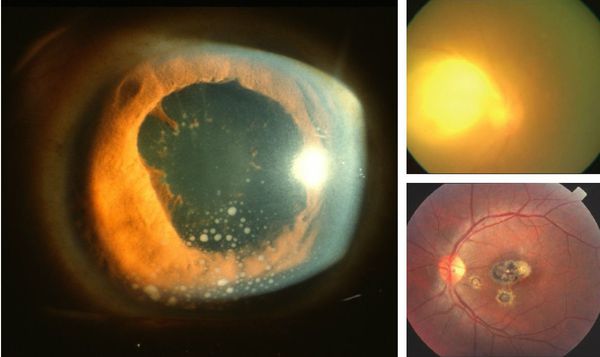
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
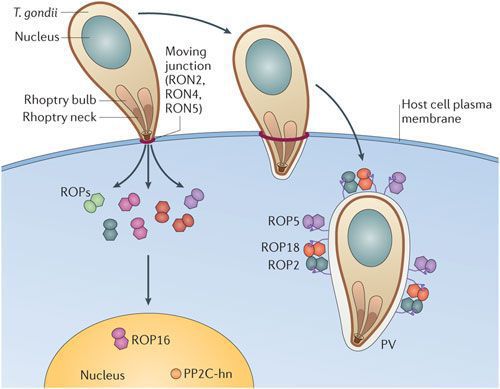
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
.jpg)
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
Этиология. Возбудитель токсоплазмоза Toxoplasma gondii относится к царству Protozoa, классу Coccidia, отряду Eucoccidiorida, типу Apicomplexa. T. gondii — условно патогенный внутриклеточный паразит, поражающий в организме промежуточных хозяев, в том числе человека, любые ядерные клетки гистеофагоцитарной системы.
Эпидемиология. Пораженность или инфицированность токсоплазмами населения Российской Федерации в среднем составляет около 20,0%. Показатели пораженности выше в регионах с теплым климатом; среди лиц ряда профессиональных групп: рабочие мясокомбинатов и звероводческих ферм, животноводы, ветеринарные работники и др. Инфицированность женщин, как правило, в 2–3 раза выше, чем у мужчин.
Заболеваемость токсоплазмозом во много раз ниже показателей инфицированности, однако трудности диагностики, несмотря на обязательную регистрацию, не позволяют судить об истинном уровне инфекции.
Восприимчивость к токсоплазмозу — практически поголовная. Распространение инфекции — повсеместное в виде носительства и спорадических заболеваний. Основной источник инфекции — дикие и домашние кошки.
Основной фактор передачи токсоплазм — сырое или недостаточно термически обработанное мясо, мясные продукты с находящимися в нем цистами токсоплазм. К дополнительным факторам передачи инфекции относятся плохо вымытая зелень, овощи, фрукты (с земли), грязные руки с находящимися на них ооцистами возбудителя.
Основные пути передачи:
- пищевой — связанный с употреблением в пищу термически плохо обработанного мяса, содержащего цисты паразита;
- контактный — ассоциированный с больными кошками, выделяющими токсоплазмы с фекалиями;
- трансплацентарный — при котором становится возможным проникновение токсоплазм в плод, с последующим развитием врожденного токсоплазмоза у новорожденного;
- парентеральный — при котором не исключается передача инфекции реципиенту при переливании крови, пересадке органов и тканей.
Беременная с токсоплазмозом не представляет эпидемиологической опасности ни для окружающих, ни для медицинского персонала, что делает возможным лечение этих пациентов как в амбулаторных условиях, так и в любом соматическом стационаре.
Патогенез. Вышедшие из цист или ооцист возбудители внедряются в эпителиальные клетки тонкого кишечника, где они размножаются, образую первичный аффект и проникая затем в региональные лимфатические узлы, а из них с током лимфы — в кровь. Диссеминация возбудителя приводит к поражению самых различных органов и тканей.
При беременности, в условиях сниженного иммунитета, наряду с первичным заражением токсоплазмами, опасным является и реактивация паразита (при инфицировании до беременности), что в значительной степени определяет течение и исход беременности.
При выходе токсоплазм из цист происходит диссеминация возбудителей. Их концентрация в тканях ассоциирована со способностью токсоплазм проникать трансплацентарно, что приводит к развитию внутриутробной патологии на любом сроке беременности.
Заражение плода наблюдается у беременных как с первичным инфицированием токсоплазмами, так и реактивацией возбудителя во время беременности у серопозитивных женщин. Поражение плода может возникать на любом сроке гестации, но особую опасность представляет его инфицирование в первом и втором триместрах. При заражении в третьем триместре беременности преобладают бессимптомные формы течения заболевания, а поздние клинические признаки проявляются через месяцы и годы.
Заражение на ранних сроках эмбриогенеза заканчивается спонтанным выкидышем, мертворождением, вызывает тяжелые нарушения развития — анэнцефалию, анофтальмию, гидроцефалию, гепатоспленомегалию и др. (табл.).
Формирование иммунитета приводит к исчезновению возбудителя из крови, прекращается его размножение в клетках. Образуются истинные тканевые цисты, которые могут длительно, десятилетиями, в интактном состоянии сохраняться в организме (носительство токсоплазм).
Клиника. Приобретенный токсоплазмоз по характеру течения делится на острый и хронический. Кроме того, в зависимости от длительности болезни и выраженности клинических симптомов возможно подострое, а также инаппарантное (субклиническое) течение инфекции, которое характеризуется определенной динамикой либо высоким уровнем специфических антител в крови, при отсутствии клинических проявлений болезни. Таким образом, наиболее удобной для практического здравоохранения, с нашей точки зрения, является следующая классификация приобретенного токсоплазмоза: острый, подострый, хронический, инаппарантный и носительство.
Клинические проявления токсоплазмоза у беременных не имеют каких-либо существенных отличий от уже известной клинической картины заболевания.
Лабораторная диагностика. Для лабораторной диагностики токсоплазмоза чаще всего применяют серологические методы: реакцию непрямой иммунофлюоресценции (РНИФ) и иммуноферментный анализ (ИФА). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM. Существенное значение в диагностике токсоплазмоза, особенно в дифференциации острого и хронического процессов, имеет определение классов иммуноглобулинов, в частности антител класса IgM. Надежно диагностировать токсоплазменную инфекцию можно лишь при сравнении результатов серологических реакций в динамике. Антитела всех классов существенно повышаются к концу второй — началу третьей недели от момента инфицирования и достигают диагностического уровня. Диагноз токсоплазмоза при наличии соответствующей клиники может быть поставлен при положительной серологической конверсии, когда второй анализ сыворотки становится положительным.
Диагностика токсоплазмоза у беременных женщин включает в себя весь комплекс необходимых клинических, параклинических и специальных (иммунобиологических) исследований, которые применяются для диагностики токсоплазмоза вообще.
Обязательным условием обследования беременной на токсоплазмоз должна быть консультация врача-инфекциониста для подтверждения либо исключения текущего инфекционного манифестного или бессимптомного (инаппарантного) токсоплазменного процесса.
Учитывая исключительную важность результатов иммунологического обследования в диагностике токсоплазмоза у беременных, необходимо правильно интерпретировать полученные данные.
Вариант 3: клинические проявления инфекции отсутствуют; серологические реакции положительные в низких, средних, иногда высоких титрах (РНИФ 1:640, ИФА IgG ≥ 200 Ед/мл; ИФА IgM — положительно). При исследовании парных сывороток (через 3–4 недели) регистрируется достоверное нарастание уровня специфических антител класса IgM.
Заключение: инаппарантный токсоплазмоз — реальная угроза инфицирования плода.
Вариант 4: имеются клинические проявления токсоплазмоза; серологические реакции положительные в низких и средних (иногда высоких) титрах: РНИФ 1:1280, ИФА IgG ≥ 200 Eд/мл; ИФА IgM — положительно, при исследовании парных сывороток в динамике регистрируется достоверное нарастание уровня специфических антител; выявляются специфические антитела класса IgM-класса. Заключение: острый токсоплазмоз.
Рекомендации: экстренная превентивная этиотропная терапия (не ранее чем со II триместра беременности); в I триместр — рассмотреть вопрос о прерывании беременности; проводят кордо- и амниоцентез на 22–23 неделях беременности; новорожденный обследуется на токсоплазмоз, и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 5: имеются клинические проявления инфекции; серологические реакции положительные в высоких или средних показателях; при исследовании парных сывороток в динамике регистрируется снижение уровня специфических антител (РНИФ ≤ 1:1280, ИФА IgG — 200 Eд/мл; ИФА IgM — положительно). Заключение: подострый токсоплазмоз. Рекомендации: этиотропная терапия (не ранее чем со II триместра); в I триместр — ставится вопрос о прерывании беременности; новорожденный обследуется на токсоплазмоз и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 6: имеются клинические проявления токсоплазмоза; серологические реакции положительны в низких или средних показателях (РНИФ 1:640, ИФА IgG — 200 Eд/мл; ИФА IgM — отрицательно); при исследовании парных сывороток (через 3–4 недели) динамики уровня антител нет; антитела класса IgM отсутствуют. Заключение: хронический приобретенный токсоплазмоз. Рекомендации: этиотропная терапия не проводится; при необходимости специфическая терапия вне беременности; прерывание беременности не показано.
Лечение. Показанием к назначению этиотропной терапии у беременных женщин являются острый, подострый и инаппарантный токсоплазмоз. Лечение хронического токсоплазмоза следует проводить строго по клиническим показаниям либо до, либо после беременности. При отсутствии жалоб и клинических показаний не нуждаются в лечении женщины, переболевшие токсоплазмозом до беременности. Эти женщины расцениваются как практически здоровые лица, не требующие специального медицинского наблюдения. Лечение беременных женщин следует проводить не ранее 12–16 недель беременности (со II триместра беременности).
Назначаются препараты группы пириметамина (Фансидар, Ровамицин).
Фансидар содержит сульфадоксин 500 мг и пириметамин 25 мг. Этиотропная терапия состоит из 2–3 циклов. Назначается 1 таблетка 1 раз в 3 дня № 8 таблеток на цикл. Учитывая возможность угнетения кроветворения под действием этиотропных препаратов, рекомендуется назначение фолиевой кислоты (в средних терапевтических дозах), а также проведение общих анализов крови и мочи. При непереносимости препаратов группы пириметаминов назначают Ровамицин, 1 таблетка которого содержит спиромицина 3 млн МЕ. Назначают по 3 млн МЕ 3 раза в день с семидневным перерывом. Хорошая переносимость Ровамицина больными, отсутствие лекарственного взаимодействия, высокая эффективность позволяют назначать его для лечения токсоплазмоза у беременных. При непереносимости пириметаминов возможна замена на антибиотики, например, эритромицин.
Противопоказаниями для назначения Фансидара и его аналогов, а также сульфаниламидных препаратов и антибиотиков являются: нарушения эритропоэза с анемией, заболевания почек с нарушением их функций, заболевания печени, декомпенсация сердечной деятельности.
В зависимости от сроков беременности целесообразно проведение не менее двух полных курсов этиотропной терапии с перерывами между ними 1–1,5 месяца.
Как показала практика, у пациенток с инаппарантным течением острого токсоплазмоза хороший эффект дает комплексное применение Фансидара с иммуномодуляторами (Галовит, Полиоксидоний). Уже после первого цикла лечения наблюдается значительное снижение IgM.
Профилактика врожденного токсоплазмоза. Профилактика врожденного токсоплазмоза должна строиться с учетом того факта, что только первичное заражение женщины во время беременности может привести к инфицированию плода. Оптимально профилактика врожденного токсоплазмоза должна включать в себя обследование женщин детородного возраста на токсоплазмоз до или, в крайнем случае, во время беременности. Неиммунные беременные женщины должны быть обязательно взяты на диспансерное наблюдение и обследоваться на токсоплазмоз 1 раз в триместр.
Литература
- О выявлении и профилактике токсоплазмоза в Москве. Методические рекомендации (№ 25). М., 2007.
- Лысенко А. Я. Клиническая паразитология. Женева, 2002.
- Hill D., Dubey J. P. Toxoplasma gondii: transmission, diagnosis and prevention // Clin. Microbiol. Infect. 2002. № 10.
- Desmonts G., Couvreur J. Toxoplasmosis in pregnancy and its transmission to the fetus // Bull. N. Y. Acad. Med. 1974. № 2.
Ф. К. Дзуцева*
Г. Ю. Никитина**
Ю. В. Борисенко*
Л. П. Иванова***, кандидат медицинских наук, доцент
С. Х. Зембатова***
*Городской центр по токсоплазмозу, **ГКБ им. С. П. Боткина, ***РМАПО, Москва
Читайте также:

