Синдром двс в клинике инфекционных болезней
Обновлено: 11.05.2024
ДВС-синдром относится к частым и наиболее тяжелым, жизненно опасным нарушениям системы гемостаза (гемостаз - комплекс реакций организма, направленных на предупреждение и остановку кровотечений).
Синонимы ДВС-синдрома - тромбогеморрагический синдром, коагулопатия потребления, гиперкоагуляционный синдром, синдром дефибринации.
ДВС-синдром (синдром диссеминированного внутрисосудистого свертывания) – это:
- вторичный патологический процесс, возникающий при постоянной и длительной стимуляции системы гемостаза;
- патологический процесс, имеющий фазовое течение, с первоначальной активацией и последующим глубоким нарастающим истощением всех звеньев системы гемостаза вплоть до полной утраты способности крови свертываться с развитием катастрофических неконтролируемых кровотечений и тяжелого генерализованного геморрагического синдрома;
- патологический процесс, при котором отмечается прогрессирующее рассеянное внутрисосудистое свертывание крови с множественным и повсеместным образованием микросгустков крови и агрегатов ее форменных элементов, что ухудшает ее реологические характеристики, блокирует микроциркуляцию в тканях и органах, вызывает в них ишемические повреждения и ведет к полиорганным поражениям.
В зависимости от интенсивности образования и поступления в кровь тромбопластина, который образуется при разрушении клеток, в том числе и кровяных, ДВС-синдром имеет различные клинические формы:
- молниеносную;
- острую;
- подострую;
- затяжную;
- хроническую;
- латентную;
- локальную;
- генерализованную;
- компенсированную;
- декомпенсированную.
Причины
Пусковыми факторами ДВС-синдрома могут явиться самые разнообразные интенсивные или длительные стимулы, так или иначе укладывающиеся в триаду Вирхова – нарушения циркуляции крови, ее свойств или сосудистой стенки.
1. При нарушении реологических характеристик крови и гемодинамики
- любой вид шока,
- кровопотеря,
- интоксикация,
- сепсис,
- резус-конфликтная беременность,
- остановка кровообращения и последующая реанимация, ,
- атония матки, ,
- массаж матки
2. При контакте крови с поврежденными клетками и тканями
-
,
- антенатальная гибель плода,
- онкологические заболевания
3. При изменении свойств крови и при массивном поступлении в кровь тромбопластических веществ
- лейкозы,
- эмболия околоплодными водами,
- переливание несовместимой крови,
- септический аборт,
- отслойка нормально расположенной плаценты с кровоизлиянием в матку,
- приращение плаценты, ,
- операции на паренхиматозных органах: матке, печени, легких, простате, почках;
- острая лучевая болезнь,
- синдром длительного сдавления,
- гангрена,
- трансплантация органов, химиотерапия, панкреонекроз, инфаркт миокарда и прочее).
Симптомы ДВС-синдрома
В течении ДВС-синдрома выделяют 4 стадии:
1 стадия – фаза гиперкоагуляции и гиперагреции тромбоцитов;
2 стадия – переходная фаза (разнонаправленные сдвиги в свертываемости крови как в сторону гипер-, так и в сторону гипокоагуляции);
3 стадия – фаза глубокой гипокоагуляции (кровь не сворачивается вообще);
4 стадия – разрешающая фаза (либо показатели гемостаза нормализуются, либо развиваются осложнения, приводящие к летальному исходу).
Симптоматика ДВС-синдрома зависит от многих факторов (причины, которая его вызвала, клиники шока, нарушений всех звеньев гемостаза, тромбозов, сниженного объема сосудистого русла, кровотечения, анемии, нарушения функций и дистрофии органов-мишеней, нарушения обмена веществ).
В первую фазу отмечается повышенная свертываемость крови, моментальное образование сгустков в крупных сосудах и тромбов в мелких (во время операции). У больного невозможно взять кровь на анализ, так как она тут же сворачивается. Как правило, первая фаза протекает очень быстро и остается незамеченной врачами. Отмечается резкое снижение артериального давления, кожные покровы бледные, покрыты холодным липким потом, пульс слабый (нитевидный). Затем развивается дыхательная недостаточность в силу поражения легких, влажный кашель и крепитация в легких, цианоз кожи, холодные ступни и кисти.
Во вторую фазу сохраняются те же симптомы, что и в первой стадии ДВС-синдрома, плюс в процесс вовлекаются почки (почечная недостаточность), надпочечники, пищеварительный тракт (тошнота, рвота, боли в животе, диарея). В головном мозге образуются микротромбы (головная боль, головокружение, судороги, потеря сознания вплоть до комы, парезы и параличи, инсульты).
Третья фаза (стадия гипокоагуляции) характеризуется массивными кровотечениями, как из первоначального очага, так и из других органов (кишечное и желудочное кровотечения вследствие изъязвления слизистой, кровь в моче – поражение почек, мокрота с примесью крови при откашливании).
Также характерно развитие геморрагического синдрома (появление массивных кровоизлияний, гематом, петехий, неостанавливающееся кровотечение в местах инъекций и во время проведения операции, кровоточивость десен, кровотечение из носа и прочее).
Четвертая фаза при своевременном и адекватном лечении ведет к восстановлению гемостаза и остановке кровотечения, но нередко заканчивается летальным исходом при массивном поражении внутренних органов и кровотечении.
Диагностика
Основные лабораторные исследования:
-
(при ДВС-синдроме отмечается снижение тромбоцитов во 2, 3 и 4 фазы);
- время свертываемости крови (норма 5 – 9 минут, в 1 стадию укорочение показателя, в последующие – удлинение времени);
- время кровотечения (норма 1 – 3 минуты); (активированное частичное тромбопластическое время – увеличение во 2 и 3 фазах ДВС-синдрома); , тромбиновое время, определение активированного времени рекальцификации плазмы – АВР (увеличение во вторую и третью стадию ДВС-синдрома);
- лизис сгустка (в норме нет, в 3 фазу лизис быстрый, а в 4 фазу сгусток не формируется); (норма 2 – 4 г/л, снижается во 2, 3 и 4 стадии);
- исследование феномена фрагментации эритроцитов вследствие повреждения их нитями фибрина (в норме тест отрицательный, положительный тест свидетельствует о ДВС-синдроме);
- снижение эритроцитов (анемия, уменьшение объема крови);
- снижение гематокрита (гиповолемия);
- определение кислотно-щелочного и электролитного баланса.
Лечение ДВС-синдрома
Терапию ДВС-синдрома осуществляет врач, столкнувшийся с данной патологией (то есть лечащий врач) вкупе с реаниматологом. При хроническом течении ДВС-синдрома его лечением занимается терапевт с гематологом.
В первую очередь необходимо устранить причину ДВС-синдрома. Например, при сепсисе назначается антибактериальная и трансуфизионная (внутривенное вливание препаратов крови) терапия, при травматическом шоке – адекватное обезболивание, иммобилизация, оксигенация и раннее хирургическое вмешательство. Или при опухолевых заболеваниях – химио- и радиотерапия, при инфаркте миокарда – купирование болевого синдрома, восстановление сердечного ритма и гемодинамики, при акушерской и гинекологической патологии радикальные меры (экстирпация матки, кесарево сечение).
Восстановление гемодинамики и реологических свойств крови осуществляется путем инфузионно-трансфузионных вливаний.
Показано вливание свежезамороженной плазмы, которая не только восстанавливает объем циркулирующей крови, но и содержит все факторы свертывания.
Также вводят кристаллоидные (физ. раствор, глюкоза) и коллоидные растворы (полиглюкин, реополиглюкин) в отношении 4/1 и белковые препараты крови (альбумин, протеин).
Назначается антикоагулянт прямого действия – гепарин. Доза гепарина зависит от стадии ДВС-синдрома (в 1 – 2 фазы она значительная). При значительной анемии переливается свежая (не более 3 суток) эритроцитарная масса.
В лечении тяжелого генерализованного ДВС-синдрома применяют фибриноген и концентраты свертывающих факторов крови (криопреципетат). Используют игинбиторы протеолиза – антипротеазы, для подавления тканевых протеаз, которые высвобождаются при повреждении клеток (контрикал, трасилол, гордокс). Также назначаются кортикостероиды (гидрокортизон, дексаметазон), так как они повышают свертываемость крови.
Параллельно ведется борьба с полиорганной недостаточностью (поддержка функций легких, почек, желудочно-кишечного тракта, надпочечников). Во 2 – 4 фазах ДВС-синдрома для восстановления местного гемостаза применяют смесь из аминокапроновой кислоты, сухого тромбина, этамзилата натрия и адроксона. Данную смесь вводят в брюшную полость через дренажи, перорально, в виде тампонов в полость матки и влагалища, а смоченные раствором салфетки наносят на рану.
Весь процесс интенсивной терапии занимает 1 – 5 суток (в зависимости от тяжести ДВС-синдрома), а последующее лечение продолжается до полного или практически полного восстановления всех полиорганных нарушений.
Осложнения и прогноз
К основным осложнениям ДВС-синдрома относятся:
- гемокоагуляционный шок (критическое падение артериального давления, расстройства дыхательной и сердечной систем и прочее);
- постгеморрагическая анемия;
- летальный исход.
Прогноз зависит от тяжести, течения и стадии ДВС-синдрома. В 1 и 2 стадии прогноз благоприятный, в 3 стадию сомнительный, в 4 (при неадекватном или отсутствующем лечении) летальный.
Важно! Все материалы носят справочный характер и ни в коей мере не являются альтернативой очной консультации специалиста.
Этот сайт использует cookie-файлы для идентификации посетителей сайта: Google analytics, Yandex metrika, Google Adsense. Если для вас это неприемлемо, пожалуйста, откройте эту страницу в анонимном режиме.
ДВС-синдром – расстройство гемостаза, связанное с гиперстимуляцией и дефицитом резервов свертывающей системы крови, приводящее к развитию тромботических, микроциркуляторных и геморрагических нарушений. При ДВС-синдроме наблюдается петехиально-гематомная сыпь, повышенная кровоточивость, дисфункция органов, а в острых случаях – развитие шока, гипотонии, сильных кровотечений, ОДН и ОПН. Диагноз устанавливают по характерным признакам и лабораторным тестам системы гемостаза. Лечение ДВС-синдрома направлено на коррекцию гемодинамики и нарушений свертывающей системы (антиагреганты, антикоагулянты, ангиопротекторы, гемотрансфузии, плазмаферез и др.).


Общие сведения
ДВС-синдром (диссеминированное внутрисосудистое свертывание, тромбогеморрагический синдром) – геморрагический диатез, характеризующийся чрезмерным ускорением внутрисосудистой коагуляции, образованием рыхлых сгустков крови в микроциркуляторной сети с развитием гипоксических и дистрофически-некротических измерений в органах. ДВС-синдром представляет опасность для жизни пациента из-за риска возникновения обширных, плохо купируемых кровотечений и острой дисфункции органов (главным образом, легких, почек, надпочечников, печени, селезенки), имеющих обширную микроциркуляторную сеть.
ДВС-синдром можно рассматривать, как неадекватную защитную реакцию, направленную на ликвидацию кровотечения при повреждении кровеносных сосудов и изоляцию организма от пораженных тканей. Встречаемость ДВС-синдрома в различных отраслях практической медицины (гематологии, реаниматологии, хирургии, акушерстве и гинекологии, травматологии и др.) достаточно велика.
Причины ДВС-синдрома
ДВС-синдром развивается на фоне заболеваний, протекающих с повреждением тканей, эндотелия сосудов и клеток крови, сопровождаемых микрогемодинамическими нарушениями и сдвигом гемостаза в сторону гиперкоагуляции. Основной причиной ДВС-синдрома выступают септические осложнения бактериальных и вирусных инфекций, шок любой природы. ДВС-синдром часто сопутствует акушерской патологии - тяжелому гестозу, предлежанию и преждевременной отслойке плаценты, внутриутробной гибели плода, эмболии амниотической жидкостью, ручному отделению последа, атоническим маточным кровотечениям, а также операции кесарево сечение.
Развитие тромбогеморрагического синдрома могут инициировать метастазирующие злокачественные опухоли (рак легкого, рак желудка), обширные травмы, ожоги, серьезные хирургические вмешательства. Нередко ДВС-синдром сопровождает трансфузию крови и ее компонентов, трансплантацию тканей и органов, протезирование сосудов и клапанов сердца, применение искусственного кровообращения.
Способствовать возникновению ДВС-синдрома могут сердечно-сосудистые заболевания, протекающие с гиперфибриногенемией, увеличением вязкости и снижением текучести крови, механическим препятствием кровотоку атеросклеротической бляшкой. К ДВС-синдрому могут приводить прием медикаментов (ОК, ристомицина, диуретиков), острые отравления (например, ядом змеи) и острые аллергические реакции.
Патогенез ДВС-синдрома
Несостоятельность гемостаза при ДВС-синдроме возникает за счет гиперстимуляции свертывающей и быстрого истощения антикоагулянтной и фибринолитической систем гемостаза.
Развитие ДВС-синдрома обуславливается различными факторами, которые появляются в кровяном русле и напрямую активируют процесс свертывания, либо осуществляют это через медиаторы, воздействующие на эндотелий. В качестве активаторов ДВС-синдрома могут выступать токсины, ферменты бактерий, околоплодные воды, иммунные комплексы, стрессовые катехоламины, фосфолипиды, снижение сердечного выброса и кровотока, ацидоз, гиповолемия и др.
Развитие ДВС-синдрома происходит с последовательной сменой 4-х стадий.
I - начальная стадия гиперкоагуляции и внутрисосудистой агрегации клеток. Обусловлена выбросом в кровь тканевого тромбопластина или веществ, обладающих тромбопластиноподобным действием и запускающих внутренний и внешний пути свертывания. Может продолжаться от нескольких минут и часов (при острой форме) до нескольких дней и месяцев (при хронической).
II - стадия прогрессирующей коагулопатии потребления. Характеризуется дефицитом фибриногена, кровяных пластинок и плазменных факторов вследствие их избыточного расхода на тромбообразование и недостаточного возмещения.
III - критическая стадия вторичного фибринолиза и выраженной гипокоагуляции. Отмечается разбалансировка гемостатического процесса (афибриногенемия, накопление патологических продуктов, разрушение эритроцитов) с замедлением свертывания крови (вплоть до полной неспособности к свертыванию).
IV - стадия восстановления. Наблюдаются либо остаточные очаговые дистрофические и некротические изменения в тканях тех или иных органов и выздоровление, либо осложнения в виде острой органной недостаточности.

Классификация ДВС-синдрома
По выраженности и скорости развития ДВС-синдром может быть острым (в т.ч., молниеносным), подострым, хроническим и рецидивирующим. Острая форма тромбогеморрагического синдрома возникает при массивном выбросе в кровь тромбопластина и ему подобных факторов (при акушерской патологии, обширных операциях, травмах, ожогах, синдроме длительного сдавления тканей). Характеризуется ускоренной сменой стадий ДВС-синдрома, отсутствием нормального защитного антикоагуляционного механизма. Подострая и хроническая формы ДВС-синдрома связаны с обширным изменением поверхности эндотелия сосудов (например, вследствие атеросклеротических отложений), выступающим в роли активирующей субстанции.
ДВС-синдром может проявляться локально (ограниченно, в одном органе) и генерализованно (с поражением нескольких органов или всего организма). По компенсаторному потенциалу организма можно выделить компенсированный, субкомпенсированный и декомпенсированный ДВС-синдром. Компенсированная форма протекает бессимптомно, микросгустки лизируются за счет усиления фибринолиза, факторы свертывания восполняются из резервов и путем биосинтеза. Субкомпенсированная форма проявляется в виде гемосиндрома средней степени тяжести; декомпенсированная - характеризуется каскадными реакциями реактивного фибринолиза, несостоятельностью коагуляционных процессов, несворачиваемостью крови.
ДВС-синдром может протекать с одинаковой активностью прокоагулянтного и сосудисто-тромбоцитарного звеньев гемостаза (смешанный патогенез) или с преобладанием активности одного из них.
Симптомы ДВС-синдрома
Клинические проявления ДВС-синдрома определяются темпом развития и распространенностью поражения, стадией процесса, состоянием компенсаторных механизмов, наслоением симптомов заболевания-индуктора. В основе ДВС-синдрома лежит комплекс тромбогеморрагических реакций и дисфункции органов.
При острой манифестной форме быстро (за несколько часов) развивается генерализованный ДВС-синдром, для которого характерно шоковое состояние с гипотонией, потерей сознания, признаками отека легких и острой дыхательной недостаточности. Гемосиндром выражается нарастающей кровоточивостью, массивными и профузными кровотечениями (легочными, маточными, носовыми, желудочно-кишечными). Характерно развитие очагов ишемической дистрофии миокарда, панкреонекроза, эрозивно-язвенного гастроэнтерита. Молниеносная форма ДВС-синдрома свойственна эмболии околоплодными водами, когда коагулопатия стремительно (в течение нескольких минут) переходит в критическую стадию, сопровождаясь кардиопульмонарным и геморрагическим шоком. Летальность матери и ребенка при этой форме ДВС-синдрома приближается к 80%.
ДВС-синдром сопровождается астеническим синдромом, плохим заживлением ран, присоединением гнойной инфекции, развитием келоидных рубцов. К осложнениям ДВС-синдрома относятся гемокоагуляционный шок, острая дыхательная недостаточность, ОПН, некроз печени, язвенная болезнь желудка, инфаркт кишечника, панкреонекроз, ишемический инсульт, острая постгеморрагическая анемия.

Диагностика ДВС-синдрома
Для установления ДВС-синдрома необходимы тщательный сбор анамнеза с поиском этиологического фактора, анализ клинической картины и данных лабораторных исследований (общего анализа крови и мочи, мазка крови, коагулограммы, паракоагуляционных проб, ИФА). Важно оценить характер кровоточивости, уточнить стадию коагулопатии, отражающую глубину нарушений.
Для ДВС-синдрома характерна петехиально-гематомная кровоточивость, геморрагии сразу из нескольких мест. При малосимптомном течении гиперкоагуляция выявляется только лабораторными методами. К обязательным скрининговым тестам относятся определение количества тромбоцитов, фибриногена, АПТВ, протромбинового и тромбинового времени, времени свертывания по Ли-Уайту. Исследование маркеров внутрисосудистого свертывания - РФМК и ПДФ, D-димера методом ИФА и паракоагуляционных проб помогает подтвердить ДВС-синдром.
Лечение ДВС-синдрома
Успех лечения ДВС-синдрома возможен при его ранней диагностике. Активные лечебные мероприятия требуются при выраженной симптоматике в виде кровотечений и органной недостаточности. Больных с ДВС-синдромом следует госпитализировать в ОРИТ и при необходимости проводить ИВЛ, активную противошоковую терапию. При малосимптомном ДВС-синдроме основным представляется лечение фоновой патологии, коррекция параметров гемодинамики и функциональных нарушений органов.
Острый ДВС-синдром требует срочного устранения его первопричины, например, экстренного родоразрешения, гистерэктомии - при акушерской патологии или антибиотикотерапии – при септических осложнениях. Для ликвидации гиперкоагуляции показано введение антикоагулянтов (гепарина), дезагрегантов (дипиридамола, пентоксифиллина), фибринолитиков. Больные должны находиться под постоянным динамическим контролем показателей гемостаза.
В качестве заместительной терапии при ДВС-синдроме применяются трансинфузии свежезамороженной плазмы, тромбоцитарной или эритроцитарной массы (при падении уровня тромбоцитов или Hb); криопреципитата (при сердечной недостаточности), физраствора. При кровотечениях, угрожающих жизни, возможно назначение антифибринолитических средств (аминокапроновой к-ты, ингибиторов протеаз). При кожных геморрагиях и ранах накладываются повязки с этамзилатом, гемостатическая губка.
По показаниям применяют кортикостероиды, оксигенотерапию, плазмаферез. Для восстановления микроциркуляции и нарушенных функций органов назначают ангиопротекторы, ноотропные препараты, посиндромную терапию. В случае ОПН проводят гемодиализ, гемодиафильтрацию. При хроническом ДВС-синдроме целесообразно использование дезагрегантов, вазодилататоров, в послеоперационном периоде - гепаринотерапии.
Прогноз и профилактика ДВС-синдрома
Прогноз ДВС-синдрома - вариативный, зависит от основного, этиологически значимого заболевания, тяжести нарушений гемостаза и своевременности начатого лечения. При остром ДВС-синдроме не исключен летальный исход в результате некупируемой большой кровопотери, развития шока, ОПН, острой дыхательной недостаточности, внутренних кровоизлияний. Предупреждение ДВС-синдрома заключается в выявлении пациентов группы риска (особенно, среди беременных и лиц пожилого возраста), лечении фонового заболевания.
МКБ-10
Общие сведения
Резкое снижение оксигенации и вентиляции организма вызывает кислородную недостаточность сердца и головного мозга и развитие угрожающих для жизни состояний. При РДСВ летальность в случае несвоевременно или неадекватно оказанной помощи достигает 60-70%.

Причины РДСВ
Механизмом, запускающим развитие респираторного дистресс-синдрома, служит эмболизация мелких сосудов легких микросгустками крови, частичками поврежденных тканей, каплями жира на фоне образующихся в тканях токсичных биологически активных веществ — кининов, простагландинов и др. Микроэмболизация легочных сосудов развивается в результате прямого или опосредованного воздействия на капиллярно-альвеолярную мембрану легочных ацинусов различного рода повреждающих факторов.
Прямое повреждающее воздействие оказывает аспирация крови, рвотных масс и воды, вдыхание дыма и токсических веществ, контузия легких, перелом ребер, разрыв диафрагмы, передозировка наркотических средств. Опосредованное, непрямое повреждение капиллярно-альвеолярных мембран вызывает активация и агрегация форменных элементов крови при бактериальных и вирусных пневмониях, сепсисе, ожогах, сочетанных травмах и травматическом шоке, сопровождающихся массивной кровопотерей, панкреатите, аутоиммунных процессах, электротравме, эклампсии и т. д.
Патогенез
Повышение проницаемости мембраны для белка и жидкости вызывает отек интерстициальной и альвеолярной тканей, снижение растяжимости и газообменной функции легких. Эти процессы приводят к развитию гипоксемии, гиперкапнии и острой дыхательной недостаточности. Респираторный дистресс-синдром может развиваться на протяжении нескольких часов или суток от момента воздействия повреждающего фактора. В течении РДСВ выделяют три патоморфологические фазы РДСВ:
- Острая фаза (до 2-5 суток) – интерстициальный и альвеолярный отек легких, поражение капилляров легких и эпителия альвеол, развитие микроателектазов. В случае благоприятного течения респираторного дистресс-синдрома спустя несколько дней острота явлений стихает, транссудат рассасывается; в противном случае возможен переход в подострое либо хроническое течение.
- Подострая фаза – развитие бронхоальвеолярного и интерстициального воспаления.
- Хроническая фаза – соответствует развитию фиброзирующего альвеолита. Происходит утолщение и уплощение капиллярно-альвеолярных мембран, разрастание в них соединительной ткани, формирование микротромбозов и запустевание сосудистого русла. Исходом хронической фазы респираторного дистресс-синдрома служит развитие легочной гипертензии и хронической дыхательной недостаточности. Выраженный альвеолярный фиброз может возникнуть уже спустя 2-3 недели.
Симптомы РДСВ
Развитие респираторного дистресс-синдрома взрослых характеризуется последовательной сменой стадий, отражающих патологические изменения в легких и типичную картину остро нарастающей дыхательной недостаточности.
- I (стадия повреждения) – первые 6 часов со времени воздействия стрессового фактора. Жалобы, как правило, отсутствуют, клинико-рентгенологические изменения не определяются.
- II (стадия мнимого благополучия) – от 6 до 12 часов со времени воздействия стрессового фактора. Развиваются нарастающая одышка, цианоз, тахикардия, тахипноэ (учащение дыхания более 20 в мин.), беспокойство пациента, кашель с пенистой мокротой и прожилками крови. Одышка и цианоз не купируются кислородными ингаляциями, содержание кислорода в крови неуклонно падает. Аускультативно в легких – хрипы, крепитация; рентгенологические признаки соответствуют диффузному интерстициальному отеку.
- III (стадия дыхательной недостаточности) – спустя 12-24 часа после воздействия стрессового фактора. Клокочущее дыхание с выделением пенистой розовой мокроты, нарастающая гипоксемия и гиперкапния, поверхностное дыхание, увеличение центрального венозного и снижение артериального давления. По всей поверхности легких выслушиваются влажные, множественные хрипы различного калибра. На рентгенограммах определяется слияние очаговых теней. В этой стадии происходит образование гиалиновых мембран, заполнение альвеол фибрином, экссудатом, распадающимися кровяными тельцами, поражение эндотелия капилляров с образованием кровоизлияний и микроателектазов.
- IV (терминальная стадия) - метаболический ацидоз, гипоксемия и гиперкапния не устраняются предельно большими объемами интенсивной терапии и ИВЛ. Ложноположительная рентгенологическая динамика (появление очагов просветлений) вызвана разрастанием соединительной ткани, замещающей паренхиму легких. В этом терминальном периоде респираторного дистресс-синдрома развивается полиорганная недостаточность, характеризующаяся:
- артериальной гипотонией, выраженной тахикардией, фибрилляцией предсердий, желудочковой тахикардией;
- гипербилирубинемией, гиперферментемией, гипоальбуминемией, гипохолестеринемией;
- ДВС-синдромом, лейкопенией, тромбоцитопенией ;
- повышением мочевины и креатинина, олигурией;
- желудочно-кишечными и легочными кровотечениями;
- угнетением сознания, комой.
Осложнения
В ходе купирования респираторного дистресс-синдрома возможны осложнения в виде баротравм легких, бактериальных пневмоний, развития ДВС-синдрома, левожелудочковой сердечной недостаточности. Проявлениями баротравмы, развивающейся вследствие проведения аппаратной вентиляции легких, служат подкожная эмфизема, пневмоторакс, пневмомедиастинум. Повышенный риск развития баротравм у пациентов с респираторным дистресс-синдромом обусловлен перерастяжением альвеол при снижении эластичности легочной ткани.
Острая левожелудочковая недостаточность (или кардиогенный отек легких) при РДСВ обусловлена застоем кровообращения в малом круге. ДВС-синдром (синдром диссеминированного внутрисосудистого свертывания) развивается при сепсисе, панкреонекрозе и других повреждающих факторах и выражается в полиорганном поражении различных систем.
Диагностика
Характерным показателем газового состава крови при РДСВ является РаО2 ниже 50 мм рт. ст. (гипоксемия), несмотря на проводимую оксигенотерапию (при FiО2 более >60%.), нарастание гиперкапнии. У пациентов с РДСВ выраженная дыхательная недостаточность и гипоксемия сохраняются даже при ингаляциях высококонцентрированной кислородной смеси.
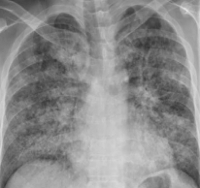
Биохимические показатели венозной крови характеризуются гипоальбуминемией, повышением свертывающих факторов, нарастанием трансаминаз и билирубина. При рентгенографии легких на периферии выявляются диффузные множественные тени (симптом "снежной бури"), снижение прозрачности легочной ткани, плевральный выпот обычно отсутствует.
Лечение респираторного дистресс-синдрома
Лечение респираторного дистресс-синдрома осуществляется в условиях отделения интенсивной терапии и реанимации. Мероприятия по купированию РДСВ включают:
- устранение стрессового повреждающего фактора;
- коррекцию гипоксемии и острой дыхательной недостаточности;
- лечение полиорганных нарушений.
На первом этапе лечения респираторного дистресс-синдрома устраняются прямые повреждающие факторы легких, назначается массивная антибактериальная терапия при бактериальных пневмониях, сепсисе, осуществляется соответствующее лечение ожогов и травм. Для устранения гипоксии проводится подбор адекватного режима кислородотерапии с динамическим контролем газов крови (с поддержанием РО2 не менее 60 мм рт.ст.). Подача кислорода может осуществляться чрез маску или носовой катетер, при неэффективной оксигенации показана ИВЛ (при ЧД 30 в минуту).
Для профилактики развития ДВС-синдрома назначаются ацетилсалициловая кислота, дипиридамол и реополиглюкин, гепарин. Несмотря на интерстициальный и альвеолярный отек, проводится инфузионная терапия для улучшения питания органов, нормализации диуреза и поддержания уровня АД. Эффективность лечения респираторного дистресс-синдрома зависит от его своевременности: оно успешно лишь на ранних стадиях данного состояния до наступления необратимых поражений легочной ткани.
Прогноз и профилактика
Летальность в III стадии респираторного дистресс-синдрома составляет около 80%, в терминальной стадии, соответствующей полиорганной недостаточности, обычно все пациенты погибают. При благоприятном исходе после купирования РДСВ функция легких может практически полностью восстановиться, однако чаще требуется длительная поддерживающая терапия.
Специфические профилактические мероприятия респираторного дистресс-синдрома отсутствуют. Следует остерегаться воздействия стрессовых повреждающих факторов, ведущих к развитию РДСВ.
2. Острый респираторный дистресс-синдром в педиатрической практике/ Александрович Ю.С., Пшениснов К.В.// Вестник интенсивной терапии. – 2014 - No3.
4. Классификация острого респираторного дистресс-синдрома/ Мороз В.В., Голубев А. М. .// Общая реаниматология. – 2012 - №4(4).
В классическую схему представления о синдроме ДВС жизнь вносит свои коррективы, основанные на клинических наблюдениях и переосмысливании привычных и догматизированных постулатов.
ДВС – приобретенная коагулопатия, расстройство системной коагуляции, характеризующееся распространенным микротромбообразованием, на фоне активациии прокоагулянтов и/или фибринолиза и потреблением антикоагулянтов, исходом которого является полиорганная недостаточность или кровотечение.
ДВС – это приобретенный неспецифический синдром, встречающийся при различной клинической патологии.
Не следует путать ДВС с коагулопатией разведения, которая может развиться при острой массивной кровопотере и проведении инфузионно-трансфузионной терапии без восполнения факторов свертывающей системы или с применением коллоидов, угнетающих коагуляцию и эффективность тромбоцитов. Также не является следствием ДВС и геморрагический синдром, связанный с охлаждением тела – при гипотермии система коагуляционного гемостаза просто выключается и кровь не сворачивается, тромбы не образуются. Не связаны с ДВС и состояния, при которых нарушен синтез факторов коагуляционного гемостаза - болезни печени, острая или хроническая печеночная недостаточность (вирусный гепатит), нарушения функции кишечника.
Этиология
Основным фактором, провоцирующим развитие ДВС является системная воспалительная реакция организма, наиболее частой причиной которой являются:
1. Инфекции: бактериальный или грибковый сепсис; тяжелые формы вирусной инфекции (ВИЧ, цитомегаловирусная пневмония, герпес), малярия.
2. Онкологические заболевания: гемобластозы (острый миелолейкоз), аденокарцинома поджелудочной и предстательной желез.
3. Акушерские осложнения: эклампсия, отслойка плаценты, эмболия амниотической жидкостью.
4. Травмы: политравма, ожоги.
5. Трансфузионные: аппаратный гемолиз, массивные переливания донорской крови, Реинфузия частично лизированной или инфицированной крови.
Патофизиология
Следующее заблуждение, связанное с представлением о ДВС – это, то, что следствием ДВС обязательно является кровотечение, от которого и умирают больные. Следует заметить, что исход ДВС в смертельное кровотечение бывает очень редко – не более нескольких процентов. В сотни раз чаще больные умирают от другого исхода ДВС – генерализованные микротромбозы, порождающие полиорганную дисфункцию, и смерть при этом медленная и мучительная. Этот факт могут подтвердить патологанатомы, которые фиксируют при аутопсии эти самые микротромбозы с давностью образования несколько суток – вокруг тромбированных капилляров уже развился некроз.
Итак, чтобы представит истинное лицо ДВС, рассмотрим существующую классификацию стадий (фаз) (Федорова З.Д. и др. (1979), Барышев Б.А. (1981)):
1. Компенсированная форма – гиперкоагуляция (ДВС I).
2. Субкомпенсированная форма – коагулопатия потребления без активации фибринолиза (ДВСII)
3. и с активацией вторичного фибринолиза (ДВС III).
4. Декомпенсированная форма – полное несвертывание крови (ДВС IV).
Если есть проблемы с синтезом факторов свертывающей системы, то уже можно наблюдать ДВС II, характеризующийся снижением уровня факторов по данным коагулограммы. Клиники тоже нет. Тоже ничего страшного, за исключением того, что если где-то возникнет механическое повреждение целостности сосудов, то система гемостаза не сможет достаточно активно этому противостоять, т.е. эрозивные поражения ЖКТ, механические или трофические повреждения слизистых буду кровить сильнее и дольше.
Небольшое различие в печальной динамике бывает при ожоговом, а иногда и при гиповолемическм шоке – здесь определенную роль играет еще один фактор, определяющий ток крови по капиллярам – вязкость. Именно при этих состояниях значимо повышается вязкость крови, развивается гемоконцентрация, так же способствующая блоку микроциркуляции.
Лабораторная диагностика
1. Определение D-димера – единственный тест, дающий достаточно основания для постановки диагноза ДВС-синдрома в фазе гиперкоагуляции.
D-димер представляет собой один из продуктов деградации фибриногена (ПДФ) и его появление в кровотоке свидетельствует о двух последовательных событиях - генерализованном образовании фибрина и активном фибринолизе.
При дилюционной коагулопатии D-димер не образуется.
2. Определение ПДФ дает в основном информацию об активности первичного фибринолиза, который происходит вне связи с генерализованным тромбообразованием.
Диагностическая ценность этого теста невелика. Тем не менее, повышенный уровень ПДФ выявляется у 89-100% больных.
4. ПТИ или МНО определяет содержание в плазме К-витаминзависимых факторов свертывающей системы, т.е. потенциал защиты от кровотечений.
5. Содержание тромбоцитов, при гиперкоагуляции, как правило, повышено, при кровотечении снижется. Уровень тромбоцитов менее 30х10 9 /л считают критическим.
6. Время свертывания – скрининговый тест, определяющий эффективность свертывающей системы. Несмотря на простоту, достаточно информативный и ценный.
7. Тест спонтанного лизиса сгустка (СЛС) – скрининговый тест, позволяющий оперативно определить активность фибринолиза при ДВСIII.
Лечение
Отсутствие убедительных данных об эффективности какого-либо лечебного алгоритма при ДВС превращают терапию его в своего рода искусство балансирования на грани возможного и недопустимого.
Основная задача лечения ДВС – устранение его причины и предотвращение ситуаций, которые могут спровоцировать его печальную финализацию.
В соответствии с изложенными выше двумя вариантами этого вида коагулопатии, не связанными между собой последовательностью развития, следует разделить рекомендации по лечению также на два варианта.
Гиперкоагуляция и блок микроциркуляции.
Следует отдавать себе отчет, что состоявшийся морфологически блок микроциркуляции лечению уже не подлежит. Нельзя допускать функциональный блок микроциркуляции (централизацию) на длительное время, так как даже у исходно здорового человека это может привести к необратимым изменениям достаточно быстро. У исходно больного человека с уже имеющейся гиперкоагуляцией, функциональный блок микроциркуляции еще быстрее перейдет на морфологический уровень и необратимый микротромбоз.
Таким образом, основной вид профилактического лечения заключается в поддержании нормальной вязкости крови и скорости кровотока, а также в предотвращении функционального блока микроциркуляции – централизации, т.е. предотвращении повышения сосудистого тонуса – постнагрузки. Нельзя также допускать и выраженное снижение постнагрузки, когда значительно снижается скорость капиллярного кровотока. Особенно это опасно при исходной гиперкоагуляции и повышенной вязкости крови.
Нормализация гемодинамики осуществляется диагностикой варианта кровообращения и соответствующей коррекцией сосудистого тонуса (вазодилятаторы или вазопрессоры), а также поддержанием достаточной скорости кровотока кардиотониками (дофамин, сердечные гликозиды).
Гепаринотерапия не показала эффективность в подобных ситуациях, однако предотвращает до половины случаев образования крупных тромбов и может быть рекомендована при исходной гиперкоагуляции, в некоторых клинических ситуациях вместе с антиагрегантами или реокорректорами. Необходим контроль за уровнем физиологических антикоагулянтов, в частности за антитромбином.
Гипокоагуляция, фибринолитическая коагулопатия.
Критическая коагулопатия неразрешима до тех пор, пока действуют ее пусковые механизмы.
Для лечения фибринолитической коагулопатии при акушерских кровотечениях необходимо снизить фибринолитическую активность и восстановить коагуляционные способности крови. Это проводят под контролем коагулограммы. Торможение фибринолитической активности достигают введением ингибиторов животного происхождения - контрикала, трасилола, гордокса. Ингибиторы фибринолиза применяют строго под контролем коагулограммы. Также применяют препараты транексамовой кислоты (Трамин) или аминокапроновой кислоты.
Восстановление коагуляционных свойств крови проводят только после торможения фибринолиза и достигают замещающей терапией - переливанием свежезамороженной плазмы. СЗП начинают вводить через 15 минут после введения болюса антифибринолитика. При несоблюдении этой последовательности больной вместе с факторами свертывающей системы получает и дополнительную дозу физиологичеких фибринолитиков, которые также содержатся в СЗП.
Введение антикоагулянтов (гепаринов), антиагрегантов и реокорректоров (растворы декстрана, ГЭК) категорически противопоказано. Необходимо следить за уровнем кальция, т.к. введение вместе с компонентами крови большого количества цитрата может иметь эффект прямого антикоагулянта.
Наряду с постоянным лабораторным контролем за гемостазом (в т.ч. и за уровнем тромбоцитов), необходимо следить и за температурой тела, чтобы исключить коагулопатию разведения или гипотермическую гипокоагуляцию.
Список использованной литературы
1. Клинический протокол диагностики и лечения пациентов с диссеминированным внутрисосудистым свертыванием крови предназначен для применения в стационарных условиях районных, областных и республиканских организаций здравоохранения, оказывающих экстренную медицинскую помощь в связи с состояниями, представляющими угрозу для жизни пациента независимо от особенностей этиологического фактора.
2. Возрастная категория: взрослое и детское население Республики Беларусь.
3. Наименование нозологической формы заболевания (шифр по МКБ-10)
Диссеминированное внутрисосудистое свертывание (синдром дефибринации) - D65;
4. Диссеминированное внутрисосудистое свертывание крови (далее- ДВС крови)- это неспецифический общепатологический процесс, связанный с поступлением в кровоток и воздействием на систему гемостаза эндогенных и экзогенных активаторов свертывания крови и агрегации тромбоцитов, что приводит:
к генерализованной активации факторов свертывания и тромбоцитов;
истощению физиологических антикоагулянтных и антиагрегантных механизмов, а затем и запасов факторов свертывания и тромбоцитов в результате их потребления;
к системной активации фибринолиза;
к образованию в кровотоке фибриновых и/или тромбоцитарных эмболов и тромбов, блокирующих микроциркуляторное русло и обтурирующих крупные сосуды;
к развитию связанных с блокадой кровотока тканевых и органных нарушений (полиорганной недостаточности) и возникновению на этом
фоне генерализованной кровоточивости и, регистрируемой лабораторно вторичной несвертываемости крови.
Совокупность изменений гемостаза, регистрируемых лабораторно, клинических проявлений полиорганной недостаточности вследствие генерализованного включения механизмов первичного и вторичного гемостаза в патогенез основного заболевания и клинических проявлений геморрагического синдрома представляют синдром диссеминированного внутрисосудистого свертывания крови (ДВС-синдром).
5. Универсальность нарушений гемостаза при ДВС крови как стереотипной реакции системы свертывания крови на мощные активирующие воздействия, возникающие при различных патологических процессах, делает объективно обоснованным существование универсального алгоритма его диагностики и патогенетической терапии (коррекции гемостаза).
Диагностика
7. Анализ клинической ситуации (оценка вероятности развития ДВС крови) является первым и главным основанием для начала его патогенетической профилактики (терапии) и выполнения гемостазиологического исследования.
Лабораторная диагностика
ЛАБОРАТОРНАЯ ДИАГНОСТИКА ДВС
9. Варианты течения ДВС:
молниеносный - от 1-2 часов (например, эмболия околоплодными водами) до 1 суток (например, септический шок в случае менингококкцемии);
острый - от 1 суток до нескольких дней или 1 недели (например, массивная кровопотеря вследствие тяжелой комбинированной травмы);
подострый - от 1 недели до 1 месяца (сепсис, преэклампсия, гестоз беременных);
хронический - от 1 месяца до 1 года (злокачественное новообразование при отсутствии радикального лечения, синие пороки сердца без хирургической коррекции, обширная гемангиома мягких тканей).
10. Диагностика ДВС.
10.1. Ситуационная диагностика (анализ клинической ситуации с точки зрения вероятности развития ДВС крови).
10.2. Выявление гемостазиологических маркеров ДВС.
Минимальный набор тестов, достаточный для диагностики и необходимый для принятия терапевтического решения:
подсчет тромбоцитов периферической крови, начиная с момента возникновения клинической ситуации, свойственной для острого или молниеносного ДВС - каждые 12 часов; определение АПТВ;
протромбиновое время Квика (далее - ПВ Квика); определение уровня фибриногена крови, коагулируемого тромбином;
тест на присутствие или количественное содержание РКМФ; определение уровня Д-димеров.
10.3. Оценка тяжести состояния пациента и выявление клинических признаков полиорганной недостаточности, ассоциированной с развитием две.
10.4. Приоритет имеют клиническая оценка ситуации и лабораторная гемостазиологическая диагностика ДВС, поскольку они обеспечивают максимально раннее и объективное его обнаружение и, соответственно, максимально эффективное лечение. Оценка состояния гемостаза (определение стадии и остроты процесса) и учет клинических проявлений ДВС необходимы для обоснованного выбора тактики этиотропной и патогенетической терапии, включая коррекцию гемостаза.
Лечение
11. Лечение пациентов с ДВС крови состоит из следующих основных блоков:
этиотропная терапия - устранение действия причинного фактора, ассоциированного с развитием ДВС крови;
посиндромная интенсивная терапия — поддержание основных гомеостатических констант и замещение утраченных функций органов и систем организма в соответствии с правилами проведения посиндромного лечения пациентов, нуждающихся в проведении интенсивной терапии и реанимации. Независимо от ситуации необходимо помнить о том, что пациент должен быть согрет, достигнут необходимый уровень ионизированного кальция в крови и pH капиллярной крови не менее 7,2; коррекция нарушений гемостаза с учетом стадии ДВС.
лекарственное средство вводят в случае снижения активности факторов протромбинового комплекса менее 50%.
Эптаког альфа активированный в дозе 90 мкг/кг в/в струйно в течение 2-5 минут каждые 2 часа вводят до остановки продолжающегося кровотечения, угрожающего жизни. Показания для введения rVIIa у детей в случае ДВС: возникшее во время полостной операции кровотечение, проявляющееся диффузной кровоточивостью со всей раневой поверхности, кровоизлияние в центральную нервную систему на фоне тромбоцитопении, а так же легочное кровотечение у пациента в состоянии тромбоцитопении во время искусственной вентиляции легких. Низкий уровень фактора V (менее 20% возрастной нормы) и гипофибриногенемия (менее 1 г/л не позволяют реализовать гемостатический эффект фактора rVIIa. Дефицит фактора V восполняют введением криоплазмы.
Ингибитор фибринолиза - апротинин вводят в суточной дозе 14000 АТрЕ/кг массы тела внутривенно методом титрования с постоянной скоростью. Перед началом суточного титрования вводят 25% суточной дозы в виде болюсной инъекции в течение 30-60 минут. Показание для введения лекарственного средства - продолжающееся кровотечение, вызванное доказанным вторичным фибринолизом или первичным фибриногенолизом. Лекарственное средство вводят до остановки кровотечения; широкий спектр антипротеазной активности лекарственное средствоов апротинина обуславливает необходимость применения при фибриногенолизе их максимальных доз. В зависимости от производителя лекарственное средствоы могут иметь различные единицы измерения активности: 1 антитрипсиновая единица (АТрЕ) лекарственного средства равна 1,33 калликреин инактивирующей единице (КИЕ).
Антикоагулянты.
Гепарин в гипокоагуляционных дозах у детей с гипокоагуляционной стадией ДВС противопоказан в связи с высокой вероятностью усиления кровоточивости. Допустимо в целях повышения антикоагулянтного потенциала донорской криоплазмы перед ее ведением реципиенту добавлять в криоплазму нефракционированный гепарин в соотношении 1 ЕД нефракционированного гепарина на 1 мл вводимой реципиенту криоплазмы.
В случае тромбоза магистрального сосуда у ребенка в гипокоагуляционной стадии ДВС показано введение натриевой соли НМГ, предназначенного для внутривенного введения путем титрования в течение суток. В случае тромбоцитопении (менее 100-10 9 /л) рассчитываемая на единицу массы тела (килограмм) терапевтическая суточная доза НМГ в анти-Ха МЕ/кг, количественно равна содержанию тромбоцитов в единице объема крови. Например, если число тромбоцитов периферической крови равно 75-10 9 /л, то суточная доза НМГ составит 75 анти-Ха МЕ/кг. Профилактику венозных тромбозов вследствие вынужденной гиподинамии проводят пациентам, имеющим центральный венозный катетер и находящимся на искусственной вентиляции легких более 3 недель. Профилактическая доза составляет 50% от терапевтической. В случае необходимости проведения экстракорпоральной детоксикации организма (гемодиализ, плазмафильтрация) при острой почечной недостаточности внутривенно болюсно вводят 5-10 анти-Ха МЕ/кг, с последующим введением 4-5 МЕ/кг в час.
Низкомолеклярный гепарин, обладающий свойством антикоагулянта и тормозящий адгезию и агрегацию тромбоцитов, у детей в гипокоагуляционной стадии ДВС запрещен.
Антидот для всех гепаринов - протамина сульфат: 1 мг протамина сульфата нейтрализует 100 анти-Ха ME НМГ или 100 ЕД нефракционированного гепарина.
Ангиопротекторы - этамзилат вводят для снижения проницаемости сосудистой стенки в дозе 10-15 мг/кг внутривенно 4 раза в сутки.
Трансфузии эритроцитарных компонентов для поддержания уровня гемоглобина крови не менее 90-100 г/л.
Читайте также:

