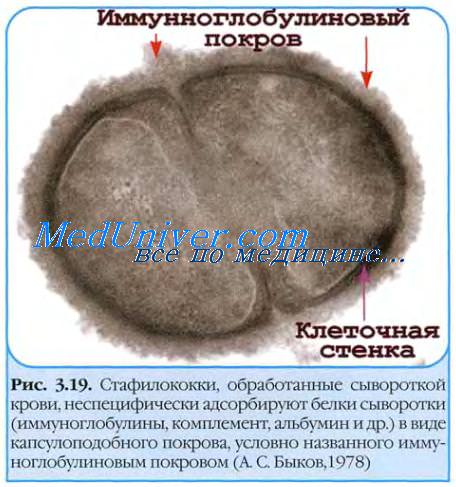
Токсин синдрома токсического шока
Обновлено: 25.04.2024
Критерии инфекционно-токсического шока. Степени ИТШ
В нашем понимании, существуют следующие клинико-патогенетические критерии ИТШ:
• генерализация инфекции и выраженность интоксикационного синдрома;
• нарушения КОС и водно-электролитного обмена;
• гипоксия;
• гемодинамические расстройства;
• расстройства микроциркуляции и капилляротрофи-ческая недостаточность;
• ДВС-синдром;
• развитие "шоковых органов" и полиорганной недостаточности.
"Шоковые органы" могут обнаруживаться не только у больных с ИТШ и, следовательно, не являются эквивалентом шока. По мнению В.А.Гологорского и соавт. (1988), дисфункция органов при шоке определяется их резервами и исходной способностью противостоять метаболическим расстройствам. По данным Г.А Рябова (1994), метаболические расстройства у больных с ИТШ сводятся к: 1) гипергликемии; 2) повышению уровня свободных жирных кислот; 3) катаболизму белков с повышением синтеза мочевины; 4) повышению внутриклеточной осмолярности.
В последние годы клинико-патогенетические различия в процессах, обусловленных грамположительной и грамотрицательной флорой, вызывающих ИТШ, рядом исследователей во внимание не принимаются и рассматриваются как архаизм.
Шоковые состояния с патофизиологических позиции целесообразно разделить на 2 категории ; 1) со сниженным сердечным выбросом и нарушенной общей периферической тканевой перфузией; 2) с нормальным или повышенным сердечным выбросом и нарушенным распределением периферического кровотока.
По мнению Г.А.Рябова (1994), для шока характерна фазовость патологического процесса. По данным В.Л.Айзенберга (1993, 1995), при ИТШ у детей, страдающих острыми кишечными инфекциями, целесообразно различать две стадии: компенсированную и декомпенсированную. Первая стадия характеризуется патологической гипердинамией с увеличением сердечного индекса в значительных пределах, тахикардией и натриемией при нормальной концентрации калия, вторая — гиподинамическим вариантом нарушения кровообращения со снижением сердечного индекса, гипонатриемией и гипокалиемией.
Для ИТШ у больных с острыми кишечными инфекциями характерно развитие ДВС-синдрома. При этом четко определяется фазовость коагулопатии. В одних случаях в клинической картине доминируют проявления тромбоза, в других — развитие геморрагического синдрома. При этом тромбоз чаще регистрируется в области мезентериальных, реже в области коронарных и мозговых сосудов. Кровоизлияния выявляются чаще на коже, слизистой оболочке кишки, в паренхиме легких, веществе и оболочках головного мозга.
Помимо непосредственного действия бактериальной флоры на сердечно-сосудистую систему и клеточный метаболизм, патогенез ИТШ определяется действием эндотоксина и липополисахаридных компонентов оболочек грамотрицательных бактерий. Последние активируют систему комплемента и освобождают биологически активные амины.
Таким образом, вначале развивается гипердинамическая фаза шока, и в связи с постепенным перемещением внутрисосудистой жидкости в интерстициальное и внутриклеточное пространства возникает гиподинамическая Фаза шока. С этого момента ИТШ более сходен с гиповолемическим.
Патогенез шока представлен ниже в виде схемы. Практически важным является разграничение шока У больных с острыми кишечными инфекциями по степени тяжести.
Шок I степени (компенсированный): тяжелое состояние больного, двигательное беспокойство, периодическое возбуждение, состояние тревоги, повышенная температура тела, бледность кожных покровов, цианоз губ и ногтевых фаланг. Характерны умеренная одышка, тахикардия и нормальное АД. Диурез умеренно снижен. Рвота и жидкий стул несколько раз в сутки. В крови — метаболический ацидоз, чаще компенсированный, гипокалиемия.
Шок II степени (субкомпенсированный): тяжелое состояние больного, заторможенность. Температура тела повышенная или нормальная. Бледность кожного покрова, цианоз. Тахикардия и глухость тонов сердца.
Пульс слабого наполнения, АД 85/60—60/20 мм рт.ст. рвота и жидкий стул под себя несколько раз в сутки. Олигурия. Декомпенсированный метаболический ацидоз, гипоксемия, гипокалиемия.
Шок III степени (декомпенсированный): крайне тяжелое состояние, сознание сохранено, возможны бред и галлюцинации, при отеке головного мозга — судороги и потеря сознания. Гипотермия и тотальный ацидоз. Тоны сердца глухие, пульс нитевидный или не определяется. дД 50/0 мм рт.ст. Анурия. Стул жидкий под себя несколько раз в сутки, но может отсутствовать. Рвота чаще всего сохраняется. В крови — декомпенсированный метаболический ацидоз, гипоксемия.
Мы наблюдали 36 762 больных с острыми кишечными инфекциями, в том числе 31 555 больных (85,8 %) с пищевыми токсикоинфекциями; 3455 (9,4 %) — сальмонеллезами, 1752 больных (4,8 %) —острой дизентерией, среди них мужчин 6,9%, женщин —93,1 %. Больных в возрасте до 20 лет — 10,9 %, 21 года — 40 лет — 26,5 %, 41 года — 60 лет — 26,9 %, 61 года — 70 лет — 25,6 %, старше 71 года— 10,1 %. Тяжелое течение отмечалось у 2,9% больных, средней тяжести — у 90,6 %, легкое — у 6,5 % больных. ИТШ развился у 57 больных (0,15 %): с выраженным обезвоживанием — у 24, а без выраженного обезвоживания с токсикозом — у 33 больных.
При пищевых токсикоинфекциях ИТШ наблюдался у 32 больных (0,1 %), в том числе с выраженным обезвоживанием — у 15, без выраженного обезвоживания — у 17 больных. При сальмонеллезе ИТШ развился у 21 больного (0,6 %), в том числе с выраженным обезвоживанием — у 9, без выраженного — у 12. При острой дизентерии ИТШ наблюдался у 4 больных (0,2 %) и всегда протекал без выраженного обезвоживания. Таким образом, ИТШ чаще всего возникал у больных сальмонеллезом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
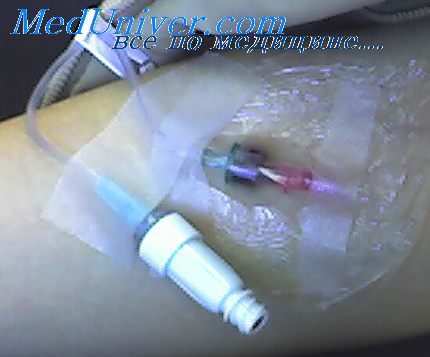
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
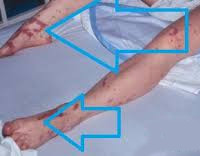
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Синдром токсического шока — тяжелое острое полиорганное поражение, вызванное экзотоксинами золотистого стафилококка или пиогенного стрептококка. Проявляется внезапным повышением температуры до 38,9°С и более, падением артериального давления, эритематозными кожными высыпаниями с последующим шелушением, профузным поносом, рвотой, признаками поражения разных органов и систем. Диагноз СТШ устанавливают на основе клинической картины, данных физикального обследования, лабораторных, в том числе бактериологических, анализов. Лечение предусматривает санацию бактериального очага, назначение антибиотиков, инфузионной и симптоматической терапии.
МКБ-10
Общие сведения
Синдром токсического шока (СТШ) впервые диагностирован в 1978 г. у семи детей со стафилококковой инфекцией. Специалисты в области гинекологии столкнулись с ним двумя годами позже, отметив связь развития синдрома у молодых женщин с использованием суперадсорбирующих гигиенических тампонов во время месячных. Абсолютное большинство пациенток — женщины в возрасте 17-30 лет. Приблизительно у половины из них развитие синдрома связано с менструацией. В четверти случаев неменструального СТШ заболевание возникает в послеродовом периоде у носительниц Staphylococcus aureus, в 75% — в результате других причин (кожного и подкожного инфицирования, перенесенных операций с тампонированием и пр.).

Причины СТШ
Синдром токсического шока вызывают экзотоксин-продуцирующие микроорганизмы, оказывающие системное воздействие на разные органы и ткани, — золотистый стафилококк (Staphylococcus aureus) и пиогенный β-гемолитический стрептококк группы А (Streptococcus pyogenes). В большинстве случаев заболевание возникает не в момент первичного заражения бактериями, а на фоне носительства инфекционных возбудителей при воздействии следующих предрасполагающих факторов:
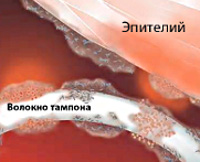
- Использование тампонов. Вероятность развития СТШ возрастает при пользовании гигиеническими средствами с повышенными адсорбирующими свойствами и нарушении рекомендуемой частоты их замены.
- Использование интравагинальных контрацептивов. Наличие во влагалище диафрагм, губок, колпачков создает благоприятные условия для размножения микроорганизмов.
- Нарушение целостности слизистых оболочек. При травмах половых органов, наличии в матке остатков плацентарной ткани, плодных оболочек, крови после родов и гинекологических операций возникают оптимальные условия для бактериального обсеменения и проникновения микроорганизмов или их токсинов в кровь.
Неменструальный синдром токсического шока может осложнять хирургические процедуры, при которых применяется перевязочный материал, накапливающий кровь (операции на полости носа с использованием турунд, тампонирование ран и др.), и травматические повреждения кожи. Сочетание указанных факторов с вирусными заболеваниями (ветрянкой, гриппом), приемом иммуносупрессивных препаратов повышает риск развития токсемии и бактериемии.
Патогенез
Ключевую роль в развитии синдрома токсического шока играют механические и химические воздействия, которые способствуют размножению бактерий и влияют на проницаемость тканей. Пусковым моментом служит проникновение в кровь значительных количеств специфических токсинов (TSST) и их взаимодействие с Т-лимфоцитами. В результате массивно высвобождаются цитокины, вызывающие полиорганную токсическую реакцию. Расширяются сосуды и повышается проницаемость их стенки, что приводит к перемещению плазмы крови и сывороточных протеинов во внесосудистое пространство. При этом наблюдается резкое падение давления, возникают отеки, нарушается коагуляция, повышается температура. Под влиянием опосредованных иммунных реакций и прямого действия токсинов поражаются кожа, паренхима печени, легких и других органов.
Симптомы СТШ
У менструирующих женщин, использующих тампоны, признаки СТШ появляются на 3—5-й день менструации. При синдроме токсического шока, осложнившем роды или гинекологические операции, патология проявляется в первые 2 дня послеродового или послеоперационного периода. Как правило, заболевание возникает остро. В редких случаях наблюдается продром в виде общего недомогания, тошноты, головной и мышечных болей. Первым признаком СТШ становится сильный озноб с повышением температуры до 39—40°С, после чего в течение 1—4 суток разворачивается полная клиническая картина.
Практически у всех пациенток возникают мышечная слабость и диффузные боли в мышцах, особенно в мускулатуре проксимальных отделов конечностей, брюшного пресса и спины. Часто беспокоят боли в суставах. Более чем 90% заболевших отмечают упорную рвоту и профузный водянистый понос, скудное количество мочи. Возникают першение в горле, парестезии, головная боль, светобоязнь, головокружение и обмороки на фоне падения АД. В ряде случаев беспокоит кашель, болезненные ощущения при глотании. В острой стадии, длящейся от 24 до 48 часов, пациентка выглядит заторможенной и дезориентированной.
Специфическое проявление синдрома — кожные высыпания в виде диффузного покраснения, которое напоминает солнечный ожог и начинает постепенно бледнеть на протяжении первых 3 дней. В последующем возникает грубое шелушение кожи, особенно заметное на подошвах и ладонях. У некоторых женщин покраснение носит характер пятен различных размеров, к которым присоединяются мелкие узелковые высыпания или точечные петехиальные кровоизлияния. Почти у четверти заболевших на 5—10-е сутки возникает сильный зуд на фоне пятнисто-узелковой сыпи. Практически у 100% пациенток к концу 1—2-ой недели наблюдается неглубокое генерализованное чешуйчатое отслаивание кожного эпителия с более выраженным пластинчатым шелушением ладоней, подошв, пальцев рук и ног. Половина пациенток, перенесших СТШ, к концу 2—3-го месяца отмечает выпадение волос и схождение ногтей.
Почти в 3/4 случаев выявляются гиперемия конъюнктивы, покраснение задней стенки глотки и слизистой рта, малиново-красный цвет языка. Каждую третью менструирующую женщину с СТШ беспокоят болезненность и отечность в области больших и малых половых губ. При тяжелом течении синдрома возникают признаки токсического поражения печени, почек, дыхательной системы с преходящей желтушностью кожи, болью в животе, пояснице, правом подреберье, помутнением мочи, одышкой и т. п.
Кроме клинически выраженного синдрома токсического шока, существует его стертая форма (при первичном проявлении или повторном эпизоде): у пациентки повышается температура, возникает озноб, умеренные мышечные боли, тошнота, рвота, понос, першение в горле. Однако артериальное давление не снижается, и патологическое состояние разрешается без лечения.
Осложнения
При тяжелом течении синдрома наблюдается токсический шок, приводящий к нарушению микроциркуляции и усугубляющий поражение паренхиматозных органов. Возникает дыхательная недостаточность с одышкой и ухудшением оксигенации крови, ДВС-синдром с тромбоэмболией и обильными кровотечениями, нарушается сердечный ритм, в результате острого тубулярного некроза отказывают почки. У пациенток со стрептококковым СТШ более чем в 50% случаев развиваются бактриемия и некротизирующий фасциит. В отдаленном периоде возможна временная потеря ногтей и волос, неврологические нарушения (парестезии, расстройства памяти, повышенная утомляемость).
Диагностика
С учетом полиорганного характера заболевания для постановки диагноза необходимо оценивать как локальные изменения со стороны женских органов, так и признаки нарушения других систем. В комплексное обследование включены:
- Осмотр гинеколога. Выявляются отечность и гиперемия половых органов, в некоторых случаях — скудные выделения гнойного характера из цервикального канала. Пальпаторно может определяться болезненность в области придатков.
- Физикальное обследование. В 100% случаев наблюдается повышение температуры более 38,9°С и падение систолического давления ниже 90 мм рт.ст. (обычно с ортостатическим снижением на 15 мм рт.ст.).
- Общеклинические анализы. Для ОАК характерны лейкоцитоз с высоким нейтрофилезом, сдвиг лейкоцитарной формулы влево, тромбоцитопения, анемия, повышение СОЭ. В общем анализе мочи определяется аномальный мочевой осадок с выщелоченными эритроцитами и стерильной пиурией.
- Биохимический анализ крови. При нарушенной функции печени повышаются уровень билирубина и активность трансфераз (выявляется почти у половины заболевших), при почечной недостаточности возникает азотемия, креатининемия, при поражении мышц — повышенное содержание КФК. В коагулограмме увеличивается протромбиновое время и частичное тромбопластиновое время, определяются продукты деградации фибрина. Анализ крови на электролиты выявляет метаболический ацидоз, снижение уровня кальция, фосфора, натрия, калия.
- Методы определения возбудителя. Для выявления инфекционного агента используют бакпосев мазка из половых органов с антибиотикограммой и посев крови (показан при подозрении на стрептококковый СТШ). Серологические исследования позволяют провести оценку показателей иммунной системы, исключить инфекционные заболевания со сходной клинической картиной.
- Инструментальная диагностика. ЭКГ позволяет своевременно выявить нарушения сердечного ритма. Флюорография или рентгенография ОГК рекомендованы для оценки состояния легких.
Синдром ТШ дифференцируют от сепсиса и инфекционных заболеваний (кори, скарлатины, лептоспироза, гепатита В, пятнистой лихорадки Скалистых гор, брюшного тифа, менингококцемии, вирусных экзантем). Пациентку консультируют анестезиолог-реаниматолог, инфекционист, кардиолог, хирург, уролог, дерматолог, пульмонолог, невропатолог.
Лечение синдрома токсического шока
При выборе схемы лечения синдрома токсического шока важно предусмотреть воздействие на факторы, вызвавшие заболевание, и мероприятия для стабилизации функций пораженных систем. Пациентке показаны:
- Санация бактериального очага. В первую очередь удаляют тампон, диафрагму, колпачок (при их наличии) и промывают влагалище стерильным раствором. При выявлении бактериально обсемененных ран возможно иссечение тканей с участками некроза.
- Антибиотикотерапия. Выбор препарата основан на результатах определения чувствительности к противомикробным средствам. До получения таких данных назначается эмпирическая терапия с учетом вероятного возбудителя и его возможной антибиотикорезистентности. Курс составляет до 10 дней.
- Инфузионная терапия. Ключевой элемент лечения — восстановление внутрисосудистого объема жидкости и стабилизация показателей гемодинамики. В зависимости от характера нарушений пациентке вливают кристаллоидные растворы, электролиты, свежезамороженную плазму крови, тромбоцитарную массу и т. п.
- Вазопрессорные средства. Если коррекция объема внутрисосудистой жидкости не позволяет нормализовать АД, вводят препараты с прессорным эффектом.
При выраженной органной недостаточности пациентке могут назначаться гемодиализ (при острой почечной недостаточности), искусственная вентиляция легких с положительным давлением на выдохе (при респираторном дистресс-синдроме). Ряд авторов отмечают более быстрое выздоровление при назначении кортикостероидов и иммуноглобулинов.
Прогноз и профилактика
В большинстве случаев благодаря достижениям современной гинекологии, своевременной диагностике и лечению пациентки со стафилококковым СТШ выздоравливают за 1—2 недели, при этом смертность на современном этапе составляет 2,6%. Температура и АД нормализуются в течение 2-х суток с момента госпитализации, а лабораторные показатели — на 7—14-ый день. Уровень эритроцитов восстанавливается через 4—6 недель. При стрептококковом токсическом шоке смертность до сих пор остается высокой и достигает 50%. Для профилактики СТШ важно соблюдать рекомендации по использованию тампонов и протоколы обследования перед родами и гинекологическими операциями для своевременного выявления возбудителей.
Токсины золотистого стафилококка. Мембранотоксины ( стафилолизины, гемолизины ). Эксфолиатины. Токсин синдрома токсического шока. Лейкоцидин ( токсин Пантона-Валентайна ). Энтеротоксины.
• Мембранотоксины (стафилолизины, или гемолизины) золотистого стафилококка. Выделяют токсины четырёх антигенных типов; бактерии способны одновременно синтезировать несколько подобных продуктов. Стафилолизины обусловливают гемолитическую активность стафилококков на средах с кровью.
а-Токсин золотистого стафилококка имеет наибольшее значение, его часто выявляют у бактерий, выделенных из клинических образцов. Он взаимодействует с клеточной мембраной и вызывает локальный протео-лиз. К его действию чувствительны эндотелиоциты, полиморфно-ядерные лейкоциты, фибробласты, гепатоциты, тромбоциты и др. При введении лабораторным животным а-токсин вызывает кожные некротические реакции, после внутривенного введения — гибель животных.
b-Токсин золотистого стафилококка (сфингомиелиназа) выявляют у 20% изолятов. Он проявляет выраженные свойства холодового гемолизина, то есть его активность максимальна при низкой температуре.
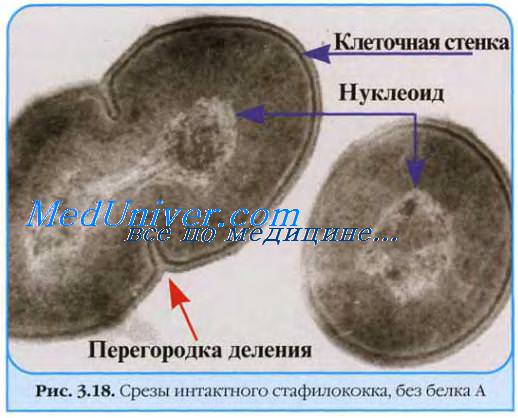
у-Токсин золотистого стафилококка — двухкомпонентный гемолизин с умеренной активностью в отношении эритроцитов человека. Гемолитическую активность на кровяных средах он обычно не проявляет, так как серосодержащие полимеры, присутствующие в агаре, инактивируют один из его компонентов.
Сигма-Токсин золотистого стафилококка — агрегат низкомолекулярных соединений, проявляющих детергентные свойства; последние обусловливают цитотоксичность широкого спектра.
• Токсин синдрома токсического шока (TSST-1 [от англ. Toxic Shock Syndrome Toxin], ранее — энтеротоксин F) — экзотоксин, обусловливающий развитие специфического симптомокомплекса (предположительно за счёт стимулирования выделения ФНО). Синтез TSST-I кодируют гены умеренных фагов; основные продуценты — стафилококки I фагогруппы, однако способностью к его образованию обладает незначительное количество штаммов.
• Лейкоцидин (токсин Пантона-Валентайна). Мишени действия TSST-1 — нейтрофилы и, возможно, макрофаги. Он нарушает водно-электролитный баланс в клетке, повышает внутриклеточное содержание циклического АМФ (одно из звеньев патогенеза стафилококковых диарей).
• Энтеротоксины А, В, Ci2, D, Е — термостабильные низкомолекулярные белки. Основные продуценты — бактерии III фагогруппы. Именно эти токсины ответственны за развитие пищевых отравлений. Наиболее часто регистрируют интоксикации, вызываемые энтеротоксинами А и D. Энтеротоксины В и С способны также вызывать развитие синдрома токсического шока в случаях, не связанных с менструациями. Проявляют свойства суперантигена.
Сенсибилизирующий эффект золотистого стафилококка. Многие компоненты бактериальных клеток и их метаболиты проявляют сенсибилизирующее действие, выражающееся в реакциях немедленного и замедленного типов. Клинически сенсибилизация бактериальными аллергенами характеризуется дерматитами, бронхоспастическим синдромом и т.д.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Клиника поражений золотистым стафилококком. Заболевания вызываемые золотистым стафилококком. Синдром ошпаренных младенцев ( болезнь Риттера фон Риттерштайна ). Синдром ошпаренной кожи ( синдром Лайелла ). Синдром токсического шока. Пищевые отравления.
Золотистые стафилококки способны поражать практически любые ткани организма человека. Инфекции, вызываемые S. aureus, включают более 100 нозологических форм (табл. 12-1).
• Внебольничные пневмонии, вызванные золотистым стафилококком ( S. aureus ), регистрируют достаточно редко, но в стационарах этот микроорганизм — второй по значимости возбудитель после синегнойной палочки.
• Стафилококковые бактериемии у госпитализированных больных развиваются при проникновении S. aureus через катетеры, из ран или очагов кожных поражений (в 20% случаев причину бактериемии установить не удаётся). Циркуляция возбудителя в кровотоке приводит к развитию метастатических поражений различных органов.
• Приблизительно у 10% больных с бактериемией золотистым стафилококком ( S. aureus ) может развиться эндокардит. В результате инфекций придаточных пазух носа, носоглотки, уха и сосцевидного отростка, а также бактериемии возбудитель может проникать в ЦНС и вызывать образование эпидуральных абсцессов и гнойных внутричерепных флебитов. Следствием эндокардита и бактериемии также считают поражения органов мочевыводящей системы (абсцессы, пиелонефриты и др.).
Синдром ошпаренных младенцев ( болезнь Риттера фон Риттерштайна )
Синдром ошпаренных младенцев (болезнь Риттера фон Риттерштайна) регистрируют у новорождённых, инфицированных штаммами золотистого стафилококка, выделяющими экс-фолиатины. Заболевание начинается бурно; характерно формирование больших очагов эритемы на коже с последующим образованием (через 2-3 сут) больших пузырей (как при термических ожогах) и обнажением мокнущих эрозированных участков.
Синдром ошпаренной кожи ( синдром Лайелла )
Синдром ошпаренной кожи (синдром Лайелла) возникает у более старших детей и взрослых. Характерны очаги эритемы, пузыри, тяжёлая интоксикация и отхождение субэпи-дермального слоя. При проведении профилактики вторичных инфекций происходит ограничение очагов поражения.
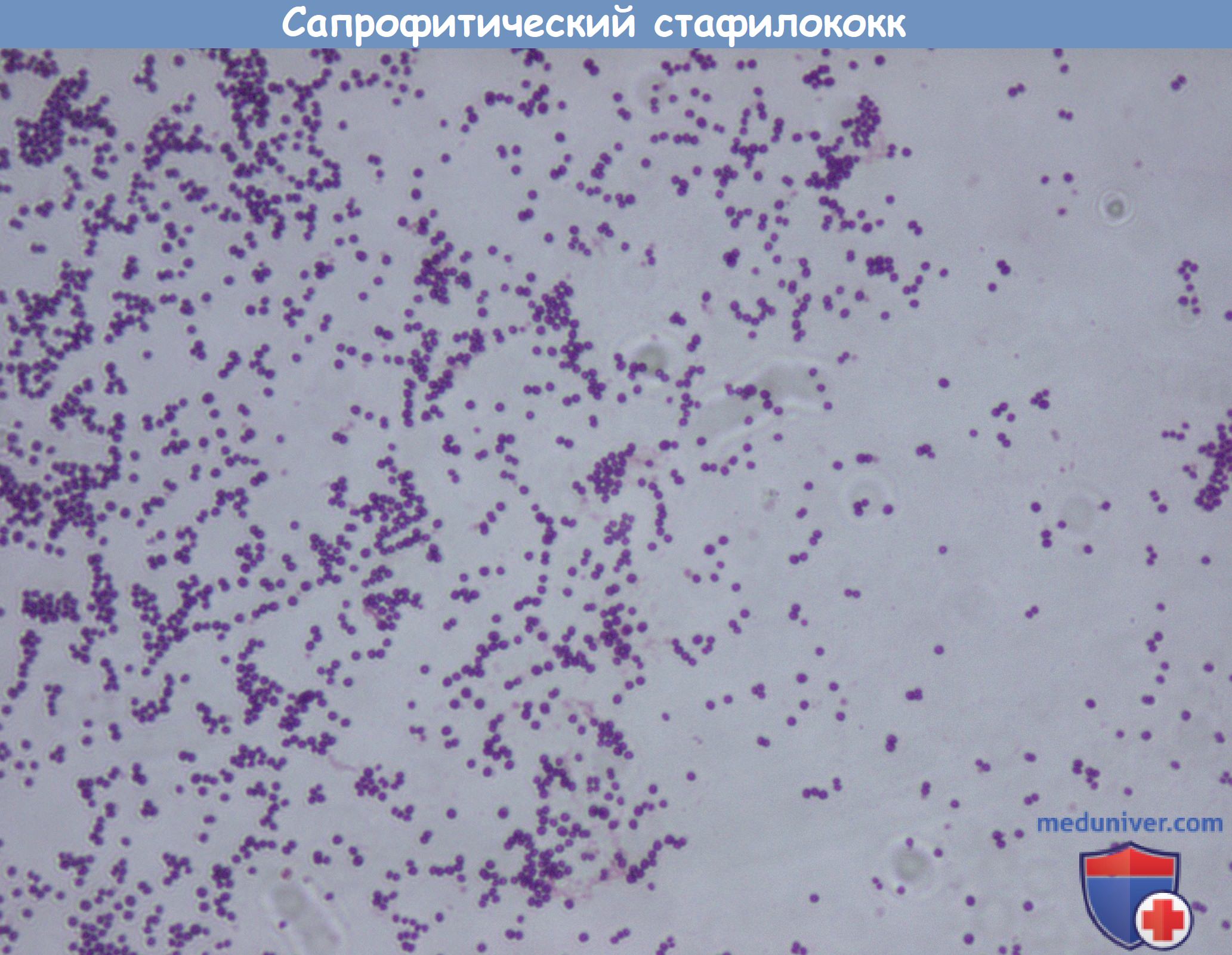
Синдром токсического шока
Пищевые стафилококковые отравления
Пищевые отравления проявляются рвотой, болями в животе и водянистой диареей уже через 2-6 ч после употребления в пищу инфицированных продуктов, обычно кондитерских изделий с кремом, консервов, мясных и овощных салатов и т.д. Высокая устойчивость стафилококков к высоким концентрациям NaCl позволяет им длительно сохраняться в различных пищевых концентратах. Патогенез поражений обусловлен способностью энтеротоксинов индуцировать избыточное образование ИЛ-2 (с проявлениями общих симптомов интоксикации и возбуждением гладкой мускулатуры кишечника).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

