Чем ослабляют живые противовирусные вакцины
Обновлено: 25.04.2024
Живые вакцины изготовляют из живых ослабленных (аттенуированных) штаммов вирусов. Такие штаммы должны обладать следующими стабильными, наследственно закрепленными свойствами:
- утрата вирулентности исходного вируса;
- сохранение способности приживаться и размножаться в организме;
- сохранение специфической иммуногенности исходного патогенного штамма;
- способность вызывать образование иммунитета у привитых животных.
Введенные в организм вакцинные штаммы должны вызывать не заболевание, а особое, качественно новое состояние — так называемый вакцинальный процесс.
Получение вакцинных штаммов с перечисленными свойствами удается путем культивирования вирулентных вирусов (обычно выделенных от больных животных в очаге инфекции) в условиях, не соответствующих их природным потребностям адаптирования к маловосприимчивым или невосприимчивым животным, а также выращивания в развивающихся куриных эмбрионах или в культуре клеток. При многократном пассировании на живых системах вирусы постепенно теряют патогенность, сохраняя антигенные свойства.
К перспективным методам получения вакцинных штаммов следует отнести селекцию природно-ослабленных штаммов вирусов при атипично или латентно протекающих инфекциях, а также селекцию мутантов, индуцированных физическими и химическими мутагенами (пониженная температура культивирования, ультрафиолетовое облучение, воздействие ультразвуком и др.).
Для приготовления живых вакцин используют также гетеротипичные антигенно-родственные апатогенные штаммы: штаммы вируса оспы голубей для профилактики оспы кур, вирус кори для защиты собак от чумы плотоядных, вакцинный штамм вируса чумы свиней для профилактики диареи крупного рогатого скота и др.
Технология изготовления живых вакцин сводится к культивированию вакцинного штамма вируса в какой-либо биологической живой системе (животные, куриные эмбрионы, культуры тканей и клеток). Полученный вируссодержащий материал подвергают очистке от балластных (клеточных компонентов и др.) веществ. Далее проводят контроль на чистоту (посев на бактериальные питательные среды), безвредность и активность на восприимчивых животных. При соответствии этим требованиям полученный материал разливают по ампулам или флаконам и подвергают лиофильному высушиванию.
Живые вакцины, полученные на основе аттенуированных вакцинных штаммов вирусов, обладают рядом преимуществ перед инактивированными. Главное из них — напряженность и длительность создаваемого ими иммунитета, приближающегося к постинфекционному. Важное достоинство большинства живых вакцин — однократное введение. При этом происходит репродукция вакцинного штамма в организме в результате образования и поступления в организм в течение длительного времени активных антигенных субстанций, обеспечивающих формирование напряженного иммунитета. Вторым преимуществом живых вакцин является возможность вводить их не только подкожно, но и перорально, интраназально и аэрозольно.
Однако живые вакцины наряду с отмеченными преимуществами имеют и ряд недостатков, связанных с тем, что действующее начало этих препаратов (живых вирусов) весьма чувствительно к неблагоприятным факторам, возникающим в производстве, при транспортировке, хранении и применении, а также не исключена возможность реверсии вируса.
В специальных требованиях предусматривается качество компонентов живых вакцин и особенно чистота вируссодержащего материала. При получении живых вакцин на культурах клеток, в куриных эмбрионах субстраты могут оказаться контаминированными посторонними вирусами, микоплазмами, бактериями, и это может привести к серьезным последствиям.
Живые вакцины не содержат консервантов, поэтому при вскрытии ампул и растворении их содержимого необходимо строго соблюдать правила асептики. При накожном методе вакцинации необходимо использование для предварительной обработки таких дезинфицирующих средств, которые длительное время сохраняются на месте применения препарата.
Вакцины. Виды антигенов вакцин. Классификация вакцин. Виды вакцин. Живые вакцины. Ослабленные ( аттенуированные ) вакцины. Дивергентные вакцины.
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
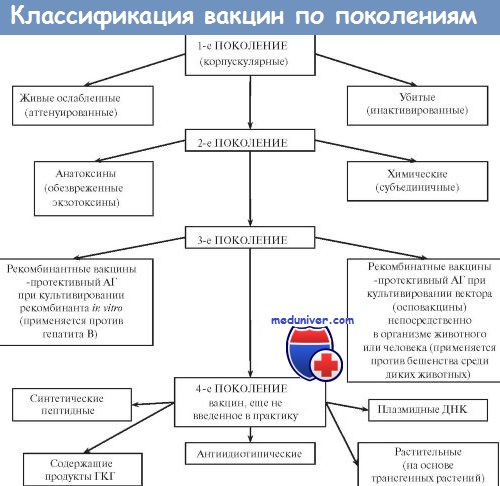
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Классификация вирусных вакцин. Типы вирусных вакцин.
Современной науке известны сотни видов патогенных вирусов, относящихся к 26 семействам, избирательно поражающим различные системы организма человека и животных. Природное многообразие вирусных болезней вызывало необходимость наряду с санитарно-гигиеническими мерами прибегнуть к специфической профилактике с использованием широкого круга вакцинных препаратов.
Вакцинопрофилактика занимает ведущее место в борьбе со многими вирусными заболеваниями человека и животных. Несмотря на большое разнообразие вирусов и вызываемых ими заболеваний, имеются общие принципы приготовления и применения вирусных вакцин. Однако в настоящее время не все вирусные болезни в одинаковой степени удается контролировать с помощью вакцинации.
Вакцинация должна сопровождаться развитием иммунологической памяти. В идеале, это поддержание специфических антител в высокой концентрации в сыворотке крови и на месте внедрения вируса. В тоже время Т-клетки, ответственные за специфический клеточный иммунитет, должны находиться в состоянии готовности быстро синтезировать свои летальные продукты (т.е. гранзимы и перфорины), когда происходит инфицирование. Все существующие на сегодня вакцины можно разделить на три общие группы: инактивированные (убитые), живые (аттенуированные) и компонентные (субъединичные) вакцины. Каждая из этих категорий вакцин имеет свои преимущества и недостатки.
В зависимости от технологии изготовления различают несколько типов вирусных вакцин:
1. Живые реплицирующиеся вакцины:
— вакцины из природно ослабленных или гетерологичных вирусов;
— вакцины из вирусов, аттенуированных пассажами в гетерологичных организмах или в культурах клеток при обычной или пониженной температуре, или реассортацией вирусных генов.

2. Нереплицирующиеся вакцины, содержащие природные вирусные антигены:
- вакцины из инактивированных целых вирионов и неструктурных вирусных белков;
- вакцины из нативных вирусных субъединиц.
3. Вакцины, полученные с помощью рекомбинантной ДНК или других новых технологий:
- вакцины, полученные путем делеции гена (генов) или точечного мутагенеза;
- вакцины на основе вирусных белков, экспрессированных in vitro в клетках эукариотов или прокатиотов;
- вакцины из вирусных белков, собранных в вирусоподобные частицы;
- вакцины, экспрессирующие вирусные антигены с помощью вирусных векторов;
- вакцины на основе вирусных химер;
- ДНК-вакцины.
4. Синтетические полипептидные вакцины.
Живые вакцины содержат авирулентные штаммы вирусов, аттенуированные разными способами, и отличаются способностью размножаться в привитом организме (реплицирующиеся антигены). Остальные типы вакцин готовят из инактивированных вирусов или их антигенных и иммуногенных компонентов (нереплицирующиеся антигены).
Используя другие принципы классификации, вакцинные препараты можно разделить на две большие группы: цельновирионные и компонентные (субъединичные). Причем к первой группе относятся как традиционные живые, так и инактивированные вакцины. Живые гомологичные вакцины, в свою очередь, могут различаться способом получения и быть представленными природно аттенуированными или искусственно ослабленными штаммами, включая рекомбинантные и реассортантные, а также штаммы, аттенуированные цельнонаправленными изменениями генома биотехнологическими методами.
К компонентным (субъединичным) вакцинам можно отнести все, которые не входят в рубрику цельновирионных вакцин. Прежде всего, сюда относятся вакцины, полученные из компонентов вирионов или вирус-инфицированных клеток после их разрушения. Кроме них к этой категории относятся субъединичные вакцины, приготовленные из вирусных белков, экспрессируемых клонированными вирусными генами в эукариотических или прокариотических системах. Сюда же можно отнести живые рекомбинантные вакцины, которые по своей сути являются реплицирующимися субъединичными вакцинами. Клонированные гены, реплицируясь в составе вирусного вектора, обеспечивают экспрессию белков, ответственных за индукцию специфического иммунитета.
Вакцины на основе вирусспецифических пептидов, получаемых синтетическим путем, в известном смысле, тоже можно отнести к разряду субъединичных (эпитопных) вакцин.
Анализ имеющихся данных свидетельствует о достаточно высокой эффективности многих вирусных вакцин, применяемых в медицинской и ветеринарной практике. Это, прежде всего, относится к живым вакцинам, применяемым для контроля таких массовых и опасных заболеваний человека, как полиомиелит, желтая лихорадка, корь, эпидемический паротит, краснуха и др. Аналогичным примером из практики ветеринарной медицины могут служить живые вакцины против чумы свиней, крупного рогатого скота и плотоядных, против ньюкаслской болезни и другие. Примером инактивированных вакцин могут служить вакцины против полиомиелита, гриппа, ящура и многих других болезней.
Некоторые из живых вакцин (оспа человека, полиомиелит, желтая лихорадка, корь, чума крупного рогатого скота, классическая чума свиней и др.) отвечают требованиям безопасности (генетическая стабильность, отсутствие реверсии, слабая реактогенность), обеспечивают длительный напряженный иммунитет и могут служить образцом для вновь создаваемых вакцинных препаратов.
Возбудители многих вирусных заболеваний (полиомиелит, грипп, ящур, катаральная лихорадка овец, чума лошадей и др.) существуют в виде нескольких антигенных типов. Поскольку иммунизация против одного из этих типов не защищает от заражения другими, эффективная профилактика возможна только при вакцинации поливалентной вакциной, содержащей антигены нескольких антигенных типов данного вируса. Вакцины, содержащие антигены более чем одного вида возбудителя, называют комбинированными (ассоциированными).
Большинство применяемых в настоящее время вакцин содержит антигены, идентичные или подобные антигенам вирулентного вируса, против которого предполагается создать иммунитет. Такие вакцины называют гомологичными. В некоторых случаях для приготовления вакцин используют гетерологичные вирусы, содержащие перекрестно-реагирующие антигены и создающие достаточный иммунитет. Такие вакцины называются гетерологичными.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Живые вирусные вакцины. Особенности живых вакцин.
Живые вирусные вакцины — это, как правило, искусственно ослабленные посредством культивирования или природные авирулентные либо слабовирулентные иммуногенные штаммы вируса, которые, размножаясь в естественно восприимчивом организме, не проявляют повышения вирулентности и потеряли способность к горизонтальной передаче.
Безопасные высокоиммуногенные живые вакцины являются лучшими из всех существующих вирусных вакцин. Применение многих из них дало блестящие результаты в борьбе с наиболее опасными вирусными болезнями человека и животных. В основе эффективности живых вакцин лежит имитация субклинической инфекции. Живые вакцины вызывают иммунный ответ на каждый протективный антиген вируса.
Основным преимуществом живых вакцин считается активизация всех звеньев иммунной системы, вызывающая сбалансированный иммунный ответ (системный и локальный, иммуноглобулиновый и клеточный). Это имеет особое значение при тех инфекциях, когда клеточный иммунитет играет важную роль, а также при инфекциях слизистых оболочек, где требуется как системный, так и локальный иммунитет. Местное применение живых вакцин обычно является более эффективным для стимулирования локального ответа у непраймированных хозяев, чем инактивированные вакцины, вводимые парентерально.
В идеале, вакцинация должна повторять иммунологические стимулы естественной инфекции, сводя до минимума нежелательные эффекты. Она должна вызывать напряженный продолжительный иммунитет при введении в небольшой дозе. Ее введение, как правило, не должно сопровождаться слабой, кратковременной общей и местной реакцией. Хотя после введения живой вакцины иногда допускается развитие у небольшой части реципиентов отдельных слабовыраженных клинических признаков, напоминающих легкое течение естественной болезни. Живые вакцины больше, чем другие, отвечают этим требованиям и, кроме того, отличаются низкой стоимостью и простотой применения разными способами.
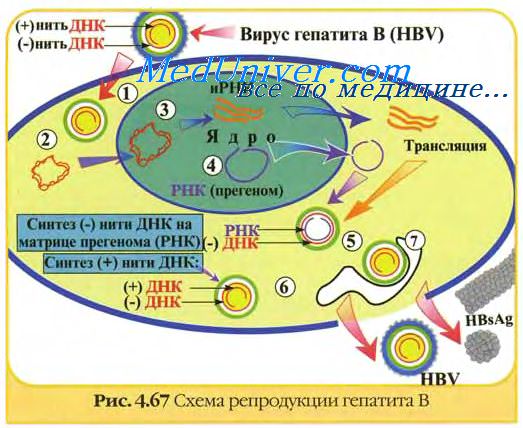
Вакцинные вирусные штаммы должны обладать генетической и фенотипической стабильностью. Их приживляемость в привитом организме должна быть выраженной, а способность к размножению ограниченной. Вакцинные штаммы обладают значительно менее выраженной инвазивностью, чем их вирулентные предшественники. Это связано в значительной мере с их частично ограниченной репликацией в месте проникновения и в органах-мишенях естественного хозяина. Репликация вакцинных штаммов в организме легче ограничивается естественными неспецифическими защитными механизмами. Вакцинные штаммы размножаются в привитом организме до тех пор, пока его защитные механизмы не затормозят их развитие.
В течение этого времени образуется такое количество антигена, которое значительно превышает его при введении с инактивированной вакциной.
Для аттенуации вирусов обычно применяют пассажи вируса в неестественном хозяине или культуре клеток, пассажи при пониженной температуре и мутагенез с последующей селекцией мутантов с измененным фенотипом.
Большинство современных живых вакцин, используемых для профилактики инфекционных болезней человека и животных, получены пассажами вирулентного вируса в гетерологичном хозяине (животные, куриные эмбрионы, различные клеточные культуры). Аттенуированные в чужеродном организме вирусы приобретают множественные мутации в геноме, препятствующие реверсии вирулентных свойств.
В настоящее время в практике широко применяют живые вакцины против многих вирусных заболеваний человека (полиомиелит, желтая лихорадка, грипп, корь, краснуха, паротит и др.) и животных (чума крупного рогатого скота, свиней, плотоядных, бешенство, герпес-, пикорна-, коронавирусные и другие болезни). Однако еще не удалось получить эффективных вакцин против ряда вирусных болезней человека (СПИД, парагрипп, респираторно-синциальная инфекция, денгевирусная инфекция и другие) и животных (африканская чума свиней, инфекционная анемия лошадей и другие).
Имеется много примеров тому, что традиционные методы аттенуации вирусов еще не исчерпали своих возможностей и продолжают играть существенную роль в разработке живых вакцин. Однако их значение постепенно уменьшается по мере увеличения масштабов использования новой технологии конструирования вакцинных штаммов. Несмотря на значительный прогресс в этой области, принципы получения живых вирусных вакцин, заложенные Л. Пастером, до сих пор не потеряли своей актуальности.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
- Живые вакцины. Защищают от полиомиелита, кори, краснухи, гриппа, эпидемического паротита, ветряной оспы, туберкулеза, ротавирусной инфекции. Основу препарата составляют ослабленные микроорганизмы — возбудители болезней. Их сил недостаточно для развития значительного недомогания у пациента, но хватает, чтобы выработать адекватный иммунный ответ.
- Инактивированные вакцины. Прививки против гриппа, брюшного тифа, клещевого энцефалита, бешенства, гепатита А, менингококковой инфекции и др. В составе мертвые (убитые) бактерии или их фрагменты.
- Анатоксины (токсоиды). Особым образом обработанные токсины бактерий. На их основе делают прививочный материал от коклюша, столбняка, дифтерии.
В последние годы появился еще один вид вакцин — молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
Живые бактериальные

Схема подходит для вакцины БЦЖ, БЦЖ-М.
Живые противовирусные

Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
- куриные эмбрионы;
- перепелиные эмбриональные фибробласты;
- первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков);
- перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293).
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
Инактивированные антибактериальные вакцины

- Культивация и очистка штаммов бактерий.
- Инактивация биомассы.
- Для расщепленных вакцин клетки микробов дезинтегрируют и осаждают антигены с последующим их хроматографическим выделением.
- Для конъюгированных вакцин полученные при предыдущей обработке антигены (как правило, полисахаридные) сближают с белком-носителем (конъюгация).
Инактивированные противовирусные вакцины

- Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться куриные эмбрионы, перепелиные эмбриональные фибробласты, первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков), перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293). Первичная очистка для удаления клеточного дебриса проводится методами ультрацентрифугирования и диафильтрации.
- Для инактивации используются ультрафиолет, формалин, бета-пропиолактон.
- В случае приготовления расщепленных или субъединичных вакцин полупродукт подвергают действию детергента с целью разрушить вирусные частицы, а затем выделяют специфические антигены тонкой хроматографией.
- Человеческий сывороточный альбумин применяется для стабилизации полученного вещества.
- Криопротекторы (в лиофилизатах): сахароза, поливинилпирролидон, желатин.
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
Анатоксины

Для дезактивации вредного воздействия токсинов используют методы:
- химический (обработка спиртом, ацетоном или формальдегидом);
- физический (подогрев).
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Я много лет вакцинируюсь от гриппа вакциной французского производителя. В этом году терапевт предложила мне сделать прививку российской вакциной. Я ничего не знаю об отечественных вакцинах, какая из них качественная?
Отвечает Полибин Роман Владимирович
Отвечает Харит Сусанна Михайловна
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Вы абсолютно правы, если в контейнере был лед. Но если там была смесь воды и льда- вакцина не должна замерзать. Однако живые вакцины, к которым относится ротавирусная, не увеличивают реактогенность при температуре менее 0, в отличие от неживых, а, например, для живой полиомиелитной допускается замораживание до -20 град С.
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму. В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска.
Отвечает Полибин Роман Владимирович
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
Читайте также:

