Цикл жизни вируса гепатита с
Обновлено: 25.04.2024
До создания своей научной группы я работал в лаборатории молекулярных основ действия физиологически активных соединений, которая занимается противовирусными препаратами, исследованиями и поиском самых разных лекарств против ВИЧ, герпеса и других вирусов. Там в 1980–1990-е годы создали препарат против СПИДа, который используется врачами с 1999 года. В лаборатории также разработали нуклеозидный препарат, который сейчас проходит третью стадию клинических испытаний.
О вирусе гепатита
Существует пять вирусных гепатитов: А, В, С, D, E.
А и E стоят особняком. Гепатит А — это болезнь грязных рук, болезнь Боткина. Всегда проявляется в острой стадии, всегда сопровождается желтухой глаз и кожного покрова. У 0,5–1% больных бывают осложнения в виде фульминантного гепатита, когда отказывает печень, но в целом после излечения человек получает пожизненный иммунитет. Гепатит E примерно такой же. Против гепатита А существует хорошая вакцина, в Китае есть препарат против гепатита E.
Хронические заболевания вызывают три остальных вида гепатита: В, С и очень странный полувирус (его называют вироидом) гепатита D. D — это паразит при паразите, сателлит гепатита B. Он может инфицировать людей, зараженных гепатитом В, использовать его белки для создания вирионов. Важно, что он ухудшает прогноз течения заболевания, ускоряет прогрессию к циррозу и раку печени.
Если сравнить гепатиты В и С, то можно отметить, что гепатит В во многих случаях вызывает желтуху, а у значительного числа пациентов (зависит от возраста) — переходит в хроническую стадию. Гепатит C крайне редко сопровождается симптомами при остром заболевании, но в 80% случаев становится хроническим.
Сколько больных гепатитом в мире?
То, что нет точной информации, сколько действительно пациентов, больных гепатитами B и С, в мире и, в частности, в нашей стране, — большая проблема. Тестируют только тех, кто приходит в больницы, проверяя их на гепатиты В, С и ВИЧ. Некоторые работы по оценке количества заболевших делались, например, на основе тестирования призывников и заключенных.
Однако в целом в России не проводится скрининг среди разных возрастов в разных регионах. Скорее всего, реальная цифра в РФ — 1 млн с лишним, но, конечно, эту оценку стоило бы верифицировать.
По информации ВОЗ, сейчас в мире 71 млн хронически больных гепатитом. Можно сказать, что количество больных уменьшается.
Открытие вирусов гепатитов
Так как гепатит А проявляет себя открыто, его вирус давно изучен. Гепатит B тоже открыто проявляется, его вирус также известен. В 1970-е годы был охарактеризован патоген гепатита D.
Сложнее было с вирусом гепатита C. Медики знали, что у немалого количества пациентов есть заболевание, сходное с гепатитом В. Понимали, что это хроническая болезнь печени; скорее всего, вызывается вирусом; что это не гепатиты А, В или D. Было известно, что часто им заболевали те, кому неоднократно делали переливание крови.
Возникает вопрос: а вызывает ли найденный вирус заболевание? Да, он есть, но вирус — не значит болезнь. Над этим вопросом работали несколько исследовательских групп. Одна из них — группа Чарлза Райса (Charles M. Rice), которая охарактеризовала недостающий фрагмент вирусной геномной РНК. Далее они получили полную РНК вируса гепатита C и инфицировали шимпанзе. Эксперимент показал, что у шимпанзе возникает болезнь, сходная с гепатитом C.
К сожалению, многие исследователи в этой области остались за кадром нобелевской награды. Большая часть важных работ того же Чарлза Райса датируется 2000-ми годами, и премию ему дали немножко не за то. Эксперименты с шимпанзе в 1990-е вели и другие группы ученых, например группа Йенса Буха, которая работала с другими командами.
Итак, в 1989 году был охарактеризован вирус гепатита C. Какие важные открытия были сделаны потом? Все 1990-е годы ученые бились над созданием его клеточных моделей: добавляли вирус к самым разным культурам клеток, а репликации не было. Ни на какой линии клеток! То есть что-то там через сутки видно, но через три дня уже этого вируса нет.
В 1997 году группа Чарлза Райса смогла инфицировать гепатитом C шимпанзе. Но и это не позволило реплицировать вирус в культуре клеток.
Прорывной была работа группы Ральфа Бартеншлагера (Ralf Bartenschlager), профессора кафедры инфекционных заболеваний Гейдельбергского университета, результаты которой опубликованы в журнале Science в 1999 году. Они смогли найти уникальную линию клеток гепатомы печени, которая поддерживала только репликацию, т. е. центральную стадию жизненного цикла вирусной РНК — что полноразмерной, что усеченной, когда удалены структурные белки (которые и образуют оболочку вириона). Но и в этих экспериментах была проблема эффективности: ученые брали огромное количество вирусной РНК, несколько миллионов клеток, а количество клеток, поддерживающих репликацию, оказалось мизерным. То есть даже в этой линии лишь совсем небольшая доля клеток является пермиссивными к вирусу.
Дальше шла работа над поиском системы репликонов, которые поддерживают репликацию без сборки вирионов. Тогда же начался скрининг ингибиторов. Группа Бартеншлагера оставалась в Европе в числе лидеров по исследованию вируса гепатита C и родственному ему. Чарлз Райс и его американская научная группа также остаются лидерами в этой области.
Чарлз М. Райс. Фото с сайта rockefeller.edu
В чем заслуга Райса? Он был тем исследователем, который сделал сходный репликон через полгода после публикации Бартеншлагера в Science. А после лаборатории Чарлза и Ральфа начали работать параллельно, характеризуя то, как происходит репликация этого вируса, как адаптируется вирус к клеткам, клетки — к вирусу и т. д. Следующее, что сделала группа Райса, — один из вариантов этой линии, который был уже более пермиссивным, лучше поддерживал репликацию: не считанного количества, а 40% клеток.
Еще одно суперважное открытие, сделанное в 2000 году: в Японии был характеризован уникальный пациент с фульминантным гепатитом — массовым некрозом печени. В норме вирус не вызывает никаких проявлений в острой стадии, а тут была массовая гибель гепатоцитов.
Наверняка кто-то из наших читателей сдавал печеночные пробы, где важны показатели АЛТ и АСТ ( аланинаминотрансферазы и аспартатаминотрансферазы ), и знает, что граница по АЛТ равна 42. Эти показатели стандартно входят в биохимический анализ крови. У японского пациента АЛТ был равен 15 тыс. Почему это интересно? В этой части исследования участвовал Такадзи Вакита (Takaji Wakita), который охарактеризовал вирус этого больного в 2003 году и показал, что такой репликон тоже суперрепликационно активен. А в 2005 году группа Вакиты вместе с Райсом продемонстрировала, что в клетках с таким полногеномным репликоном происходит сборка инфекционных частиц, т. е. вирус от этого пациента в этой линии клеток проходит полный клеточный цикл. И дальше вся биология патогена исследовалась в вышеуказанной клеточной инфекционной системе.
Нобелевский комитет, к сожалению, не отметил заслуг ни Ральфа Бартеншлагера, ни Такадзи Вакиты. Хотя они, с моей точки зрения, достойны награды, и многие специалисты в этой области исследований считают, что они могли бы стать лауреатами Нобелевской премии.
Лечение гепатита C
Борьба с вирусом гепатита C шла долго. От открытия вирусов в 1989 году до создания репликонов прошло 10 лет, и 16 лет — до появления инфекционной системы, она была сделана в 2005 году. А уже в 2011-м в клинику вошли первые противовирусные препараты прямого действия.
Гепатиты В и С — онкогенные вирусы, вызывающие рак печени, а именно гепатоклеточную, или гепатоцеллюлярную, карциному. Считается, что именно эти два вируса обуславливают до 80% случаев этого рака печени. Люди умирают не только от рака, но и от цирроза печени. Это сотни тысяч смертей в год. Поэтому с вирусами гепатитов В и С надо бороться. От гепатита В есть профилактическая вакцина, а от гепатита C нет и, по-видимому, не будет. Тем не менее, существуют эффективные лекарства.
В конце 1990-х — начале 2000-х гепатит C начали лечить рекомбинантными интерферонами. Курс длился от полугода до года в зависимости от генотипа вируса. Терапия интерферонами очень плохо воспринималась, потому что они вызывают гриппоподобное состояние. К тому же такое лечение было малоэффективным: больной проходил полный курс, но вылечивался лишь в 40% случаев; к 60% пациентов вирус возвращался.
Что есть сейчас? Несколько препаратов, направленных на три вирусных белка: полимеразу (NS5B), протеазу (NS3) и регуляторный белок NS5A. При помощи этих препаратов можно вылечить любого пациента; эффективность 99%. Как говорят на конференциях, во многих случаях недостающие 1% или 2% обусловлены не столько устойчивостью вируса, сколько тем, что ряд пациентов не приходит сдавать анализы через полгода, а по медицинским стандартам излечением считается отсутствие вирусной РНК через шесть месяцев после окончания лечения.
Нужно подчеркнуть, что гепатит C в отличие от гепатита В излечим. Если вирусной РНК нет через полгода после окончания терапии, он не возродится, а если вирус опять обнаруживается, то имеет место случай реинфекции, что подтверждается секвенированием. Соответственно, теперь вылечить от гепатита C можно любого человека.
Уже в середине 2010-х годов стало понятно, что при помощи вышеописанных препаратов можно лечить случаи коинфекции с гепатитом В или ВИЧ. Единственное, что нужно при этом учитывать, — взаимодействие лекарств. Можно вылечить и гепатит C, и многие случаи цирроза печени, в этой области также имеется огромный прогресс.
Стоит отметить, что излечение от инфекции действительно снижает риски появления рака печени. Однако для таких пациентов эти риски всё равно остаются повышенными. И особенно высокими в случае, если уже появились цирроз или фиброз. Но у многих пациентов может происходить и регрессия фиброза.
Полученные наработки можно использовать для борьбы с коронавирусами
— На ваш взгляд, почему Нобелевскую премию за открытие вируса гепатита C вручили в этом году? Это как-то связано с пандемией коронавируса?
— Вы исследуете коронавирус?
— Мы сделали первую систему проверки на антитела в Москве. Помогали коллегам одного из ФНКЦ ФМБА, которые работали в первую волну, искать доноров плазмы. Но наши усилия были ограничены тем, что наш институт относится к Миннауки, и у нас всех женщин с детьми до 14 лет, всех пожилых отправили на удаленку. В нашей лаборатории работали очно всего два человека.
На мой взгляд, в борьбе с COVID-19 нужно искать противовирусные препараты. Все ударились в создание вакцин, но что там с вакциной получится. У меня легкий скептицизм, к тому же, например, у меня аутоиммунное заболевание, что является противопоказанием к этой вакцинации.
Мы хотим и пытаемся анализировать полиморфизмы человека, которые могут определять устойчивость или чувствительность к инфекции или чувствительность к заболеванию, потому что те же полиморфизмы с интерфероном лямбда, они же интерлейкины-28В, возможно, будут играть важную роль. Это сейчас очень горячая тема, и все вирусологи что-то в этой области делают.
— Путь до победы над коронавирусом может занять десятилетия, как это было с вирусом гепатита C?
— Да, над гепатитом C мучались почти 30 лет. Но на самом деле работа шла с 1999 по 2011 год. Как говорят западные клиницисты, которые работают с гепатитом C, денег при этом выделялось намного меньше, чем на борьбу с ВИЧ. Ученые чрезвычайно быстро разобрались с вирусом гепатита C очень малыми усилиями при очень маленьком финансировании. Нашли четыре рецептора, которые необходимы, уникальную клеточную линию, которую можно заразить; разобрались, что определяет чувствительность этой линии; обнаружили, что адаптация вируса под эту линию делает его неинфекционной к животным. Правда, пока работали только с шимпанзе. Следующая модель — это так называемые голые мыши, иммунодефицитные мыши, которым в раннем возрасте приживляют человеческие гепатоциты, и у них вырастает химерная человеческая печень, состоящая на 80% из клеток человека. Это работа группы Лорна Тиррелла (Lorne Tyrrell) из Альбертского университета (Канада), где работает Майкл Хоутон. И это ближайшая модель из существующих.
Что такое гепатит Е? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит Е — это острое (и редко хроническое) инфекционное заболевание, которое вызывает вирус гепатита Е. Клинически проявляется синдромом общей инфекционной интоксикации, энтерита (воспаления тонкой кишки) и холестаза (застоя желчи), желтухой, увеличением и нарушением работы печени. Болезнь протекает доброкачественно, за исключением беременных, у которых заболевание имеет катастрофические последствия в любом триместре беременности.
Этиология
Вид — вирус гепатита Е (HЕV)
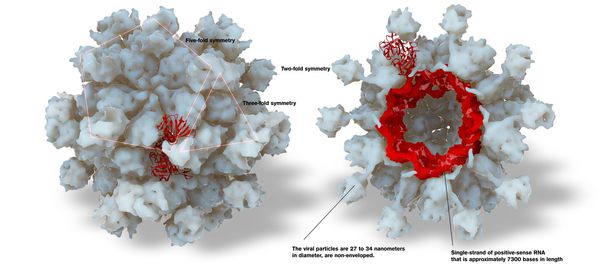
Данный вирус представляет собой одноцепочечный РНК-вирус округлой формы диаметром 30-35 нм. Он лишён наружной оболочки. На поверхности вириона есть вдавления, напоминающие чаши.
Чтобы вирус внедрился в клетку, в процессе жизни он кодирует трансмембранный белок и такие ферменты, как РНК-зависимую РНК-полимеразу, РНК-хеликазу, метилтрансферазу и папаин-подобную протеазу.
Существует пять генотипов вируса:
- I и II — только человеческие;
- III и IV — есть также у животных, т. е. может передаваться от них людям; вызывает хронические формы, если есть предрасположенность;
- V — птичий.
При температуре от 0°C быстро инактивируется. Длительно сохраняется в воде и при отрицательных температурах. Неплохо себя чувствует в ЖКТ человека. Хорошо сохраняется в плохо прожаренном мясе. При нагревании воды до 71°C погибает в течение 20 минут, при кипячении — практически мгновенно [1] [2] [3] [8] [10] .
Эпидемиология
Источник инфекции — вирусоноситель или человек, который уже болен какой-либо формой гепатита Е, в особенности острой. Вирус распространяется с последней недели инкубационного периода и до 30 дней от начала заболевания.
Каждый год повсеместно регистрируется около 3,3 млн случаев заболевания. При этом количество людей с гепатитом Е, который протекает пока без симптомов или совсем себя не проявляет, по предварительным оценкам может достигать 20 млн. Смертность — около 4 %, преимущественно умирают беременные.
В окружающую среду вирус выделяется с экскрементами инфицированных людей. Иногда человек заражается при употреблении недостаточно приготовленного мяса свиней, оленей и моллюсков.
- фекально-оральный — через заражённые вирусом руки (контактно-бытовой путь), воду или пищу;
- парентеральный — при переливании крови (встречается редко);
- половой путь — при орально-анальном контакте;
- вертикальный — от матери к плоду.

Наибольшее значение имеет водный путь передачи. Часто он связан с сезоном дождей и наводнениями, когда вода загрязняется фекалиями.
Восприимчивость к гепатиту Е высокая. Преимущественно болеют люди 15-44 лет. К группе повышенного риска относятся работники животноводческих ферм и боен.
Факторы риска заражения:
- высокая плотность населения, особенно в бедных странах;
- антисанитария, несоблюдение правил личной гигиены, неправильное хранение, обработка и приготовление пищи;
- нарушения санитарно-технических требований на объектах водоснабжения — заражение воды;
- бытовой очаг заболевания.
Заболевание обычно возникает в осенне-весенний период. В основном распространено в странах Восточной и Южной Азии.
После перенесённой болезни формируется стойкий иммунитет, чаще пожизненный [1] [3] [7] [9] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Е
Болезнь начинается постепенно. Инкубационный период длится от 2 до 10 недель.
Как и в случае гепатита А, заболевание обычно протекает в бессимптомной и субклинической (предсимптомной) форме.
При возникновении явных клинических признаков (т. е. при манифестации), преобладают случаи лёгкого и среднетяжёлого течения. Симптоматика медленно нарастает. Появляется немотивированная слабость, подташнивание, снижение аппетита, повышение температуры до 37,1-38,0°С (субфебрилитет), дискомфорт и тяжесть в правом подреберье, дискомфорт в суставах, возможна рвота.
Вслед за этими симптомами через 3-7 дней наступает желтушный период, который длится максимум один месяц. Он сопровождается пожелтением кожи и слизистых оболочек, потемнением мочи и обесцвечиванием кала. Общее состояние больных не улучшается, сохраняется плохое самочувствие, выраженный дискомфорт в правом подреберье, увеличение размеров печени и селезёнки, желтушность кожных покровов, нарастает зуд кожи.
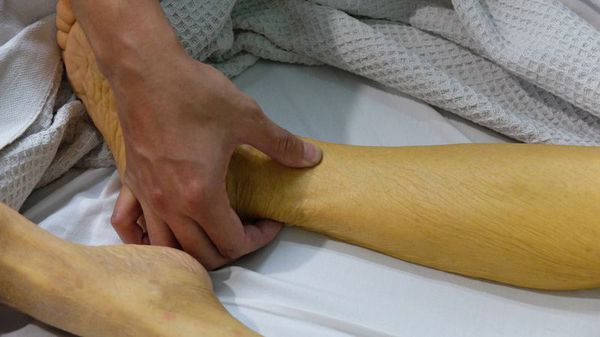
При неосложнённом и нетяжёлом течении начинает медленно регрессировать в течение нескольких недель. Как правило, после этого человек полностью выздоровливает, иногда развиваются непродолжительные остаточные явления в виде астении (бессилия) и дискомфорта в правом подреберье.
Раньше считалось, что гепатит Е — лишь острое заболевание. Однако в последнее время накоплен ряд данных, позволяющих выделить небольшую группу больных, переносящих хронический вариант болезни. Он встречается у ВИЧ-инфицированных людей в стадии СПИДа, после пересадки органов, а также у тех, кто получает мощную иммуносупрессивную терапию.
Специфичной симптоматики у хронического гепатита А нет. Больные жалуются на повышенную утомляемость, артралгии, неустойчивый стул, тяжесть в правом подреберье, субфебрилитет, иногда устойчивый лёгкий зуд кожи. Если не лечить это состояние, может развиться цирроз печени.
Гепатит Е у беременных
При заражении беременной в I и II триместрах происходит 100 % гибель плода. Летальность самих беременных невелика.
При заражении беременной в III триместре ребёнок может родиться живым, но 50 % из них умирают в первые месяцы жизни. Смертность самих женщин достигает 25-30 %. А если беременные живут в районах, которым не свойственно данное заболевание, то летальность может достигать 80 %.
Тяжесть течения Гепатита А при беременности связана со специфической аутоиммунной перестройкой организма женщины. В этом случае заболевание часто протекает по фульминантному типу (острой печеночной недостаточности) — на фоне начальных симптомов болезни резко нарастает желтуха, развивается тяжёлая интоксикация, некупируемая рвота, кровотечения (ДВС-синдром), нарушается сознание. Роды (преждевременные или выкидыш) стремительно ухудшают состояние больной: развиваются массивные послеродовые кровотечения, острая почечная недостаточность, печеночная энцефалопатия. Из-за такого состояния в острый период искусственно прерывать беременность нельзя [1] [5] [6] [8] [9] .
Патогенез гепатита Е
В цитоплазме гепатоцитов внешняя оболочка вируса вируса раскрывается, и запускается выработка вирусных белков. Одновременно с этим происходит подготовка клетки-хозяина к этому процессу.
Во время своей жизни вирус напрямую провоцирует дегенеративные изменения в гепатоцитах, в т.ч. вызывая их гибель по типу баллонной дистрофии — переполнение клетки жидкостью. После этого готовые вирусные частицы распространяются и заражают новые здоровые клетки.
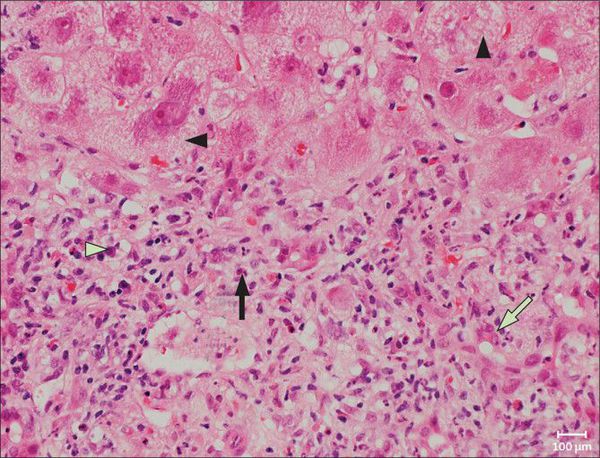
Со временем в организме формируются специфические антитела, которые позволяют полностью вывести вирус из организма человека (за исключением случаев выраженного угнетения иммунитета).
Тяжёлое течение гепатита Е у беременных не связано со свойствами вируса напрямую. Оно вызвано лишь иммунологической перестройкой иммунной защиты беременных. Из-за этого развивается каскад иммунопатологических и гормональных реакций, которые приводят к массированному некрозу гепатоцитов, дефициту плазменных факторов свёртывания и внутрисосудистому гемолизу — разрушению эритроцитов крови [1] [2] [3] [5] [10] .
Классификация и стадии развития гепатита Е
По клиническим признакам выделяют два варианта заболевания:
- безжелтушная форма — до появления симптомов или при освобождении организма от вируса и формировании стойкого иммунитета;
- желтушная форма — при нарастании симптомов.
По тяжести процесса гепатит Е делят на четыре степени:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная, гепатит у беременных).
Факторы риска развития тяжёлого течения болезни:
- беременность любого триместра (наиболее неблагоприятно заболевание протекает в III триместре);
- пожилой возраст:
- мужской пол;
- иммуносупрессивная терапия (на фоне трансплантации органов); ;
- комбинированная соматическая патология (сахарный диабет, ишемическая болезнь сердца, аутоиммунный гепатит, пациенты на гемодиализе);
- наличие хронической вирусной патологии печени (вирусные гепатиты В и С);
- алкоголизм.
По исходу заболевание бывает трёх типов:
- с выздоровлением (полным, с остаточными явлениями);
- с хронизацией;
- с неблагоприятным прогнозом (у беременных) [4][5][6] .
Осложнения гепатита Е
Осложнения при гепатите Е можно разделить на три группы:
- Истинные (печёночные) осложнения:
- острая печёночная недостаточность — осложнение с неблагоприятным исходом, при котором быстро развивается массивное повреждение ткани печени (до 90 %), резкое нарушаются её функции, возникает печёночная энцефалопатия (нарушение работы мозга), геморрагический синдром (повышенная кровоточивость) и коагулопатия (нарушение свёртывания крови);
- холестаз — нарушение синтеза и выведения желчи (желтуха), осветление кала и потемнение мочи, появление выраженного кожного зуда и чувства горечи во рту;
- тромбо-геморрагический синдром у беременных (ДВС-синдром) — кровотечения и кровоизлияния различной интенсивности и направленности;
- преждевременные роды или выкидыш у беременных.
- Внепечёночные осложнения: — острое неврологическое заболевание, которое сопровождается нарушением чувствительности в руках и ногах, мышечной слабостью и иногда параличом.
- острый поперечный миелит — нарушение всех функций спинного мозга;
- различные нейропатии и полирадикулопатии;
- панкреатит — тошнота, рвота, опоясывающие боли в животе; — боли в поясничной области, нарушение мочеобразования, повышенная потеря эритроцитов и белка с мочой;
- повышение вероятности развития рака кожи и заболеваний кровеносной системы.
- Резидуальные (постгепатитные) явления:
- дискинезия (нарушение моторики) желчевыводящих путей — застой желчи, чувство тошноты, отрыжка, горечь во рту;
- постгепатитная гепатомегалия — увеличение печени в связи с разрастанием соединительной ткани;
- постгепатитный синдром — повышенная утомляемость, астения, раздражительность, чувство тошноты и дискомфорта в правом подреберье [1][2][6][7][8] .
Диагностика гепатита Е
Лабораторная диагностика:
- Клинический анализ крови — нормальный объём эритроцитов или умеренная лейкопения, повышение количества лимфоцитов, моноцитов и снижение нейтрофилов в крови, сниженная или нормальная СОЭ.
- Биохимический анализ крови — повышенный уровень общего билирубина за счёт прямой и непрямой фракции, увеличение АЛТ и АСТ, сниженый индекс протромбина (ПТИ), повышение тимол-вероналоовой пробы (уменьшение альбуминов и увеличение гамма-глобулинов), повышение ГГТ и щелочной фосфатазы.
- Общий анализ мочи — появление гематурии, протеинурии и цилиндрурии (обнаружение эритроцитов, белка и цилиндров в моче).
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина.
- Серологические тесты — обнаружение антител в сыворотке крови:
- анти-HЕV IgM — выявляются при острой инфекции с конца первой недели от момента заражения, могут сохраняться до двух лет, иногда бывают ложноположительными при активной ЦМВ-инфекции;
- анти-HЕV IgG — выявляются с 41 дня в течение 15 лет методом иммуноферментного анализа (ИФА);
- HЕV RNA — выявляются при острой инфекции, начиная с 22 дня, а также при хронизации в течение долгого времени благодаря полимеразной цепной реакции (ПЦР).
- УЗИ органов брюшной полости — увеличение печени с реактивным изменением структуры её ткани, увеличение лимфоузлов в воротах печени, иногда увеличена селезёнка.
Дифференциальная диагностика с другими заболеваниями:
- Вирусные гепатиты В и С — связь с парентеральными вмешательствами (например, с переливанием крови), более длительный преджелтушный период, характерные серологические тесты. , желтушная форма — выраженный синдром общей инфекционной интоксикации, увеличение лимфоузлов, тонзиллит, специфические изменения общей крови и серологические тесты.
- Жёлтая лихорадка — острое начало, высокая температура, гиперемия и отёчность лица, временное улучшение, а затем ухудшение состояния. — острое начало, высокая температура, частое поражение почек, выраженные боли в икроножных мышцах, изменения общей крови бактериального характера.
- Псевдотуберкулёз — умеренно высокая температура, мезаденит (воспаление лимфоузлов брыжейки кишечника), терминальный илеит (воспаление подвздошной кишки), симптомы носков и капюшона (мелкоточечные высыпания), скарлатиноподобная сыпь, бактериальные изменения крови, специфические маркеры.
- Острые кишечные инфекции, например, сальмонеллёз — острое начало, выраженный синдром поражения ЖКТ (энтерит, колит, высокая температура).
- Листериоз — высокая температура, увеличение лимфоузлов, поражения железистой ткани ротоглотки, бактериальная кровь.
- Сепсис — гектическая (изнуряющая) лихорадка, выраженные полиорганные нарушения.
- Амебиаз — характерные симптомы поражения кишечника, эозинофилия крови, выявления возбудителя.
- Токсические поражения печени — связь с употреблением токсинов, отсутствие синдрома общей инфекционной интоксикации.
- Опухоли гепатобилиарной области — длительное постепенное начало, отсутствие яркой выраженной симптоматики, умеренное повышение АЛТ или АСТ, резкое повышение СОЭ, характерные изменения на УЗИ, КТ или МРТ. — типичные болевые приступы, умеренное повышение АЛТ или АСТ, данные инструментальных исследований [1][2][6][8][10] .
Лечение гепатита Е
При лёгкой степени гепатита Е лечение проводится в амбулаторных условиях (на дому). Во всех остальных случаях показано стационарное лечение в инфекционном отделении больницы. Режим постельный или полупостельный.
Чтобы снизить нагрузку на поражённую печень, необходимо придерживаться механически и химически щадящей диеты № 5 по Певзнеру. Она подразумевает употребление витаминов и повышенного количества воды (более 1,5 л в сутки), исключение алкогольных и газированных напитков, жаренной и острой пищи, грибов, сдобного теста и других продуктов.
Специфического лечения, которое бы устраняло причины гепатита Е, нет. В основном все методы направлены на устранение симптомов, интоксикации и восстановление нормальной функции печени.
Показан приём сорбентов и препаратов, которые повышают энергетические ресурсы. Иногда назначают гепатопротекторы. Если случай тяжёлый, то проводится терапия гормональными средствами и препаратами крови, а также гипербарическая оксигенация (использование кислорода под высоким давлением) и плазмаферез.
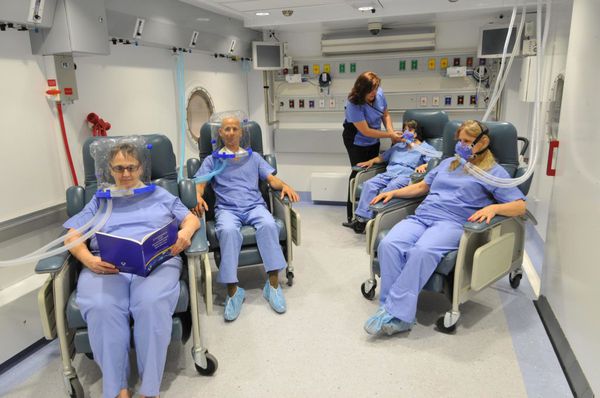
Назначение инфузионной терапии — внутривенного введения глюкозо-солевых растворов и витаминов — зависит от степени тяжести и определённых симптомов.
При тяжёлом течении и хронизации возможно применение препаратов общевирусного действия. Они позволяют снизить вирусную нагрузку.
Людям, получающим цитостатическую (противоопухолевую) терапию по возможности следует снизить дозу на 30 %. Это повышает вероятность спонтанной гибели вируса.
Беременные с гепатитом Е должны находиться в условиях реанимации инфекционного стационара. В острый период болезни лечение проводится по общим принципам, преждевременное родоразрешение противопоказано.
Выписывать больных можно в том случае, если в ходе лечения у них стойко улучшается клиническая картина и лабораторные показатели. После выписки пациенты, которые идут на поправку после неосложнённых форм болезни, находятся под наблюдением врача в течение шести месяцев. Осмотр и обследования проводятся минимум один раз в месяц [5] [6] [8] [9] .
Прогноз. Профилактика
Прогноз гепатита Е зачастую благоприятный, за исключением случаев заболевания при беременности. После выписки из больницы окончательное выздоровление наступает спустя 2-3 месяца. Крайне редко болезнь может стать хронической и затяжной.
Чтобы снизить количество случаев инфицирования, необходимо придерживаться следующих правил:
- создавать все условия для того, чтобы потребляемая питьевая вода была безопасной (касается водоснабжения);
- соблюдать правила утилизации сточных вод (канализационное хозяйство);
- соблюдать правила личной гигиены (всегда мыть руки);
- следить за качеством обследования работников, которые связаны с пищевой промышленностью;
- соблюдать технологию хранения, приготовления и транспортировки продуктов питания и воды;
- беременным на любом сроке стоит воздержаться от поездок в потенциально опасные в эпидемиологическим плане места (тёплые страны, особенно Азиатского региона).

Для предотвращения развития болезни разработана специфическая профилактика — вакцинация против гепатита Е. С этой целью применяется вакцина Hecolin (Китай). Она вырабатывает иммунитет к одному генотипу у 95 % трехкратно привитых людей [1] [2] [3] [5] [8] .
Вирусный гепатит С является одной из главных причин хронических заболеваний печени. Первичная диагностика гепатита С осуществляется путем определения антител к белкам вируса гепатита С (ВГС) в сыворотках с использованием широко представленных на рынке тест-систем для иммуноферментного анализа (ИФА). Положительные результаты, полученные при скрининге сывороток, несут информацию о самом факте инфицирования, однако серологические методы не позволяют разграничить разрешившуюся острую инфекцию от хронического заболевания, а также оценить эффективность антивирусной терапии. В связи с этим для установления диагноза и характеристики активности хронического гепатита наряду с комплексным клиническим обследованием пациентов проводятся вирусологические исследования, направленные на определение прямых маркеров ВГС - РНК и вирусспецифических белков.
Патогенез гепатита С остается во многом неясным. До сих пор не существует однозначного ответа на вопрос, как присутствие вируса в организме влияет на развитие заболевания. Во многом это обусловлено тем, что исследователи этой проблемы получают противоречивые результаты. В этом обзоре мы постарались коротко изложить существующие в настоящее время опубликованные данные и результаты собственных исследований, касающиеся связи между присутствием РНК и белков ВГС в организме больных и активностью хронического гепатита С.
Для изучения распределения РНК вируса гепатита С в различных органах и тканях инфицированного организма применяют методы полимеразной цепной реакции с этапом обратной транскрипции (ОТ-ПЦР), гибридизации in situ, ПЦР in situ. Вирусные белки выявляют либо с помощью поликлональных сывороток, либо с помощью моноклональных антител.
Для оценки влияния вирусной нагрузки на активность хронического гепатита С, которая может варьировать от минимальных гистологических изменений в печени до случаев цирроза и гепатокарциномы, используют различные варианты количественного и полуколичественного методов ОТПЦР. Активность патологического процесса в печени оценивают по уровню активности фермента аланинаминотрансферазы (АЛТ), индексу гистологической активности (ИГА). Стадию заболевания характеризуют, используя гистологический индекс склероза (ГИС). Гистологический диагноз (ИГА и ГИС) ставится на основании морфологического изучения биопсийного материала печени и выражается в баллах в соответствии с международной классификацией (DesmetV.J. et al., 1994).
По данным ряда исследователей, репликация вируса возрастает по мере прогрессирования болезни (Cho S.W. et al., 1996), и более высокий уровень виремии коррелирует с более серьезным повреждением печени (Gretch D. et al., 1994). При исследовании парафиновых срезов печени Dries V. с соавт. (1999) отмечали более частое выявление РНК В ГС в печени пациентов с высоким уровнем воспалительной активности по сравнению со случаями, при которых повреждения печени были минимальны. По мнению авторов, это связано с тем, что вирусная нагрузка клеток печени может определять воспалительно-некротическую реакцию (Dries V. et al., 1999). По данным Jamal M.M. с соавт. (1999), у пациентов с постоянно нормальным уровнем АЛТ наблюдается значительно более низкий уровень РНК ВГС в печени, чем у больных с повышенным уровнем АЛТ. Adinolfi L.E. с соавт. (1998) указывают, что у пациентов с циррозом печени уровень РНК в печени превышает таковой у пациентов с низким уровнем ИГА (1-4). Наиболее высокий уровень РНК ВГС в печени наблюдается у больных с ИГА>8 (Adinolfi L.E.etal., 1998).
В противоположность этому большинство исследователей сходятся на том, что прямая связь между количеством РНК ВГС в организме (как в печени, так и в периферической крови) и степенью активности патологического процесса отсутствует (BallardiniG.etal., 1997, McGuinnesP.H. et al., 1996, Negro F. et al., 1998, 1999, Rodriguez-Inigo E.et al., 1999, Sugano M. et al., 1995). Поданным этих авторов, присутствие вируса в организме и уровень вирусной РНК не коррелируют со значениями ИГА, ГИС или АЛТ. Есть данные об уменьшении уровня вирусной РНК в печени при прогрессировании хронического гепатита С (Di MartinoetaL, 1997).
Результаты, полученные в нашей лаборатории, согласуются с последней концепцией: при исследовании материалов (ткани печени, сыворотки и лимфоцитов периферической крови) от 75 пациентов с хроническим гепатитом С не было обнаружено достоверных отличий между частотой выявления РНК ВГС у больных с различной активностью заболевания (Лакина Е.И. и др., 2000). При проведении нами количественного анализа уровня РНК ВГС в сыворотке крови больных ХГС (Amplicor Monitor Test, v.2.0., "Roche Diagnostics") также не выявлено значимой корреляции между показателями ИГА, ГИС, АЛТ и уровнем виремии.
В настоящее время в литературе активно обсуждается вопрос о роли лимфоцитов в развитии ВГС-инфекции. Результаты выявления РНК ВГС в мононуклеарах периферической крови больных гепатитом С, полученные разными исследователями, варьируют в широких пределах. Так, по данным одних авторов, РНК ВГС в мононуклеарах периферической крови встречается у 24% больных (Young K.S. et al., 1993), по данным других - у всех (100%) обследованных (MellorG. et al., 1998, OkumuraA. et al., 1998). Согласно нашим данным, РНК ВГС в лимфоцитах периферической крови выявляется в 64% случаев. Связи между наличием ВГС в лимфоцитах и активностью гепатита С не обнаружено.
Zignego A.L. с соавт. (1995) показали, что РНК вируса чаще встречается в клетках крови пациентов с более серьезными повреждениями печени. Для объяснения существования этой связи авторы предположили, что активная инфекция различных субпопуляций клеток, вовлеченных в иммунный ответ хозяина, может нарушать их функцию, приводя к персистенции ВГС и развитию хронических повреждений печени. Частое обнаружение РНК ВГС в периферических мононуклеарах больных с хроническими повреждениями печени может объясняться тем, что при длительной ВГС-инфекции клеток печени происходит увеличение пула инфицированных лимфоидных клеток путем передачи от клетки к клетке (Zignego et al., 1995). Показано, что инфицированные лимфоидные клетки могут быть причиной заражения здоровой печени, пересаженной в организм ВГС-инфицированного пациента (Feray С. et al., 1992). Внепеченочный резервуар инфекции может также служить источником реактивации болезни после прекращения интерферонотерапии (Gil В. et al., 1993).
При изучении вопроса о том, насколько уровень вируса в сыворотке отражает его количество в печени, данные исследователей расходятся. Тогда как одни авторы выявляют корреляцию между присутствием геномной РНК в печени и уровнем виремии (De Moliner L. et al., 1998, Mc Guinnes P.H. et al., 1996, Negro F. et al., 1999), другие (Ballardini G. et al., 1997) подобную связь отрицают. Martin с соавт. (1998) указывают на существование корреляции между количеством РНК ВГС в печени и в сыворотке крови, но не в периферических мононуклеарах. В работе Sugano M. с соавт. (1995) сообщается о положительной корреляции между уровнем РНК ВГС в печени и сыворотке крови до лечения интерфероном. После интерферонотерапии корреляция между количеством РНК в печени и в сыворотке не была обнаружена. Подсчет инфицированных клеток в печени после проведения гибридизации in situ показал, что число клеток, содержащих РНК ВГС, может колебаться от 4,8% до 87,6% у разных больных, и уровень виремии прямо зависит от числа инфицированных клеток в печени (Gosalvez J. et al., 1998, Lau G.K.K. et al., 1994, Rodriguez-Inigo E. et al., 1999). При сопоставлении частоты выявления РНК ВГС в печени и в сыворотке крови нами были получены результаты, согласно которым примерно в трети случаев возникает ситуация, когда при наличии вируса в печени РНК ВГС в сыворотке не выявляется: частота выявления РНК ВГС в печени составляет 86%, в сыворотке крови -51%. Эти результаты согласуются с данными других авторов (Haydon G.H. et al.„ 1998, Seidi S. et al., 1999). Например, в работе Haydon G.H. с соавт. (1998) геномная РНК ВГС выявлена в клетках печени 10 из 12 пациентов, негативных по этому показателю в сыворотке.
Жизненный цикл ВГС включает образование репликативных (минус-) цепей РНК, которые служат матрицей для образования геномных молекул. Частота выявления репликативной формы РНК ВГС по данным одних исследователей составляет 35% случаев (Gastaldi M. et al., 1995), тогда как по данным других до 100% (Okabe M. et al., 1997, Sansonno D. et al., 1997, Chang M. et al., 2000). Существенное расхождение данных может объясняться трудностями, возникающими при определении минус-РНК, так как количество негативных цепей РНК на один (lanford R.E. et al., 1995) - три (Mellor J. et al., 1998) порядка ниже, чем +РНК. Это объясняется тем, что одна молекула -РНК может служить матрицей для синтеза нескольких геномных молекул.
Среди исследователей нет единого мнения о том, насколько репликация вируса связана с процессами повреждения печени и выходом вирусных частиц в периферическую кровь (De Moliner L. et al., 1998. Negro F. et al., 1999). По данным Negro F. с соавт. (1998, 1999), использовавших полуколичественный метод PCR, нет строгой связи между вирусной репликацией и уровнем виремии. Согласно полученным нами данным, репликация вируса в печени сопровождается большей частотой выявления РНК ВГС в сыворотке крови, однако достоверной корреляции между этими параметрами не обнаружено. Несоответствие между количеством выявленных геномной и репликативной форм РНК ВГС в печени и уровнем виремии может быть следствием ряда причин: 1 - элиминации вируса из сыворотки с помощью специфических антител; 2 - поступления ВГС в периферическую кровь не только из печени, но и из других органов и тканей; 3 - нарушения процесса высвобождения вируса из клеток печени под действием лекарственных средств или других факторов (Negro F. et al., 1998). Опыты, проведенные в нашей лаборатории, не выявили достоверной корреляции между частотой встречаемости минус-РНК ВГС в печени и степенью поражения печеночной ткани (Лакина Е.И. и др., 2000). Это согласуется с предположением, что вирус может реплицироваться, не вызывая серьезных повреждений в ткани печени (Negro F. et al., 1998). Однако есть данные о возможном участии вирусной репликации в развитии цитопатического эффекта (Chang M. et al., 2000, Tsutsumi M. et al., 1994). С помощью метода гибридизации in situ показано, что клетки, содержащие репликативную форму РНК вируса, локализованы преимущественно в очагах поражения печени (Tsutsumi M. et al., 1994). Обнаружена достоверная корреляция между количеством гепатоцитов, содержащих репликативную форму РНК ВГС, и степенью воспаления печени. Следует отметить, что для геномной РНК ВГС авторы такой связи не выявили (Chang M. et al., 2000).
Согласно мнению большинства исследователей, хотя печень и является главным органом, где происходит вирусная репликация, ВГС может реплицироваться в периферических мононуклеарах, лимфатических узлах, поджелудочной железе, в меньшей степени - в костном мозге, селезенке, щитовидной железе и надпочечниках (Lerat Н. et al., 1996, Okumura A. et al., 1998, Gowans E.J., 2000, Grovatto M. et al., 2000, Radkoowski M. et al., 2000).
Наряду с определением РНК, перспективным методом изучения активности вирусной репродукции является выявление вирусных белков непосредственно в тканях с помощью иммуногистохимических методов (ИГХ). В качестве иммунных реагентов для детекции антигенов ВГС используются как моноклональные антитела (Ballardini G. et al., 1995, Gonzalez-Peralta R.P. et al., 1994, Noun-Aria K.T et al., 1995, Sansonno D. et al., 1995, Nayak N.C., SatharS.A., 1999), так и поликлональные антисыворотки, полученные от экспериментально иммунизированных животных (Gonzalez-Peralta R.P. et al., 1994, Tsutsumi M. et al., 1994) или больных хроническим гепатитом С людей (Ballardini G. et al., 1995, Nouri-Aria K.T. et al., 1995).
Большой интерес представляет вопрос о связи экспрессии вирусных белков с активностью патологических процессов в печени. Согласно большинству исследований, число гепатоцитов, содержащих вирусные антигены, не коррелирует ни со степенью гистологических изменений в печени, ни с показателями биохимической активности (Gonzalez-Peralta R.P. et al., 1994, Nayak N.C., Sathar S.A., 1999, Gowans E.J., 2000). С другой стороны, Hiramatsu N. с соавт. (1992) показали, что экспрессия антигенов ВГС в печени возрастала с увеличением степени поражения органа. Sansonno D., Damacco F. (1993), изучая печень больных острым гепатитом С, обнаружили топографическую связь между очагами воспаления и некроза с одной стороны и гепатоцитами, экспрессирующими антигены ВГС, - с другой. Однако при переходе болезни в хроническое состояние эта связь не обнаруживалась.
Мы изучали распределение антигенов нуклеокапсида, неструктурных белков NS3, NS4A и NS4B с помощью полученных нами МКА в клетках печени больных хроническим гепатитом С на криостатных срезах печени. Были использованы биопсийные материалы от больных с различной активностью гепатита С и на разных стадиях заболевания. Параллельно ткань печени анализировали методом RT-PCR на наличие геномной и репликативной цепей РНК ВГС. В целом, антигены ВГС обнаружены в печени 33 из 34 (97%) пациентов, имеющих геномную РНК в ткани печени. Уровень детекции белка нуклеокапсида составлял 53%, NS3 - 76%, NS4 - 81%. Репликативная форма РНК ВГС значительно чаще ассоциировалась с выявлением соrе-белка. При этом доля антиген-позитивных гепатоцитов варьировала в широких пределах от 1 до 90% у разных пациентов, составляя в среднем около 32%. У больных с ХГС обнаружены качественные и количественные различия в соотношении структурных и неструктурных белков ВГС в клетках печени. В целом, все исследованные белки накапливались в печени пациентов с более тяжелыми формами ХГС (Абдулмеджидова АГ. и др., 2000). Между антиген-содержащими клетками и очагами воспаления и некроза ткани печени топографической связи выявлено не было, что подтверждает ранее полученные данные (Sansonno D., Damacco F., 1993). Эти результаты свидетельствуют в пользу гипотезы об отсутствии прямого цитопатического действия ВГС.
Анализ внутриклеточной локализации вирусных белков методом ИГХ показал, что специфическое окрашивание наблюдается только в цитоплазме гепатоцитов, что согласуется с большинством опубликованных работ (Ballardini G. et al., 1997, Blight К. et al., 1994, Brody R.I. et al., 1998, Gonzalez-Peralta et al., 1994, 1995, Nouri-Aria K.T. et al., 1995, Sansonno D. et al., 1995 (a,b), 1997).
Большой интерес представляет использование моноклональных антител для выявления белка нуклеокапсида ВГС в сыворотках крови больных гепатитом С и доноров (Onto E. et al., 1996, Jolivet-Reynaud С. et al., 1998, Masalova O.V. et al., 1998). Подобные исследования наталкиваются на две основные трудности: низкая концентрация вируса и блокирование антигенов ВГС антителами в составе иммунных комплексов (Onto E. et al., 1996, Shiratori Y. et al., 1997). В нашей лаборатории разработан метод для количественного определения соге-белка, входящего в состав циркулирующих в плазме "свободных" вирионов и иммунных комплексов. При исследовании плазм от 80 антиВГС-позитивных доноров оказалось, что вирусная РНК выявляется только в половине образцов. В 94,4% РНК-позитивных плазм выявлен и белок нуклеокапсида ВГС. Концентрация белка core в разных образцах варьировала в широких пределах и составляла 5-850 пг/мл (Масалова О.В. и др., 2000). В сыворотках пациентов с ХГС (n=71) белок нуклеокапсида был обнаружен у 74% больных. Концентрация соге-белка не коррелировала с тяжестью заболевания Показано, что циркуляция ВГС в виде иммунных комплексов ассоциирована с более продвинутой стадией ХГС (согласно значениям ГИС) (Masalova O.V. et al., 2000). Тест-системы для ИФА на основе моноклональных антител, позволяющие определять белок нуклеокапсида не только на качественном, но и на количественном уровне, являются более простым и дешевым, чем ПЦР, методом выявления ВГС. Их внедрение в практику здравоохранения может существенно обогатить возможности современной диагностики и контроля за течением гепатита С.
Таким образом, несмотря на десятилетнее изучение вопроса о связи между присутствием вируса гепатита С в организме и прогрессированием хронического гепатита, многое по-прежнему остается неясным. Данные о роли вирусного генома и вирусных белков в патогенезе инфекции противоречивы. Необходимы дальнейшие исследования по комплексному анализу обоих компонентов иммунного распознавания: вируса (РНК, структурных и неструктурных белков) и иммунной системы хозяина (антител к ВГС, Т-клеток, цитокинов и иммунных комплексов). Эти знания необходимы для разработки эффективных средств профилактики и специфических препаратов для лечения гепатита С, что позволит контролировать это широко распространенное тяжелое заболевание человека.
* Работа поддержана РФФИ, проект № 01-04-48890
Хронический гепатит С – заболевание печени, вызванное вирусом гепатита С, длительностью 6 и более месяцев. В 10 – 40% случаев хронический гепатит С прогрессирует до цирроза печени, а в 5% случаев до гепатоцеллюлярной карциномы (чаще у пациентов с циррозом или выраженным фиброзом).
Пользователи протокола: гастроэнтерологи, инфекционисты, терапевты, врачи общей практики, а также врачи смежных специальностей, осуществляющие ведение и лечение пациентов с гепатитом С на разных стадиях заболевания.
Методология: Протокол разработан на основе Клинических руководств ведущих международных сообществ (EASL, AASLD, CASL, SASL, FASL, EACS, РОПИП) и адаптирован с учетом используемых на территории Казахстана методов диагностики и лечения. Классификация рекомендаций, использованная в данном протоколе, представлена в Таблице 1.
Таблица 1. Классификация рекомендаций
Классификация
Клиническая классификация
Общепринятой классификации ХГС не существует. При постановке диагноза необходимо указывать вирусологический статус (генотип и вирусную нагрузку), активность (биохимическую и/или гистологическую), а также стадию заболевания (по данным непрямой эластографии или морфологического исследования).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
(+) исследования необходимые для пациентов с ЦП
Хронический гепатит С протекает бессимптомно или малосимптомно и может сопровождаться такими неспецифичными симптомами как:
• Депрессия (оценивается у всех пациентов с использованием шкалы Бека)
• сахарный диабет 2 типа
При сборе анамнеза следует учитывать указания на гемотрансфузии, трансплантацию органов и тканей, небезопасные инвазивные (немедицинские) манипуляции, принадлежность в группам риска (потребители наркотиков, лица с беспорядочными половыми связями, пациенты, находящиеся на хроническом гемодиализе, пациенты с онкогематологическими заболеваниями, лица, живущие с ВИЧ и другими парентеральными инфекциями, сексуальные партнеры лиц с ВГС, медицинские работники, дети, рожденные от HCV-инфицированных матерей, лица с измененными функциональными пробами печени). Лицам с указанными факторами риска необходим профилактический скрининг на наличие ВГС (anti-HCV).
При физикальном обследовании на начальной стадии ХГС патологии не выявляется, за исключением незначительной гепатомегалии. По мере прогрессирования заболевания может отмечаться увеличение и уплотнение печени. Спленомегалия и другие стигмы хронического заболевания печени могут проявляться на более поздних стадиях.
Вирусный гепатит С преимущественно протекает бессимптомно. При переходе хронического гепатита С в цирроз в 6,4% случаев отмечаются симптомы, обусловленные дисфункцией печени и портальной гипертензией:
В ряде случаев ВГС выявляется у пациентов с ГЦК, которая, как правило, протекает бессимптомно, кроме случаев запущенной стадии, когда опухоль достигает значительных размеров, вызывая ухудшение функции печени (желтуха, асцит, печеночная энцефалопатия), боли в верхнем правом квадранте, астенизацию и потерю веса.
ОАК с подсчетом тромбоцитов. Могут быть выявлены анемия (в результате гиперспленизма, кровотечений из ВРВ), лейкопения, тромбоцитопения (в результате гиперспленизма и прямого миелодепрессивного влияния ВГС), ускорение СОЭ (при инфекционных осложнениях).
Биохимический профиль включает определение показателей АЛТ, АСТ, ГГТП, альбумина, билирубина, щелочной фосфатазы, МНО или ПВ, а также рутинных (глюкозы, креатинина, холестерина) и некоторых специфических показателей, таких как, гамма-глобулины, IgG (скрининг аутоиммунного гепатита), сывороточное железо и ферритин (скрининг гемохроматоза и вторичной перегрузки железом), церулоплазмин (скрининг болезни Вильсона-Коновалова), АФП (скрининг ГЦК). Активность АЛТ и АСТ может быть минимальной ( < ВГН), слабовыраженной (< 5 ВГН), умеренной (5-10 ВГН), выраженной (>10 ВГН) и не всегда коррелирует с гистологической активностью. Уровень билирубина при ХГС, как правило, нормальный. Его увеличение может наблюдаться при остром гепатите или свидетельствовать об ухудшении деятельности печени на поздней стадии заболевания, что также сопровождается снижением уровня альбумина и увеличением МНО или ПВ. Показатели щелочной фосфатазы и ГГТП могут увеличиваться при остром гепатите и оставаться на уровне нормы при хроническом гепатите.
В план клинического лабораторного обследования включаются также ОАМ, копрограмма.
- anti-HCV, маркеры других парентеральных инфекций таких как ВГВ (HBsAg, HBeAg, anti-HBs, anti-HBe, anti-HBc total/IgM), ВГD (anti-HDV у носителей HBsAg), ВИЧ (anti-HIV), а также (при подозрении на острый гепатит) ВГА (anti-HAV) и ВГЕ (anti-HEV)
Качественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа.
• В случае подозрения на острый ВГС или у иммуносупрессивных пациентов необходимо определение HCV RNA (рекомендация А1)
• Если тест на anti-HCV положительный, необходимо определить HCV RNA, чувствительным молекулярным методом (рекомендация А1)
• Пациенты с положительным тестом anti-HCV и отрицательным молекулярным тестом на HCV RNA должны быть протестированы на HCV RNA через 3 месяца для подтверждения элиминации вируса (рекомендация А1).
− ИФА (+) в 50% в момент острых проявлений, поэтому ПЦР при подозрении на ОГС проводится во всех, в том числе, ИФА (–) случаях
Количественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа, а также определение генотипа ВГС.
В настоящий момент известно 6 различных типов вируса, которые обозначаются цифрами от 1 до 6. Также существует подтипы, обозначаемые буквами (например, подтип 1а и 1b). На территории РК преимущественно распространенны генотипы 1b, 2 и 3.
Функциональные пробы щитовидной железы (ТТГ)
Тест на беременность
Определение полиморфизма гена интерлейкина – 28В. Результат анализа полиморфизма в гене ИЛ28В полезен в прогнозе эффективности лечения и принятии решения о выборе режима терапии у пациентов с ВГС 1 генотипа. 1
Инструментальные исследования
Радиологическое исследование
Радиологическое исследование печени (в первую очередь УЗИ) позволяет идентифицировать признаки стеатоза, выраженного фиброза и перехода в цирроз печени (закругление контуров печени, неравномерность поверхности и крупнозернистость паренхимы печени), признаки портальной гипертензии и тромбоза (увеличение диаметра, кавернозная трансформация, наличие тромбов воротной и селезеночной вен, асцит, спленомегалия), а также наличие объемных образований (ГЦК). Могут использоваться и другие визуализирующие технологии (КТ, МРТ).
Эндоскопическое исследование
При прогрессировании хронического гепатита С в цирроз диагностика портальной гипертензии может, помимо прочих методов, осуществляться путем эндоскопического обследования, позволяющего выявить варикозное расширение вен (пищевода и желудка) и портальную гастропатию.
Оценка тяжести заболевания печени должна проводиться до ПВТ. Выявление пациентов с циррозом печени имеет особое значение, так как эффективность ПВТ обратно пропорциональна стадии фиброза. Отсутствие выраженного фиброза имеет значение при принятии решения о времени начала ПВТ. Пациенты с явными клиническими признаками цирроза не нуждаются в биопсии печени для оценки стадии фиброза. Пациенты с признаками цирроза печени должны быть обследованы на ГЦК. Выраженный фиброз может быть у пациентов с нормальной активностью АЛТ, поэтому оценка степени тяжести заболевания должна проводиться независимо от показателей АЛТ. Пункционная биопсия остается эталонным методом оценки стадии фиброза печени. Риск тяжелых осложнений при биопсии очень низок (от 1/4000 до 1/10000). У пациентов с нарушением свертываемости крови можно использовать трансюгулярную биопсию печени с одновременной оценкой давления в портальной вене. При ХГС альтернативные, неинвазивные методы (непрямая эластография и биомаркеры) могут быть использованы вместо биопсии. Непрямая эластография может быть использована для оценки стадии фиброза печени у пациентов с ХГС, но необходимо учитывать факторы, которые могут повлиять на достоверность результатов, например выраженная активность заболевания, ожирение. Оба метода (непрямая эластография и биомаркеры) точны при оценке цирроза и нулевого фиброза, но менее точны при промежуточных стадиях фиброза. Комбинирование биомаркеров и непрямой эластографии повышает точность оценки стадии фиброза и уменьшает необходимость в проведении ункционной биопсии. В случае противоречивых результатов биомаркеров и непрямой эластографии, можно использовать пункционную биопсию печени. Гистологическая оценка также необходима при смешанной этиологии (например, ВГС с ВГВ, метаболическим синдромом, алкоголизмом или аутоиммунными заболеваниями).
Пункционная биопсия печени (ПБП) – относительно безопасный метод оценки морфологических изменений печени у пациентов с ХГС. ПБП позволяет оценить выраженность фибротического процесса и некровоспалительных изменений. Результаты ПБП легко интерпретируются и поддаются полуколичественной оценке. ПБП проводится в динамике с целью оценки прогрессирования поражения печени при ХГС. ПБП – единственный доступный метод, позволяющий оценить вклад сопутствующих заболеваний (стеатогепатит, гемохроматоз, аутоиммунный гепатит и т.д.) в патологическом процессе и их влияние на течение и эффективность лечения ХГС. Необходимо помнить, что ПБП имеет ряд ограничений. В частности, имеет значение опыт врача, проводящего пункцию, и морфолога, оценивающего морфологические изменения; малый объем образцов ткани печени; инвазивность и дискомфорт для пациентов; риск развития осложнений. ПБП требует строгого выполнения правил ее выполнения в условиях специализированных отделений и наличия квалифицированных морфологов.
2. Всем пациентам перед выполнением биопсии печени должно быть выполнено УЗИ ОБП. Данное исследование позволяет выявить анатомический вариант строения печени и наличие очаговых образований в ее паренхиме, что может потребовать проведения прицельной биопсии под визуальным контролем.
3. В течение недели перед проведением пункции необходимо определить количество тромбоцитов и протромбиновое время (ПВ), либо протромбиновый индекс (ПИ)
• Если количество тромбоцитов ≥90 000 /мм3, то манипуляцию можно выполнять рутинным способом (чрескожная биопсия печени)
• Если ПВ удлинено менее чем на 3 сек. в сравнении с контрольным значением (предоставляется лабораторией, в которой выполняется исследование образца крови), ПИ не менее 70%, тромбиновое время (ТВ) и активированное частичное тромбопластиновое время (АЧТВ) не превышают 1,5 нормы, биопсию можно проводить чрескожным доступом
• Во всех других случаях решение о выполнении биопсии печени принимается на индивидуальной основе путем оценки пользы и риска от планируемой манипуляции. В случае строгой необходимости в проведении биопсии печени у пациентов с гипокоагуляцией или низким количеством тромбоцитов в некоторых случаях может быть оправдана заместительная терапия
4. Перед биопсией необходимо подписать у пациента информированное согласие, в котором доступно описана методика манипуляции и возможные осложнения.
5. Во время выполнения биопсии врач и пациент должны быть в постоянном контакте. Больной четко и своевременно должен выполнять команды врача. При повышенной возбудимости пациента и отсутствии признаков печеночной недостаточности возможно назначение седативных препаратов.
6. Выбор иглы для биопсии целесообразно осуществлять с учетом личного опыта оператора. В повседневной практике удобны в применении иглы Менгини и иглы типа Tru-cut.
7. Врачи, личный опыт которых не превышает 20 манипуляций, выполняют биопсию в присутствии и под контролем более опытного доктора в условиях специализированного гепатологического центра.
9. Активное наблюдение пациентов в течение 8 часов и первой ночи после манипуляции должно проводиться в условиях медицинской организации. Оценка результатов ПБП проводится с применением полуколичественных шкал описания степени некро-воспалительных изменений и стадии фиброза ткани печени (см. Таблицы 3 и 4).
Таблица 3. Морфологическая диагностика степени некровоспалительной активности гепатита
*Для определения стадии заболевания печени чаще применяется шкала METAVIR
К преимуществам метода относятся:
• Неинвазивность
• Воспроизводимость
• Больший чем при биопсии оцениваемый объем ткани печени (в 100-200 раз больше)
• Быстрота и удобство применения (обследование занимает в среднем 5 мин)
• Немедленный результат
• Оценка эффективности терапии
• Возможность обследования детей
• Высокой биохимической активности (АЛТ/АСТ выше верхнего лимита нормы в 3 и более раз)
• Не менее 60% успешных измерений.
Таблица 5. Интерпретация результатов непрямой эластографии
Читайте также:

