Как отличить папиллому от контагиозного моллюска
Обновлено: 25.04.2024
Кафедра акушерства и гинекологии Казанской государственной медицинской академии
Кафедра акушерства и гинекологии Казанской государственной медицинской академии
2ООО "Био Фарма", Москва
Институт химической физики им. Н.Н. Семенова РАН, Москва
Институт химической физики им. Н.Н. Семенова РАН, Москва
Генитальные кондиломы у женщин: факты и противоречия
Журнал: Российский вестник акушера-гинеколога. 2012;12(2): 78‑80
Мальцева Л.И., Фаррахова Л.Н., Кучеров В.А., Стовбун С.В., Сафронов Д.Ю. Генитальные кондиломы у женщин: факты и противоречия. Российский вестник акушера-гинеколога. 2012;12(2):78‑80.
Mal'tseva LI, Farrakhova LN, Kucherov VA, Stovbun SV, Safronov DIu. Genital condylomas in women: facts and contradictions. Russian Bulletin of Obstetrician-Gynecologist. 2012;12(2):78‑80. (In Russ.).
Кафедра акушерства и гинекологии Казанской государственной медицинской академии
Кафедра акушерства и гинекологии Казанской государственной медицинской академии
Кафедра акушерства и гинекологии Казанской государственной медицинской академии
2ООО "Био Фарма", Москва
Институт химической физики им. Н.Н. Семенова РАН, Москва
Институт химической физики им. Н.Н. Семенова РАН, Москва
Диагностика ОК несложна, генитальные бородавки хорошо определяются визуально и при осмотре кольпоскопом. Локализуются кондиломы на шейке матки, стенках влагалища, промежности, перианальной области, нередко поражается и наружное отверстие уретры, клитор. Кольпоскопически кондиломы могут выглядеть как остроконечные разрастания, иметь закругленную папуловидную форму или напоминать папиллярные образования. Размеры разрастаний различны - от мелких единичных до массивных, перекрывающих вход и полость влагалища. Биопсию кондилом проводят при неясном диагнозе, признаках атипии, окрашивании бородавок, повышенной их плотности и фиксации на подлежащих тканях, кровоточивости или изьязвлении.
Клиническая симптоматика не всегда зависит от степени поражения. Нередки ситуации, когда при наличии единичных ОК беспокоят зуд, жжение во влагалище, постоянные неприятные ощущения или дискомфорт при половом контакте, и даже болезненность, тогда как обширные поражения не вызывают никаких жалоб. Если ОК очевидны, тест на ВПЧ не рекомендуется, потому что это не приведет к изменению тактики лечения.
Дифференцировать генитальные кондиломы следует с контагиозным моллюском, плоскоклеточной папилломой, широкой кондиломой, фиброэпителиальным полипом, значительно реже - с дерматитом и псориазом.
Контагиозный моллюск вызывается ДНК-содержащим покс-вирусом. Типичными для этого заболевания являются единичные или сгруппированные мелкие, гладкие папулы 3-6 мм в диаметре с точечным вдавлением в центре. Высыпания между собой, даже если они множественные, никогда не склеиваются, хотя и могут образовывать бляшкоподобные очаги.
Плоскоклеточная папиллома - множественное папиллярное образование, располагающееся в преддверии влагалища ниже кольца девственной плевы. Иногда папилломы локализуются на медиальной поверхности малых половых губ. Папилломы покрыты многослойным плоским эпителием и нередко являются случайной находкой при отсутствии жалоб. Связь их с ВПЧ не доказана, происхождение неясно.
Фиброэпителиальный полип - доброкачественное папилломатозное образование без сосудистой атипии, гистологически имеет характерные для полипа признаки.
Широкие кондиломы при сифилисе - плоские плотные на широком основании розово-красного цвета образования.
При подозрении на дерматит, псориаз и в неясных случаях необходима консультация дерматолога. Следует помнить о раке вульвы и влагалища, где лишь комплексная оценка позволит избежать ошибки.
Существует два подхода к лечению остроконечных кондилом: традиционный - полная ликвидация всех поражений или удаление кондилом как косметического неудобства. В отношении мужчин-носителей ВПЧ без клинических проявлений единого мнения нет. В настоящее время профилактическое лечение мужчин не принято, так как нет достоверных данных о его эффективности. Известно спонтанное выздоровление - обратное развитие остроконечных кондилом у 29-39% больных. Нередко спонтанно излечиваются дети, у которых появление кондилом в возрасте 2-3 лет связано с интранатальным инфицированием. Эффективность различных методов лечения ОК даже с учетом повторных курсов составляет 60-80%. Рецидивы в 25-50% случаев наступают в течение первых 3 мес после лечения и чаще всего обусловлены реактивацией вируса [5]. Деструктивные физические методы лечения являются наиболее популярными, и первым выбором способа может быть электроэксцизия, лазерная вапоризация, криохирургия, радиоволновое иссечение или фотодинамическая терапия. Электроэксцизия освобождает от вирусов в радиусе 20 мм от центра поражения. Консервативное лечение небольших поражений проводится подофиллином, трихлоруксусной кислотой или солкодермом. В англоязычных странах используется 5% крем имиквимод (Аldara) или 15% мазь синекатехина, лечение проводят в течение 16 нед. В настоящее время нет доказательств того, что иньекции интерферона локально приводят к регрессии или уменьшению частоты рецидивов остроконечных кондилом.
Материал и методы
На первом этапе лечения проводилась санация сопутствующей инфекции в соответствии с выявленным возбудителем, после чего - противовирусная терапия панавиром у 140 женщин (1-я группа). Группами сравнения явились 165 женщин (2-я группа), получивших только электроэксцизию кондилом и 92 больные (3-я группа), у которых электроэксцизия была дополнена применением α-интерферона в свечах вагинально в течение 2 нед после операции.
Схема лечения панавиром 1-й группы состояла в использовании комбинации двух форм препарата: свечей ректально (по 1 свече через день, N10) и геля вагинально 2 раза в день в течение 14 дней. После противовирусной терапии проводили удаление кондилом путем электроэксцизии.
Результаты и обсуждение

Результаты оценивали по частоте рецидивов, элиминации вирусов и регрессу жалоб (см. таблицу).
Использование электроэксцизии и α-интерферона в послеоперационном периоде привело к элиминации вирусов у 76,2% женщин. Высокоонкогенные типы вируса, выявленные у 2 женщин этой группы, сохранились после лечения. Продолжали беспокоить такие симптомы, как бели (у 16 женщин) и сохранился зуд во влагалище (у 12). Следует подчеркнуть, что предложенная нами схема лечения панавиром несколько отличается от рекомендуемой фирмой-изготовителем, однако чисто эмпирически такой вариант был принят как оптимальный. Только местное применение геля панавира в сочетании с деструктивными методами по эффективности равно использованию комбинации α-интерферона и метода деструкции, тогда как комбинация довольно продолжительного системного лечения панавиром (свечи ректально) и местной терапии (гель вагинально) в сочетании с деструкцией кондилом дает хороший стойкий эффект.
Стоимость лечения генитальных кондилом высока во всем мире. Рецидивы заболевания, повторные курсы терапии и при этом недостаточная эффективность приводят к удорожанию лечения настолько, что его можно сравнивать с лечением СПИДа. Применение панавира в предложенном варианте - это однократные затраты, но высокая эффективность, составляющая, по нашим данным, 99,3% при 6-месячном наблюдении и 92,5% - при 2-летнем. Способность препарата оказывать иммуномодулирующее, доказанное в многочисленных исследованиях, и противовирусное действие при различных заболеваниях обнадеживает при лечении инфекции, вызванной не только низкоонкогенными типами ВПЧ, но и высокоонкогенными, что может способствовать профилактике рака шейки матки.
Выводы
1. Предложенная схема лечения пациенток с генитальными кондиломами комбинацией довольно продолжительного системного и местного применения панавира в сочетании с последующей электроэксцезией кондилом дает хороший и стойкий эффект.
2. Способность панавира оказывать иммуномодулирующее и противовирусное действие обнадеживает при лечении инфекции, вызванной не только низкоонкогенными, но и высокоонкогенными типами ВПЧ.
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
ГБУЗ "Клинический кожно-венерологический диспансер" Министерства здравоохранения Краснодарского края, Краснодар
Контагиозный моллюск: старая проблема — новые решения
Журнал: Клиническая дерматология и венерология. 2017;16(3): 76‑81
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
В работе освещены основные особенности эпидемиологии и иммунологии, современного течения контагиозного моллюска; представлен сравнительный анализ эффективности и безопасности существующих методов лечения данного заболевания в разные возрастные периоды. Авторами сделан вывод об эффективности и хорошей переносимости 5% раствора гидроксида калия (Молютрекс) при лечении контагиозного моллюска у детей, в том числе у пациентов с атопическим дерматитом.
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения, Москва
ГБУЗ "Клинический кожно-венерологический диспансер" Министерства здравоохранения Краснодарского края, Краснодар
Вирусные инфекции кожи — распространенные заболевания в практике дерматолога. Инфекции наиболее часто вызваны герпесвирусами, вирусами папилломы человека и контагиозного моллюска (ВКМ). Среди вирусных инфекций особое место занимает заболеваемость контагиозным моллюском (КМ) в связи с высокой распространенностью в детском возрасте. Так, по данным S. Seo [1, 2], инфицированность детей школьного возраста ВКМ составляет 2—8%. По данным K. Kyriakis [3], общая относительная заболеваемость среди 162 детей амбулаторного приема составляет 3,2%, при этом основную часть составляют дети в возрасте от 3 до 5 лет.
Дерматотропный поксвирус представляет собой крупный (200—300 нм), прямоугольный, двуспиральный ДНК-вирус, который размножается в цитоплазме инфицированных эпителиальных клеток. По меньшей мере, насчитывают четыре генотипа (MCV 1—4), самым распространенным из которых во всем мире является 1-й тип. Причем у детей КМ, как правило, провоцируется ортопоксвирусом 1-го типа (MCV-1), а у взрослых — вирусом 2-го типа (MCV-2). Подобная ситуация обусловлена тем, что вирус 1-го типа передается в основном контактным и опосредованным путем, через общие предметы, а вирус 2-го типа — через половые контакты. Однако все типы вируса вызывают одинаковые клинические проявления [4—6]. Есть несколько заслуживающих особого внимания характеристик ВКМ, которые делают его уникальным по сравнению с хорошо изученными представителями рода ортопоксвирусов. Во-первых, ВКМ вызывает хроническую инфекцию с минимальными проявлениями или без признаков воспаления. В отличие от него вирус оспы обезьян и вирус ветряной оспы вызывают острые заболевания, которые имеют значительно более высокие показатели заболеваемости и смертности по сравнению с КМ. Во-вторых, ВКМ поражает и персистирует только в кератиноцитах, в то время как вирусы различных типов оспы поражают другие виды клеток и тканей. В-третьих, молекулы, кодируемые ВКМ, отличны от тех, которые кодируются членами рода ортопоксвирусов. Эта разница в продуцируемых ими молекулах, вероятно, отражает различие тропизма к тканям этих вирусов и фенотипическую разновидность болезней, которые они вызывают. ВКМ — единственный вирус в отличие от вирусов различных видов оспы, который является патогенным исключительно для человека. В связи с победой над вирусом натуральной оспы, прививка от этого заболевания была ликвидирована из прививочного календаря вакцинации; таким образом, ВКМ остается единственным циркулирующим поксвирусом, заражающим людей по всему миру. Вместе с тем ВКМ имеет присущие поксвирусам свойства, проявляющиеся в высокой контагиозности и патогенности [7].
Так, A. Kawahar и M. Yoshida [8] обнаружили ДНК ВКМ с помощью полимеразной цепной реакции (ПЦР) в образцах кожи без высыпаний у 17 из 20 исследуемых пациентов, что говорит о передаче вируса с инфицированных очагов видимо непораженной кожи. Также возможно инфицирование через одежду, полотенца, игрушки, которых касается пациент. У 10 пациентов была обнаружена ДНК вируса в коже пальцев обеих кистей. Также результаты исследований подтвердили непрямой путь передачи через другие предметы: вирусная ДНК была обнаружена на письменном столе, шкафу, ящике с игрушками и кране, который находился в общем пользовании у детей в школе.
Общеизвестно, что ВКМ адаптировался с точки зрения роста и устойчивости к местным иммунным системам в коже человека. Он поражает только кожу и реже слизистые оболочки [9].
Клиническая картина данного заболевания описана почти 200 лет назад, проведено множество клинических и фундаментальных исследований, оценено негативное влияние на качество жизни пациента. КМ — это вирусная инфекция с доброкачественным течением, характеризующаяся образованием восковидных папул телесного цвета, куполообразной формы, в среднем 3—5 мм в диаметре [10].
Папулы содержат воскообразный материал, который состоит из клеточного детрита и многочисленных частиц вируса. Элементы К.М. обычно располагаются группами в одном или двух кожных регионах, но также они встречаются и в рассеянном виде, редко поражаются ладони и подошвы, слизистые оболочки, например, губ, щек, конъюнктивы. Заболевание может развиться в любом возрасте, но в большинстве случаев у детей и молодых взрослых. У большинства иммунокомпетентных пациентов обычно обнаруживают меньше 20 папул, но у некоторых их может быть до нескольких сотен. Поражения, как правило, бессимптомны, но иногда они вызывают зуд, вокруг них может развиться воспалительная реакция [11].
Нарушение кожного барьера может объяснить рост распространенности и большого количества высыпаний у больных с атопическим дерматитом [12, 13]. У пациентов с атопическим дерматитом, в связи сухостью кожи и нарушением эпидермального барьера, часто встречаются диссеминированные формы заболевания [14]. Применение топических кортикостероидов и ингибиторов кальциневрина в связи с их иммуносупрессивным действием является одним из провоцирующих факторов в развитии заболевания у больных атопическим дерматитом [15].
Явление воспаления вокруг очагов поражения служит результатом реакции хозяина в ответ на вирус. Однако связанный с ними зуд может также способствовать распространению и внедрению вирусов через поврежденную кожу. Ограниченный дерматит вокруг папул, как правило, регрессирует спонтанно.
Постановка диагноза при данном заболевании обычно не вызывает трудностей, устанавливается клинически и не требует специальных методов диагностики. При гистологическом исследовании определяется вирусная акантома, а в цитоплазме кератиноцитов — эозинофильные тельца-включения (тельца Гендерсона—Патерсона) [14]. Заболевание характеризуется доброкачественным течением, высокой контагиозностью и ограниченной продолжительностью течения [16—18]. У некоторых пациентов происходит спонтанная инволюция в течение 6—9 мес, однако зачастую поражения могут сохраняться годами [16]. Пораженные участки имеют неэстетичный вид, вызывают обостренное восприятие высыпаний окружающими и родителями ребенка [18].
Заживление происходит, как правило, без возникновения рубцов. В подавляющем большинстве случаев заболевание поражает детей школьного возраста до 12 лет [17]. Особенно это относится к южным регионам, в которых до 10% школьников страдают КМ, причем в качестве факторов, способствующих заболеванию, могут рассматриваться тесный физический контакт, плотно прилегающая одежда и плохая гигиена [18].
Несмотря на многочисленные возможности лечения, специфическая противовирусная терапия КМ до сих пор отсутствует. Один из самых распространенных методов лечения — удаление моллюсков с помощью кюретки или пинцета [19], но при значительной диссеминации моллюсков и их неблагоприятной локализации (например, на лице, шее или генитальной области), а также в случае малого возраста ребенка, возникают большие трудности в применении этого метода. Благодаря чрезкожной анестезии с помощью лидокаин-прилокаиновой мази [19], нанесенной за 30—60 мин до операции, безболезненное удаление моллюсков иногда возможно, однако во многих случаях, а особенно если ребенок неспокоен, обойтись без седации или общего наркоза не удается. Предварительное ожиривание кожного покрова мазью перед удалением моллюсков также значительно затрудняет механические манипуляции, поскольку бранши пинцета соскальзывают с элементов моллюска, что затрудняет техническое выполнение задачи.
Криотерапия жидким азотом хотя и менее болезненный метод, но требует больше времени, чем удаление моллюсков с помощью кюретки или пинцета, и редко позволяет достичь эффекта за одну аппликацию — необходимо проведение нескольких процедур [20].
Применяемые иногда импульсные углекислотные лазеры [21], а также электрокоагуляторы не обладают явными преимуществами с точки зрения практичности и переносимости. При наличии рекомендованных консервативных методов терапии имеются многочисленные альтернативные методы, из которых каждый по себе требует высокой степени лояльности, а также терпения со стороны родителей лечащегося ребенка.
Последний обзор Cochrane по лечению КМ опубликован в 2009 г. В нем рассмотрены 11 рандомизированных контролируемых исследований с 495 участниками [22]. В обзор не вошли пациенты с ИППП и ВИЧ. Мало доказательств эффективности следующих препаратов: нитрит натрия в сочетании с салициловой кислотой по сравнению с салициловой кислотой, масло австралийского лимонного мирта по сравнению с оливковым маслом, и крем бензоила пероксида по сравнению с кремом третиноин [22]. Большинство из широко используемых процедур (например, кюретаж) были исключены из обзора Cochrane. Из него было исключено проспективное рандомизированное исследование Hanna, поскольку его результаты показывали крайне небольшую частоту улучшения после нескольких посещений и не давали информацию о том, когда произошло посещение [23]. В обзоре Cochrane были опубликованы три рандомизированных исследования, а одно все еще продолжается [24]. Результаты испытаний показали отсутствие существенной разницы между аблационной и иммуномодулирующей терапией, а также химическими методами.
Салициловая кислота в виде пластыря [25] или ретиноевая кислота (третиноин) [26] иногда успешно применяются, однако могут привести к значительной ирритации участков кожи, расположенных по периферии очага поражения. Кроме того, эти средства недоступны в России.
Эффективность топической аппликации иммунного модулятора имиквимода недостаточно изучена, препарат не разрешен к применению у детей, недостаточно изучен вопрос о необходимой длительности лечения, а стоимость терапии является крайне высокой [27].
N. Al-Mutairi и соавт. [28] в 16-недельном исследовании с участием 37 пациентов показали, что нет существенных отличий между криотерапией и аппликациями 5% крема имиквимод (34 из 37, или 92%). S. Seo и соавт. [29] сравнили эффект 10% раствора гидроксида калия с таковым у 5% крема имиквимода; обе процедуры были эффективны (57 и 77% соответственно), однако авторы наблюдали высокую частоту местных побочных эффектов, связанных с раздражающим действием 10% раствора гидроксида калия.
Дальнейшие консервативные методы терапии, применяемые с разным успехом, включают топическую аппликацию подофиллотоксина [30], применение кантаридина [31], трихлоруксусной кислоты, фенола, нитрата серебра [31] или йода [25]. Следует предположить, что некоторые из применяемых химических веществ путем поражения эпидермиса и обусловленной этим индукции иммунного ответа вызывают уничтожение вируса [32].
В настоящий момент имеется множество доказательств того, что для лечения КМ в детском возрасте пригоден гидроксид калия. Так, R. Romiti и соавт. [34] описывали топическую аппликацию 10% раствора гидроксида калия, который используют для изготовления микологических нативных препаратов, для лечения у детей инфекции КМ. В то же время та же самая рабочая группа показала, что благодаря применению 5% раствора гидроксида калия, также наносимого 2 раза в день, у 20 детей с КМ были достигнуты сравнимые показатели эффективности лечения (в среднем в течение 6 нед) при значительно уменьшенном профиле побочных явлений [32, 35].
B. Mahajan и соавт. [36] сообщают о применении 20% раствора гидроксида калия при лечении 27 детей в возрасте от 8 мес до 14 лет.
D. Hinostroza-Da-Conceicao и соавт. [37] изучали эффект воздействия 15% раствора гидроксида калия, наносимого каждый вечер, на 46 пациентов различного возраста.
В Англии K. Short и соавт. недавно представили первое двойное слепое плацебо-контролируемое исследование по применению 10% раствора гидроксида калия у детей в возрасте от 2 до 12 лет [32].
Однако во всех выше описанных исследованиях наблюдали довольно высокую частоту побочных эффектов в виде жжения, изъязвления элементов, появления пигментаций и рубцов.
F. Neri и соавт. [38] попытались снизить частоту побочных эффектов и провели испытание 5% раствора гидроксида калия. Во время лечения чувство жжения отсутствовало или было минимальным, ни в одном случае не наблюдалось нарушений пигментации в конце данного исследования. Главный вывод, который был сделан в результате данного исследования, что 5% водный раствор гидроксида калия оказался таким же эффективным, как и 10% раствор гидроксида калия, но вызывал меньшее раздражение. Данное исследование также подчеркивает эффективность применения 5% гидроксида калия в лечении КМ, защищая детей от более агрессивных физических методов лечения [32].
В исследовании эффективности и безопасности 5% гидроксида калия T. Jansen и соавт. [39] принял участие 21 ребенок, при этом у 14 пациентов отмечался атопический дерматит, а у 3 пациентов была атопическая экзема. Наиболее распространенным побочным эффектом, наблюдаемым у 76,2% пациентов, было временное небольшое жжение непосредственно после наружного применения. У 2 пациентов развилась поствоспалительная гиперпигментация, разрешившаяся через 1—3 мес [32].
В настоящий момент существует множество различных методов терапии КМ, такие как кюретаж, механическое удаление, электрокоагуляция или криотерапия, аппликации салициловой кислоты и третиноина, которые часто бывают болезненными и вызывают достаточно большое количество побочных эффектов в виде воспалительной реакции, образования рубцов и гиперпигментации.
Применение стабилизированного 5% раствора гидроксида калия хорошо изучено в многочисленных исследованиях, его эффективность не уступает гидроксиду калия в более высоких концентрациях, но при этом 5% раствор не вызывает побочные эффекты при правильном применении.
Данный 5% раствор гидроксида калия следует аккуратно наносить c помощью кисточки или тонкого аппликатора (входит в комплект) утром и вечером только на элементы КМ, избегая при этом попадания на здоровую кожу. Средство не следует смывать — оно должно высохнуть. Рекомендовано наносить 5% раствор гидроксида калия до возникновения покраснения (воспаления) папул КМ, после чего применение раствора следует прекратить (обычно покраснение возникает в период от 2 до 10 дней использования). Покрасневшие элементы свидетельствуют о том, что образования КМ в ближайшем будущем исчезнут приблизительно в течение 2—6 нед после покраснения. Нельзя применять 5% раствор гидроксида калия более 14 дней, наносить на воспаленные элементы КМ и на другие образования кожи (бородавки, папилломы и т. д.).
Выводы
Таким образом, данные многочисленных клинических исследований подтверждают высокую эффективность и хорошую переносимость стабилизированного 5% раствора гидроксида калия (Молютрекс) при лечении детей, страдающих КМ, в том числе у пациентов с атопическим дерматитом. Легкость применения, безопасность, а также фармакоэкономические характеристики позволяют использовать его в домашних условиях как средство первой линии терапии контагиозного моллюска.
Некоммерческое партнерство "ГЕРПЕС-ФОРУМ";
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения Москвы
ФГБУ "Российский научный центр хирургии им. акад. Б.В. Петровского" РАМН, Москва
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
Центр вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии Департамента здравоохранения, Москва, 129226, Российская Федерация
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
ФПКМР РУДН, Москва
Центр вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии Департамента здравоохранения, Москва, 129226, Российская Федерация
Бородавки и контагиозный моллюск: сложные случаи "простых" диагнозов
Журнал: Клиническая дерматология и венерология. 2014;12(3): 63‑71
Халдин А.А., Молочков А.В., Гилядов А.Д., Быханова О.Н., Лапушко О.В., Исаева Д.Р., Баграмова Г.Э., Обыденнова К.В. Бородавки и контагиозный моллюск: сложные случаи "простых" диагнозов. Клиническая дерматология и венерология. 2014;12(3):63‑71.
Khaldin AA, Molochkov AV, Giliadov AD, Bykhanova ON, Lapushko OV, Isaeva DR, Bagramova GÉ, Obydennova KV. Warts and molluscum contagiosum: complex cases of simple diagnoses. Klinicheskaya Dermatologiya i Venerologiya. 2014;12(3):63‑71. (In Russ.).
Некоммерческое партнерство "ГЕРПЕС-ФОРУМ";
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения Москвы
Вирусные заболевания человека, в частности, дерматологические, представляют одну из наиболее значимых медико-социальных проблем современного здравоохранения. Среди вирусных дерматозов различают заболевания, обусловленные вирусами папилломы человека и контагиозного моллюска. В подавляющем большинстве случаев диагностика бородавок и контагиозного моллюска не представляет проблем, однако разнообразие их клинических проявлений и локализаций требуют от врача знаний и клинического опыта. В статье обобщен опыт работы центра вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии. Опираясь на собственный опыт наблюдений, авторы описывают патоморфоз клинических проявлений папилломавирусной инфекции и контагиозного моллюска, представляющий в настоящее время определенные трудности для диагностики и лечения этих вирусных дерматозов. Подробно представлена клиническая картина папилломавирусной инфекции и контагиозного моллюска у детей и взрослых с учетом локализации эффлоресценций, сопутствующих заболеваний как со стороны кожного покрова, так и внутренних органов и систем. Лечение вирусной патологии представляет собой сложный и трудоемкий процесс. Накопленный опыт позволил авторам выработать общие подходы к терапии и тактике ведения пациентов, инфицированных вирусом папилломы человека, в зависимости от места локализации патологии. Следует также обратить внимание на необходимость комплексного лечения с целью профилактики рецидивов. Речь идет о сочетании методов деструкции вирусных новообразований с использованием иммунных препаратов противовирусного действия. Авторами представлен положительный опыт использования комбинации рекомбинантного интерферона-альфа-2b с антиоксидантами при лечении и профилактике рецидивов бородавок различной локализации.
Некоммерческое партнерство "ГЕРПЕС-ФОРУМ";
Московский научно-практический Центр дерматовенерологии и косметологии Департамента здравоохранения Москвы
ФГБУ "Российский научный центр хирургии им. акад. Б.В. Петровского" РАМН, Москва
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
Центр вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии Департамента здравоохранения, Москва, 129226, Российская Федерация
Московский научно-практический центр дерматовенерологии и косметологии Департамента здравоохранения, Москва, 119071, Российская Федерация;
Центр вирусной патологии кожи, Москва, 129226, Российская Федерация
ФПКМР РУДН, Москва
Центр вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии Департамента здравоохранения, Москва, 129226, Российская Федерация
Среди вирусных дерматозов можно условно выделить две группы инфекций. Такое деление основано на тропности возбудителей, т.е. степени вовлечения в вирусный процесс кожи, внутренних органов и нервной системы; роли иммунной системы в патогенезе заболеваний; течении вирусных дерматозов (склонность к спонтанным рецидивам) и возможности к вирусной персистенции.
Однако это деление, как было сказано выше, носит условный характер, так как любая вирусная инфекция кожи манифестирует на фоне снижения иммунитета (системного и/или местного), может проявляться повторно (реинфицирование ВПЧ и ВКМ), а также персистировать не только в паравертебральных ганглиях (как ГВИ), но и в клетках кожи и слизистых оболочках (как ВПЧ и ВКМ) [5, 6].
Вместе с тем такое деление, с позиции практической медицины, вполне логично и оправдано. Действительно, в подавляющем большинстве случаев контагиозного моллюска и бородавок с различной локализацией поражений кожи клиническая диагностика самого дерматоза и выбор рутинного подхода к лечению пациента обычно не вызывают затруднений. Однако в ряде случаев при видимой простоте эти заболевания являются очень сложными, а лечение пациента занимает много времени и сил. Нам, специалистам центра вирусной патологии кожи Московского научно-практического центра дерматовенерологии и косметологии, нередко приходится сталкиваться с ситуациями, требующими индивидуального и неординарного подхода к лечению больных вирусными дерматозами.
Анализ работы центра позволяет констатировать, что к основным сложностям терапии можно отнести следующие: локализация вирусных высыпаний в сложных для удаления местах и в зонах повышенной чувствительности кожи; непрерывные рецидивы с вовлечением в вирусный процесс новых областей поражения; гигантские кондиломы Бушке-Левенштейна, занимающие большую площадь кожи и слизистых оболочек (аногенитальные бородавки, расположенные площадкой); ладонно-подошвенные бородавки у пациентов на фоне синдрома Рейно, некоторых ангиитов кожи, венозной недостаточности, сахарного диабета, хронического лимфостаза, а также онихомикозов; бородавки, в том числе аногенитальные, у ВИЧ-инфицированных больных.
Считается, что лечение детей с бородавками и контагиозным моллюском не вызывает сложностей. Действительно, в большинстве случаев вирусные новообразования локализуются в доступных для удаления местах и обычно носят ограниченный характер. Однако в последнее время нам все чаще приходится сталкиваться с неординарными ситуациями, и в первую очередь это касается локализаций высыпаний, в частности приуроченности вирусных эффлоресценций к аногенитальной области (рис. 1) и к лицу (рис. 2). Рисунок 1. Клинические проявления папилломавирусной инфекции в аногенитальной области у детей. а - аногенитальные бородавки у мальчика в возрасте 2 лет; б - то же у мальчика в возрасте 4 лет; в - гигантская кондилома у девочки в возрасте 5 лет. Рисунок 2. Клинические проявления папилломавирусной инфекции и вируса контагиозного моллюска на коже лица у детей. а - плоские бородавки в сочетании с вульгарными бородавками на коже кистей; б - сочетание вульгарных и плоских бородавок; в - распространенные высыпания контагиозного моллюска.
Причинами таких клинических ситуаций являются поздняя обращаемость по поводу вирусных дерматозов, а также наличие подобного заболевания на руках у близких родственников. В первом случае эффлоресценции, как правило, вначале локализуются на кистях и/или туловище, а далее наблюдается аутоинокуляция вирусов, во втором - заражение ребенка происходит контактно-бытовым путем. Сложности лечения при таких локализациях связаны с тем, что в вирусный процесс вовлекаются области, где имеется повышенная чувствительность кожи и слизистых оболочек, более высокий риск вторичных бактериальных осложнений, а также существует возможность формирования значимых косметических дефектов после удаления вирусных новообразований. В связи с этим в терапии должны применяться наиболее щадящие методы удаления (лазерные или радиохирургические технологии) с адекватным обезболиванием. В случаях сочетания вульгарных и плоских бородавок удалять следует лишь вульгарные, а области с плоскими бородавками рекомендуется лечить консервативно с применением противовирусных средств (мази и гели с интерфероном-альфа-2b). Необходимым условием при ведении детей с аногенитальными бородавками, особенно девочек, является ВПЧ-типирование. В случае выявления ВПЧ высокого онкогенного риска целесообразно провести вакцинацию после удаления вирусных новообразований с дальнейшим динамическим наблюдением.
Следует особо отметить, что вирусные новообразования в области лица почти всегда возникают в результате аутоинокуляции при наличии у пациента высыпаний на кистях и достаточно часто встречаются не только у детей, но и у взрослых. В случае вирусного поражения кожи в области головы высыпания могут возникать на любом участке. Наиболее часто вирусные новообразования локализуются в области век, носогубного треугольника и ушных раковин (рис. 3, а-д), реже - на волосистой части головы или губах (см. рис. 3, е, ж). Рисунок 3. Клиническая картина вульгарных бородавок на коже головы при различной локализации на фоне сопутствующей патологии со стороны кожного покрова. а - в области нижнего века на фоне акне (комедоны); б - то же на фоне себорейного дерматита; в - в области боковой поверхности спинки носа на фоне розацеа; г - в области ушной раковины на фоне себореи; д - то же на фоне ксероза; е - на коже волосистой части головы на фоне себорейного дерматита; ж - на слизистой оболочке нижней губы на фоне хейлита у пациента с бородавками на пальцах кистей.
Анализ всех случаев наличия бородавок в области головы свидетельствует, что практически у всех пациентов есть фоновые кожные патологии: себорейный дерматит, акне, розацеа, хейлит или конституциональный ксероз. По-видимому, именно наличие данных дерматозов и является фактором, способствующим аутоинокуляции вируса в результате расчесывания, а также воспалительных реакций в коже, ведущих к дисбалансу местного иммунитета. В связи с этим при обращении пациентов с бородавками на кистях и наличии у них какого-либо дерматоза на лице для профилактики распространения вирусного процесса следует рекомендовать применение мазей или гелей с интерферонами в течение 10-14 дней после удаления высыпаний.
В подавляющем большинстве случаев заражение ВПЧ с развитием аногенитальных бородавок у взрослых происходит в результате половых контактов. Заболеваемость ими в структуре инфекций передаваемых половым путем достаточно высокая и имеет стойкую тенденцию к росту. У многих пациентов вирусный процесс носит локализованный характер и обычно не вызывает сложностей при адекватной терапии, базирующейся на удалении высыпаний и иммунной профилактике рецидивов. Однако в ряде случаев лечение данной группы больных становится трудным и длительным процессом.
Для достижения терапевтического эффекта при лечении гигантских кондилом Бушке-Левенштейна требуется много времени и процедур. Важным условием успешного лечения служит комбинированная терапия с обязательным назначением курсового обкалывания области высыпаний интерферонами. Чтобы больной полностью закончил курс терапии, который нередко занимает 1-2 мес, очень важно оказывать ему психологическую помощь и проводить индивидуальное консультирование. При вовлечении в вирусный процесс слизистых уретры или его развитии в полости рта необходима консультация и лечение пациента у клиницистов соответствующего профиля. Лучше, чтобы удаление вирусных новообразований проводил специалист, так как вероятность осложнений в этих ситуациях крайне велика, и наряду с деструкцией вирусных высыпаний требуется комплекс реабилитационных мероприятий. Во всех случаях локализации вирусного процесса в аногенитальной области или на слизистой оболочке полости рта обязательно следует проводить ВПЧ-типирование. Если причиной вирусной патологии является онкогенный штамм возбудителя, необходима вакцинация пациента с целью профилактики раковых заболеваний и его последующее динамическое наблюдение.
В контексте лечения одной из наиболее проблемных групп пациентов являются больные с ладонно-подошвенными бородавками. Эта локализация характеризуется крайне упорным течением и склонностью к спонтанным повторным проявлениям. Особые сложности возникают при наличии у пациентов сопутствующих заболеваний, которые нередко являются фоновым процессом для развития вирусного процесса. В первую очередь это грибковая инфекция кожи стоп и ногтей, а также сосудистые заболевания нижних конечностей и сахарный диабет (рис. 5). Рисунок 5. Клинические проявления папилломавирусной инфекции на фоне сопутствующей патологии. а - подошвенные бородавки на фоне эпидермофитии стоп; б - то же на фоне хронического лимфостаза; в - то же на фоне сахарного диабета. Сопутствующие заболевания приводят к нарушению микроциркуляции, развитию гиперкератоза и способствуют снижению естественной резистентности кожи к вирусным инфекциям. В результате этого течение вирусного процесса становится, как правило, крайне агрессивным. Это проявляется в большей распространенности и генерализации вирусных высыпаний на подошвах, в устойчивости к различным методам деструкции с повторными проявлениями в местах удаления, в нарастании кожной симптоматики с вовлечением в процесс новых областей, а также в плохой заживляемости после удаления элементов. В связи с этим пациентов, страдающих ладонно-подошвенными бородавками на фоне сопутствующих заболеваний, необходимо готовить к удалению новообразований. В первую очередь необходимо устранить или нивелировать действие провоцирующих факторов - лечить грибковую инфекцию, проводить сосудистую терапию, контролировать содержание глюкозы в сыворотке крови. Также обязательным компонентом является длительная местная терапия интерферонами (мазь, гель), которая позволяет значительно снизить риск повторных проявлений. Местная интерферонотерапия должна предшествовать удалению высыпаний и продолжаться после его проведения еще в течение 14 дней. Учитывая плохую регенерацию тканей при сосудистых патологиях, после удаления бородавок необходимо назначение препаратов, улучшающих репаративные процессы в коже, а также дезинфицирующих или антибактериальных средств.
В заключение следует остановиться на сложных случаях, связанных с рецидивирующим течением вирусных дерматозов, обусловленных ВПЧ. По имеющимся данным, примерно у 30% пациентов после удаления вирусных новообразований отмечается появление новых элементов, а при некоторых локализациях частота возрастает. По нашим наблюдениям, наиболее часто рецидивы возникают при ладонно-подошвенных и аногенитальных бородавках. Причинами этого могут служить нерациональные методы удаления, несоблюдение принципов комплексной терапии и профилактики вирусных дерматозов, а также иммунодефициты как системного, так и местного характера. При выборе метода удаления следует оценивать толщину рогового слоя участка, пораженного ВПЧ, локализацию высыпаний и степень глубины деструктивного воздействия выбранной методики. В настоящее время накопленный опыт позволяет рекомендовать следующие подходы в зависимости от локализации бородавок:
1) криодеструкция при вульгарных бородавках на кистях, в том числе подногтевых;
2) электрокоагуляция при ладонно-подошвенных;
3) радиохирургия или лазерная вапоризация при вульгарных бородавках на лице;
4) радиохирургические методики при аногенитальных бородавках, в том числе с формированием гигантских кондилом Бушке-Левенштейна и поражением слизистых оболочек.
Что такое кондиломы остроконечные? Причины возникновения, диагностику и методы лечения разберем в статье доктора Богданова Дениса Валерьевича, проктолога со стажем в 21 год.
Над статьей доктора Богданова Дениса Валерьевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Остроконечные кондиломы — образования на коже, вызванные наличием в тканях вируса папилломы человека (ВПЧ). Активизация вирусов приводит к появлению разрастаний на поверхности кожи в области заднего прохода, наружных половых органов и анальном канале.
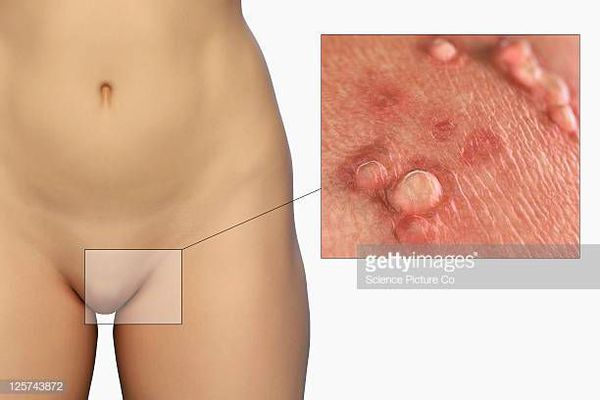
Аногенитальные бородавки представляют собой выступающие над поверхностью кожи объёмные мягкие выросты бледно-розового цвета с неоднородной поверхностью. Размеры и количество бородавок варьируются от единичных кондилом 1-2 мм в диаметре до множественных, часто сливных образований размером до 9-10 см и даже более.
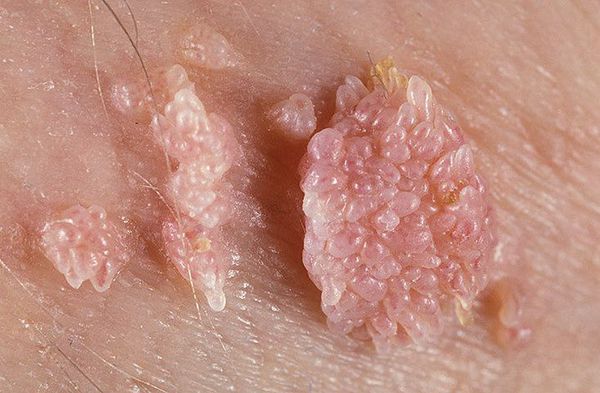
Кондиломы могут появляться и вырастать до значительных размеров буквально за несколько дней.
Причиной появления кондилом является присутствие вируса папилломы человека в крови. В организм вирус попадает при половом контакте через дефекты в слизистой или коже. Возможен перинатальный путь передачи — ребёнок заражается во время родов от больной матери при прохождении по родовым путям. Также имеет место контактно-бытовой путь передачи, но данные об этом варианте передачи немногочисленны.
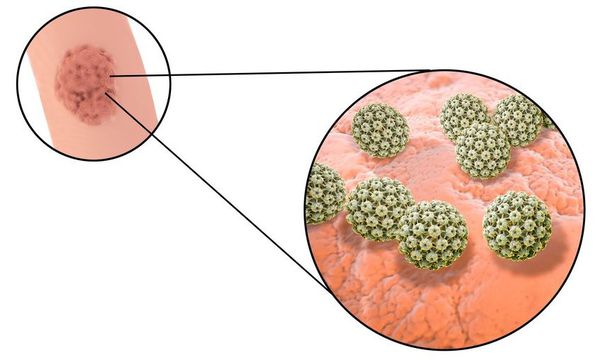
Длительное время после заражения человек может не подозревать о своём носительстве ВПЧ. Период инкубации зависит от особенностей иммунитета индивида и может длиться от двух месяцев до трёх лет. В дальнейшем, при снижении активности иммунных механизмов, в характерных локациях появляются бородавки (кондиломы). [7] [8] [16]
ВПЧ относится к одной из наиболее частых инфекций, передающихся половым путём (ИППП) — до 55-65% от общего числа заболеваний. [1] [4] [6] Опасность его состоит также в том, что носитель может не подозревать о своём заболевании и не иметь внешних признаков инфекции (выростов, бородавок).
Известно до 600 видов ВПЧ (HPV), некоторые из которых проявляются бородавками кожи на груди, лице, подмышечных впадинах. Другие выбирают своей локализацией слизистые оболочки рта, половых органов или анального канала. При аногенитальных кондиломах чаще выявляют 6 и 11 типы HPV (папилломавируса). [4]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы остроконечных кондилом
Вне обострения наличие ВПЧ в крови никак не проявляется. При активации вирусной инфекции симптомы болезни могут появиться буквально за несколько часов:
- образование остроконечных кондилом (чаще в местах наибольшей травматизации, трения при половом контакте):
– на коже вокруг ануса, в промежности, на уздечке, головке полового члена, губках наружного отверстия мочеиспускательного канала у мужчин;
– на слизистой половых губ у женщин, в уретре у мужчин;
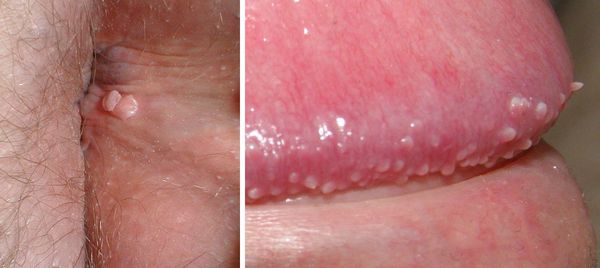
- зуд, жжение, дискомфорт в месте появления бородавок — такие неприятные ощущения часто бывают очень интенсивными и значительно влияют на самочувствие пациента;
- ощущение инородного предмета в анальном канале (при образовании кондилом внутри заднепроходного отверстия);
- выделение небольшого количества крови в виде алых полосок при дефекации (если кондиломы расположены внутри анального канала и травмируются при прохождении каловых масс);
- дизурия, болезненность при мочеиспускании, если бородавки находятся в уретре;
- болезненность во время полового акта (диспареуния).
Другим вариантом проявления ВПЧ может стать наличие в области промежности папул с бархатистой поверхностью или пятен серовато-бурого, розового или красновато-коричневого цвета. [2] Такие морфологические формы встречаются намного реже и часто вызывают затруднение при постановке первичного диагноза.
Патогенез остроконечных кондилом
Ключевым моментом в патогенезе заболевания становится проникновение HPV в организм хозяина. При однократном половом контакте вероятность заражения составляет 80%, затем при хорошем состоянии иммунной системы инфекционные агенты подвергаются элиминации (уничтожаются).
Вирусы различных типов адаптированы к определённому хозяину. Существуют сотни типов вирусов, многие из них не опасны для человека, так как тропны к тканям млекопитающих, рептилий и птиц и вызывают у них доброкачественные опухоли (образование папиллом). [3]
При изучении ВПЧ выделили три рода вирусов — альфа, бета, гамма. Из них аногенитальные поражения вызывают папилломавирусы первой группы (α). Инфекционные агенты, относящиеся к родам Бета и Гамма, чаще встречаются при папилломах ороговевающего эпителия [3] — появляются подошвенные, ладонные бородавки.
В родах при классификации вирусов выделили типы (генотипы). Они обозначаются арабскими цифрами. Из сотни генотипов вирионов выделяют частицы с высоким канцерогенным риском – это α 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59. Их выявляют в 90-95% случаев при злокачественных процессах шейки матки, влагалища и вульвы. Особенно значимы 16 и 18 типы. Такие онкогенные типы ВПЧ, содержащие в своём ДНК белки Е6 и Е7, способны подавлять активность белков-супрессоров опухолей р53 и рRb, приводя к быстрому злокачественному перерождению папиллом в карциномы.
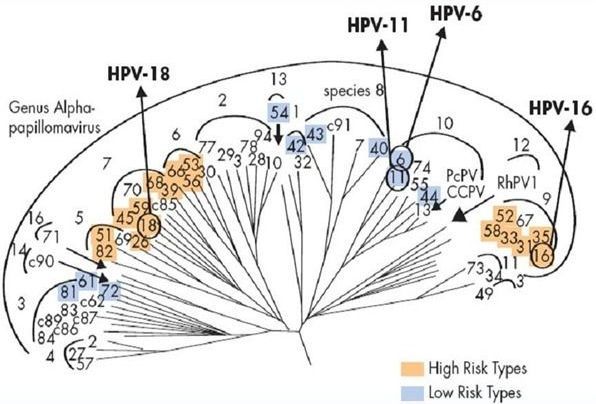
Порядка 90% случаев аногенитальных кондилом вызываются ВПЧ α 6 и 11. Это возбудители низкого канцерогенного риска. [5] К этой же группе низкого риска относят ВПЧ 40, 42, 43, 44, 54, 61, 72, 81.
Проникновение
Вирионы через микроскопические повреждения проникают в базальный слой эпителия, затем прикрепляются к белкам мембраны клетки. Далее они задействуют механизм рецепторного эндоцитоза (при участии интегрина и белка L1 из вирусного капсида) и попадают в цитоплазму. Белок L2 из капсида вируса способствует высвобождению ДНК вируса и попаданию его в ядро. [5]
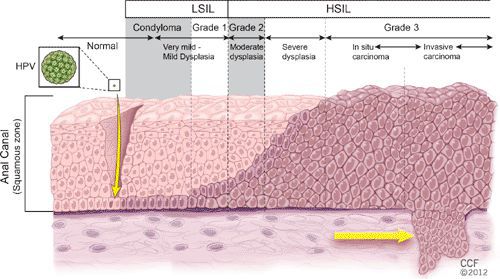
Размножение
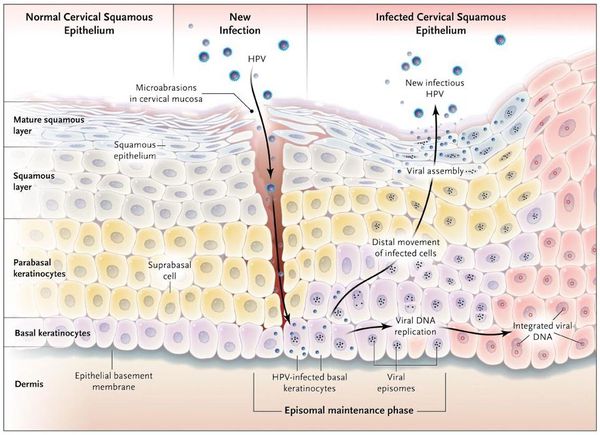
Проявления
Появляются аномальные эндофитные или экзофитные выросты эпителия — папилломы, пятна или кондиломы. Рыхлая слизистая или атипичный эпителий выростов склонен к быстрой травматизации и мацерации (размягчению). На таком фоне быстрее присоединяется вторичная инфекция, появляются болезненность, дискомфорт, обильное отделяемое, воспаление, отёк, неприятный запах, изъязвление кондилом. [2] [3]
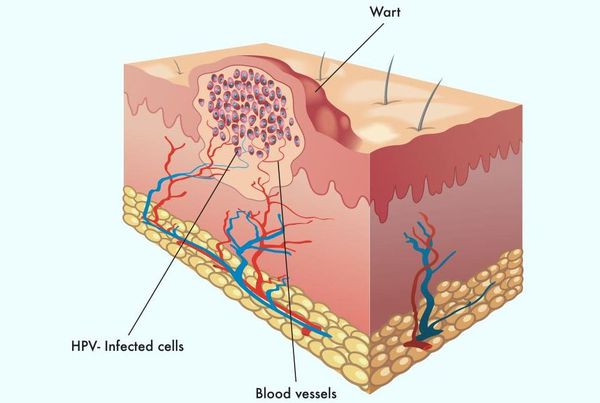
В клетках базального слоя происходит активная репликация вируса, по мере дифференцировки клеток кондилом их кровоснабжение резко обедняется, редуцируют центральные сосуды. Но, оставаясь в верхних слоях эпителия в неактивной форме, именно здесь вирус опасен в плане контактного инфицирования.
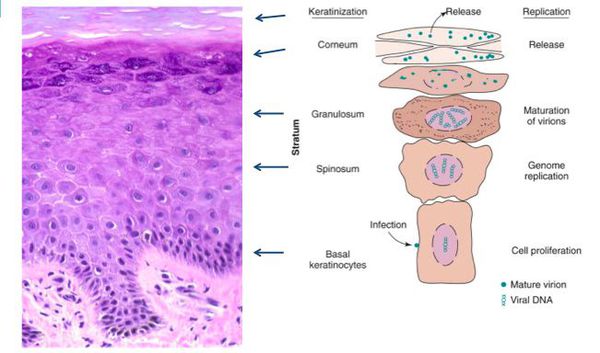
При гистоанализе биопсийных материалов эпителий утолщён, выявляются участки акантоза, папилломатоза. Обнаруживаются койлоциты (изменённые в размерах клетки со светлой цитоплазмой, множеством вакуолей, перинуклеарным светлым ободком). Их ядра гиперхроматичны. Часто встречаются клетки с двумя ядрами и более. [8]
Из вышеперечисленного можно сделать вывод: вирусы, вызывающие образование аногенитальных бородавок, в 90% случаев относятся к типам α 6 и 11 HPV. [6] [7] Они с низкой степенью вероятности могут вызвать малигнизацию (раковое перерождение). Однако часты случаи совместной персистенции (пребывания) вирусов различных типов у одного носителя. Это обязывает пациента и доктора особенно внимательно относится к профилактическим осмотрам, их качеству и регулярности для предотвращения аноректального рака.
Классификация и стадии развития остроконечных кондилом
Остроконечные кондилломы являются наиболее частыми, классическими проявлениями папилломавирусной инфекции кожи и слизистых в аногенитальной области — до 65% от числа заболеваний, передающихся половым путёv. [1]
Другими диагностическими находками могут быть:
- бородавки в виде папул;
- инфильтрация слизистой в виде пятен розовато-серого или коричневого цвета;
- внутриэпителиальная неоплазия;
- бовеноидный папулёз, болезнь Боуэна — отдельный вид папул, они появляются как пятна на слизистых красновато-бурого, оранжево-бурого цвета, на коже цвет образований серовато-розовый;
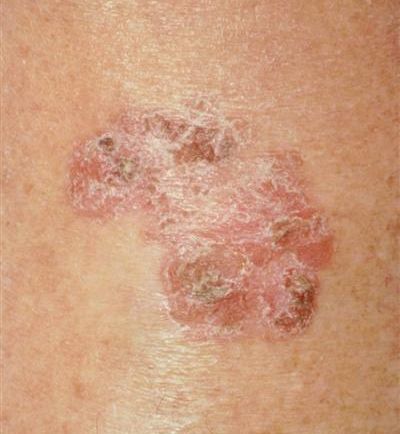
- гигантская папиллома (Бушке — Левенштейна). Её рост начинается с остроконечных кондилом, которые довольно быстро увеличиваются в размерах и количестве, сливаются и превращаются в крупную опухоль с неровной поверхностью, покрытой вегетациями и ворсинчатоподобными выступами.
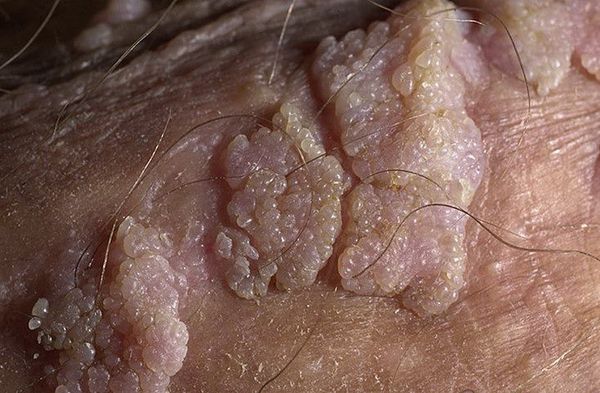
Хотя болезнь (гигантская папиллома) ассоциируется с типами вирусов 6 и 11, с низким риском канцерогенеза, именно в случаях гигантских папиллом происходит подавление белка-супрессора опухолей р53, и образование трансформируется в плоскоклеточный рак. Причиной такой частой малигнизации (озлокачествления) может быть наличие иммунодефицитных состояний, ассоциированных инфекций, хронических дистрофических состояний кожи (склероатрофический лихен, красный плоский лишай). Даже после радикального хирургического лечения [9] папиллома Бушке — Левенштейна склонна к частому рецидивированию. [10]
Осложнения остроконечных кондилом
Эстетические проблемы. Быстро разрастающаяся ткань кондилом, помимо физического дискомфорта, приносит массу неудобств пациенту. Выросты в области наружных половых органов, заднего прохода значительно снижают самооценку и мешают полноценной половой жизни и правильной гигиене.
Нагноение, воспаление. Аногенитальные бородавки имеют свойство быстро травмироваться при незначительных механических воздействиях или трении. Эти микротравмы, ранки становятся воротами для вторичного инфицирования. Появляются эрозии, перифокальное воспаление. Раны начинают мацерироваться (мокнуть), нагнаиваться. При развитии осложнения присоединяются неприятный запах и боль. Проводить тщательную гигиеническую обработку перианальной области из-за разрастаний становится невозможным, что ещё больше усугубляет воспалительный процесс.
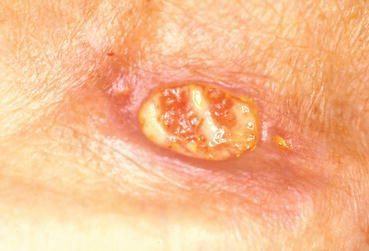
Малигнизация. Типы вирусов с высокой канцерогенной активностью, персистируя (долго находясь) в коже и слизистых, приводят к трансформации клеток и их перерождению в атипичные (раковые) клетки. Как уже упоминалось, аногенитальные бородавки обычно не так опасны в плане раковой трансформации, как вирусное поражение шейки матки (ВПЧ 16, 18 типов и т. д). Но проблема может появиться, если у пациента присутствует два и более типов вируса с различными индексами канцерогенности и имеется иммунодефицитное состояние.
Важно изменение образа жизни в целом для постоянного поддержания здоровья и предупреждения активизации дремлющих вирионов.
Диагностика остроконечных кондилом
При выявлении остроконечных кондилом в перианальной зоне целью дополнительных диагностических исследований является уточнение генотипа ВПЧ, а также исключение внешне схожих с ними образований:
- интрадермальный невус;
- контагиозный моллюск;
- сифилитический шанкр;
- себорейный кератоз.
Быстрым способом установления ВПЧ в образованиях (кондилломах) во время приёма является проба с 5% раствором уксусной кислоты. Под воздействием этого вещества папилломы, вызванные HPV, бледнеют, приобретая сероватый, бледный оттенок, в них визуализируется характерный капиллярный рисунок. Исследование носит предварительных характер.
Минимальные лабораторные исследования:
- серологическая реакция на возбудителей сифилиса;
- обнаружение антител к ВИЧ, гепатитам В,С;
- ПЦР для типирования вируса;
- цитология мазка из шейки матки у женщин;
- цитология мазков-отпечатков;
- исследование биоптатов и удалённых образований — аногенитальных бородавок.
При частых рецидивах болезни, крупных размерах опухолей, быстром их росте или сомнительном диагнозе прибегают к дополнительным методам исследования.
При частых обострениях проводится исследование имунного статуса.
При подозрении на злокачественное перерождение кондилом, папилломах на широком основании, нетипичных выделениях из влагалища или прямой кишки проводят:
- УЗИ вагинальным и ректальным датчиком;
- колоноскопию;
- УЗИ органов брюшной полости;
- рентгенографию органов грудной клетки;
- кольпоскопию;
- исследования на ИППП . [1][12][13]
Часто пациенты направляются на консультацию к гинекологу, урологу, онкологу и дерматовенерологу.
Лечение остроконечных кондилом
В случае с остроконечными кондиломами наиболее результативен комплексный подход к лечению. Следует обязательно информировать пациента о необходимости лечения половых партнёров, их возможном носительстве ВПЧ.
Даются общие рекомендации о необходимости модификации образа жизни для поддержания адекватного состояния иммунитета, предупреждения дополнительного инфицирования другими ИППП:
- упорядочение половой жизни;
- применение барьерных методов контрацепции;
- коррекция веса;
- достаточные физические нагрузки;
- правильное питание и т. д.
Консервативное лечение
Применяются препараты, стимулирующие местный и гуморальный иммунный ответ. Это необходимо, так как у всех больных с папилломатозным поражением выявлялись нарушения интерферонового статуса (системы врождённого иммунитета). [1] Противопоказаниями к терапии иммуномодуляторами являются папилломы на широком основании.
Редуцирование симптомов возможно в трёх из четырёх случаев (до 84%) при единичных кондиломах небольших размеров. [1] [17]
При упорном, рецидивирующем течении болезни, а также если больного беспокоят эстетические моменты, для профилактики раковой трансформации прибегают к хирургическим методам.
Хирургическое лечение
В зависимости от размеров, формы, расположения кондиломы и предпочтений хирурга возможно применение химических, физических, цитотоксических методов удаления.
Физические методы применяются при любых размерах и расположении аногенитальных бородавок. По выбору используется скальпель, лазерная вапоризация, криодеструкция (разрушение ткани бородавки экстремально низкими температурами под воздействием жидкого азота) или радиоволновой способ (radioSURG).
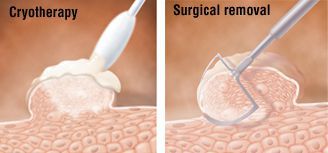
Ткани иссекаются включительно с собственной пластиной дермы. Если удаляется кондилома анального канала, дно раны образует внутренний сфинктер. В перианальной зоне дно раны должна составлять подкожная клетчатка.
Удаление образований не проводится без консультации онколога, если есть малейшие подозрения на малигнизацию (изъязвление, некроз, инфильтративный рост).
Обычно при иссечении кондиломы достаточно местной или спинальной анальгезии (снижения чувствительности к боли). Госпитализация может проводиться в случаях некоторых сопутствующих заболеваний (патология свертывания и другие), а также при невозможности амбулаторного лечения.
Прогноз. Профилактика
Прогноз при своевременном и адекватном лечении остроконечных кондилом благоприятный. Обязательно проведение гистологического исследования удалённых образований для исключения диагноза злокачественной опухоли. В сомнительных случаях необходимы дополнительные консультации гинеколога, дерматовенеролога, онколога, радиолога, лабораторные и инструментальные исследования.
При комплексном лечении обычно все симптомы исчезают. Однако не исключены рецидивы, частота которых колеблется от 10 до 50% и более. На увеличение риска рецидивов влияет общее состояние здоровья пациента, наличие у него сопутствующих заболеваний и иммунодефицитных состояний.
Профилактика включает в себя:
- своевременное, профилактическое обследование у гинеколога, уролога и проктолога;
- коррекцию образа жизни, питания;
- упорядочение половых отношений.
До начала половой жизни можно по схеме пройти вакцинацию поливалентной вакциной от ВПЧ 6, 11, 16, 18 типов (самые частые причины остроконечных кондилом — HPV 6 и 11) и рака шейки матки (HPV 16 и 18). Рекомендуемый возраст для введения вакцины — 9-17 лет (к примеру, в календаре США от 2015 года рекомендуемы возраст вакцинации — 9-11 лет). В ряде стран (США, Австрия, Германия, Франция и др.) вакцинация включена в календарь обязательных прививок. В России в настоящее время это добровольная процедура. [18]
Читайте также:

