На какой вирус похож вирус вич
Обновлено: 25.04.2024
Вокруг темы ВИЧ-инфекции множество заблуждений. Это происходит из-за недостаточной информированности населения о происхождении и способах передачи заболевания. Наиболее распространенной является путаница в понятии, что такое ВИЧ, чем он отличается иммунодефицита и от СПИДа.
Что такое ВИЧ?
ВИЧ – вирус иммунодефицита человека. Поражая клетки иммунной системы, он вызывает развитие ВИЧ-инфекции, которая угнетает работу иммунитета и приводит к развитию СПИД – синдрома приобретенного иммунного дефицита. На скорость развития ВИЧ-инфекции влияет множество факторов. Определяющим из них является статус иммунной системы человека.
Что такое иммунный статус?
Иммунный статус – это комплексный показатель, демонстрирующий общее состояние иммунной системы. Он отображает активность органов иммунитета и вырабатываемых ими клеток, для защиты организма.
Для изучения состояния иммунитета проводят клинико-лабораторное исследование, которое включает в себя сбор анамнеза пациента и клинический анализ крови.
Проведение анализов на выявление бактерионосительства и вирусоносительства.
После получения предварительной информации, проводят иммунограмму - тесты ориентировочного уровня, позволяющие выявить грубые нарушения в работе иммунной системы. Проведение тестов предполагает получение следующей информации:
- Число лимфоцитов.
- Фагоцитарная (захватывающая) активность лейкоцитов.
- Количество и качество работы Т- и В-клеток.
- Концентрация иммуноглобулинов.
Полученные данные исследуют с помощью флюоресцирующих сывороток, чувствительных к CD-антигенам - поверхностным антигенным маркерам. CD-антигены это специфические белки, выполняют функцию рецепторов и веществ, отвечающих за взаимодействие клеток иммунной системы между собой.
На данный момент известно порядка 350 CD-антигенов и их список продолжает пополняться. Но для мониторинга ВИЧ-инфекции интерес представляют CD4+ и CD8 антигены, связанные с Т-лимфоцитами. Их число определяет ВИЧ-статус человека.
Что такое ВИЧ-статус? Как его узнать?
ВИЧ-статус – это показатель, демонстрирующий наличие или отсутствие ВИЧ-вируса в организме человека. Для определения ВИЧ-статуса применяют следующие виды диагностики.
- Косвенные тесты – выявляют наличие специфических антител к ВИЧ.
- Прямые тесты – определяют сам вирус, его антигены и нуклеиновые кислоты, тем самым выявляя вирусную нагрузку.
Важным показателем вирусной нагрузки является число CD4+ Т-лимфоцитов. Снижение их количества на фоне увеличения числа CD8+ лимфоцитов помогает выявить наличие ВИЧ-инфекции, оценить состояние иммунной системы человека и ее способность противостоять развитию СПИДа.
Иммунодефицит и ВИЧ - одно и то же?
Нет! Это разные понятия.
Иммунодефицит – это нарушение функций иммунной системы. Дефекты иммунитета могут быть первичными, т.е. врожденными, например, синдром Ди Джоржи, синдром Вискотта-Олдрича, болезнь Костмана и т.д. Или вторичными, т.е. приобретенными в процессе жизни.
ВИЧ – это вирус иммунодефицита человека, который относят к ретровирусам. По своей сути, это неклеточный инфекционный агент, который проникает в организм человека и поражает клетки иммунной системы, вызывая ее угнетение и развитие синдрома приобретенного иммунного дефицита СПИД.
В простом понимании, ВИЧ – это инфекция, вызывающая иммунодефицит. Но сам по себе иммунодефицит может возникнуть и под влиянием совершенно иных факторов – плохая экология, острое отравление организма, хронический стресс, ранее перенесенные инфекционные заболевания, гельминты, неправильный рацион питания и т.д.
ВИЧ и СПИД - одно и то же?
Нет! Не нужно путать причину и следствие.
ВИЧ – это вирус. А СПИД – это тяжелые последствия заражения вирусом. Проникая в организм человека, он вызывает развитие ВИЧ-инфекции – прогрессирующее заболевание, терминальной стадией которого и является СПИД.
Какие бывают ВИЧ-статусы? Что означают?
Согласно классификации ВОЗ, ВИЧ-статус человека может быть положительным, отрицательным или сомнительным. Последний вариант возможен в том случае, когда полученных в ходе тестов и анализов данных, недостаточно для того, чтобы подтвердить или опровергнуть наличие ВИЧ-инфекции в организме человека. Для получения положительного или отрицательного результата необходимо повторное исследование. Его проводят спустя 3, а затем 6 месяцев.
Положительный и отрицательный.
- Положительный ВИЧ-статус – в крови человека обнаружены антитела к ВИЧ-инфекции, что указывает на инфицирование вирусом.
- Отрицательный ВИЧ-статус – антител к ВИЧ-инфекции в крови не обнаружено. Человек здоров.
Ложноположительный и ложноотрицательный.
В редких случаях проведение тестов и анализов может дать ложноположительный или ложноотрицательный результат. Он возможен вследствие как из-за особенностей иммунитета пациента, так и неправильного хранения биоматериалов и элементарной врачебной ошибки.
- Ложноположительный – в крови обнаружены антитела к ВИЧ-инфекции, но при этом анамнез человека исключает возможность заражения вирусом. В этом случае речь может идти об сходных по своей структуре антителах, которые вырабатываются в организме при иных заболеваниях. Исследование необходимо провести повторно.
- Ложноотрицательный – антител к ВИЧ-инфекции не обнаружено, но анамнез человека и состояние его иммунной системы указывают на то, что он заражен вирусом. Скорее всего, тестирование было проведено преждевременно, т.е. не прошло 3 месяца с момента инфицирования. Или же иммунная система настолько слаба, что не в состоянии вырабатывать антитела к ВИЧ-инфекции. Исследование проводят повторно.
Для чего человеку знать свой ВИЧ-статус?
- При не выявленной ВИЧ-инфекции - продолжительность жизни 9-11 лет.
- Постановка диагноза СПИД при отсутствии лечения – 6-9 месяцев.
- При выявлении ВИЧ-инфекции на поздних стадиях и последующем лечении – 10-40 лет.
- Ранняя диагностика и эффективная ВААРТ – 20-50 лет.
Информирован - значит вооружен! Чем раньше произойдет выявление инфицирования, тем лучше. Пациенты с ВИЧ-инфекцией проходят высокоактивную антиретровирусную терапию, живут полноценной жизнью и доживают до глубокой старости. Определив свой ВИЧ-статус, вы проявляете заботу о своем здоровье и безопасности окружающих.

Обзор
Автор
Редакторы
Обратите внимание!
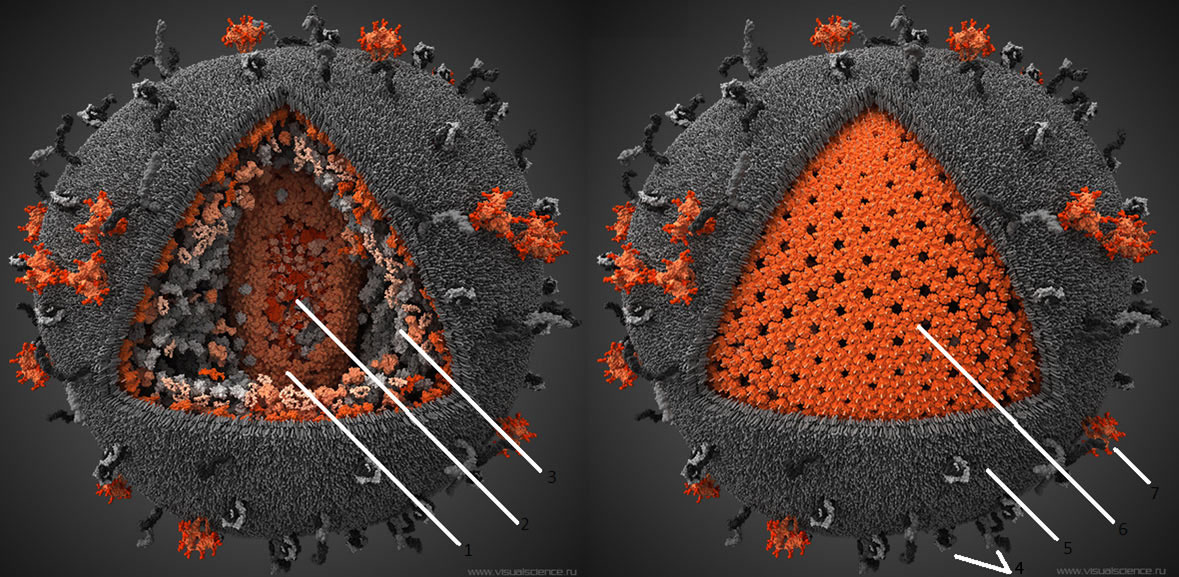
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
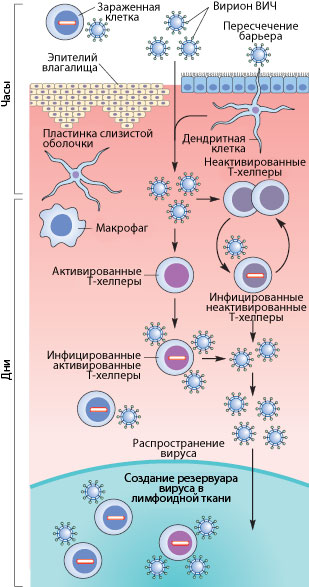
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Предполагается, что именно летучие мыши стали природным резервуаром для вируса SARS-CoV-2. Антитела, нейтрализующие вирус в пробирке, в организме могут, наоборот, усиливать инфекционный процесс. Иллюстрация Pixabay
Прошло 13 лет. Вакцина до настоящего времени не создана, и более того, о ней и бюджетных средствах, ушедших на ее создание, уже стараются не вспоминать, как, впрочем, и о научной репутации тех, кто ее обещал на уровне законодательной власти. Давайте с другой стороны посмотрим на проблему. На ВИЧ-вакцину были потрачены время и деньги. Сколько в 2007 году было ВИЧ-инфицированных россиян? Более 400 тысяч. Но сейчас-то уже на миллион больше, почти 1 400 000. Это не нули, это сломанные судьбы россиян, причем не менее 320 000 из них уже погибли от СПИДа. И где эта спасительная вакцина, которая должна была остановить эту эпидемию? Никаких выводов от нанесенного природой поражения сделано не было. Представления об инфекционных процессах остались прежними, то есть одними на все инфекции, и на имеющую нециклический характер ВИЧ-инфекцию, и на заканчивающуюся стерильным иммунитетом натуральную оспу. И сейчас мы вновь пошли по этому кругу, удобному, понятному и безответственному…
– Получается, что те врачи и ученые ввели в заблуждение общество и власть. Как тогда они объясняли, что создали ВИЧ-вакцину?
– По-видимому, есть какие-то принципиальные затруднения. Сейчас мы уже продвинулись вперед в знании иммунологии. Что мешает создать вакцину?
– Если сказать коротко, то явление антителозависимого усиления инфекции, о котором начали говорить только недавно, хотя оно известно с 1960-х годов. Антитела, нейтрализующие вирус в пробирке и на моделях живой ткани, в условиях организма могут усиливать инфекционный процесс, и это очень распространенное явление в мире вирусов и бактерий. Как его ни скрывай, а оно все равно вылезет.
Это разделение антител по функции, конечно, не укладывается в типовые представления об иммунитете, написанные для врачей авторами учебников, но так устроен мир.
– Получается, что, кроме первых двух типов антител, чуть ли не все остальные наносят вред организму! Когда нам важные люди говорят, что если есть антитела к вирусу, значит, человек защищен. О каких антителах идет речь? Не разобравшись в самих антителах, нам уже обещают на основании их наличия ввести иммунологический паспорт на каждого, а уж на основании этого паспорта решать, выпускать ли человека из карантина, допускать к работе или сажать его в самолет. Что за антитела образуются в ходе новой коронавирусной инфекции?
– Те же, что и во время прежних аналогичных инфекций. Проблема хорошо изучена, но и ее предпочитают замалчивать персонажи, так усердно дискредитирующие вакцинацию у нас в России. Основной антигенной детерминантой коронавирусов является S-белок. К нему, насколько это известно на сегодняшний день, в основном образуются антитела. Скорее всего некоторые из этих антител могут усиливать инфекционный процесс, облегчая проникновение возбудителя болезни в иммунные клетки через Fc-рецепторы. Одновременно они меняют тропность вируса (то, к чему он пристает, какие клетки атакует, сродство) с рецептора ACE2 бронхиальных клеток на Fc-рецепторы макрофагов и моноцитов и тем самым генерализуют инфекционный процесс…
– Я бы сравнил нынешнюю ситуацию с чрезвычайной: начался в доме пожар, а редактор Википедии сидит там за компьютером. Сирены воют, примчались пожарные, ему предлагают помощь, начинают спасать, а он быстро смотрит на номер пожарной машины, находит в Сети ссылки на пожарную часть и ищет информацию, есть ли у командира пожарного расчета публикации в зарубежных изданиях по пожарному делу, можно ли ему доверить свое спасение?
– Что бы сейчас вы посоветовали делать, какие действия властей считаете разумными: тесты, вакцинация?
Благодаря коронавирусу эпидемиология и иммунология уже стали другими, в научный оборот вовлечены новые понятия, которых раньше в научном пространстве России не было, мы их как раз сегодня обсуждали. Появились новые специализированные центры для лечения инфекционных больных. В борьбу с эпидемией вовлечены десятки тысяч медицинских специалистов, набирающихся собственного опыта и знаний, отсутствующих в учебниках, по которым они когда-то учились. Врачи и власти стали понимать, что эпидемические катастрофы не ушли в прошлое и нужно к ним готовиться заранее.
Читайте также:

