Оптическая плотность образца гепатит
Обновлено: 26.04.2024
Поверхностный антиген гепатита В в сыворотке крови в норме отсутствует.
Обнаружение поверхностного антигена (HBsAg) гепатита В в сыворотке подтверждает острое или хроническое инфицирование вирусом гепатита В.
При остром заболевании HBsAg выявляется в сыворотке крови в последние 1-2 недели инкубационного периода и первые 2-3 недели клинического периода. Циркуляция HBsAg в крови может ограничиваться несколькими днями, поэтому следует стремиться к раннему первичному обследованию больных. Метод ИФА позволяет выявить HBsAg более чем у 90% больных. Почти у 5% больных самые чувствительные методы исследования не обнаруживают HBsAg, в таких случаях этиология вирусного гепатита В подтверждается наличием анти-HBсAg JgM или ПЦР.
Концентрация HBsAg в сыворотке крови при всех формах тяжести гепатита В в разгар заболевания имеет значительный диапазон колебаний, вместе с тем имеется определенная закономерность: в остром периоде существует обратная связь между концентрацией HBsAg в сыворотке и тяжестью болезни.
Высокая концентрация HBsAg чаще наблюдается при легких и среднетяжелых формах болезни. При тяжелых и злокачественных формах концентрация HBsAg в крови чаще низкая, причем у 20% больных с тяжелой формой и у 30% со злокачественной антиген в крови может вообще не обнаруживаться. Появление на этом фоне у больных антител к HBsAg расценивается как неблагоприятный диагностический признак; он определяется при злокачественных формах гепатита В.
При остром течении гепатита В концентрация HBsAg в крови постепенно снижается вплоть до полного исчезновения этого антигена. HBsAg исчезает у большинства больных в течение 3 месяцев от начала острой инфекции.
Снижение концентрации HBsAg более чем на 50% к концу 3-й недели острого периода, как правило, свидетельствует о близком завершении инфекционного процесса. Обычно у больных с высокой концентрацией HBsAg в разгар болезни он обнаруживается в крови в течение нескольких месяцев.
У больных с низкой концентрацией HBsAg исчезает значительно раньше (иногда через несколько дней после начала заболевания). В целом срок обнаружения HBsAg колеблется от нескольких дней до 4-5 мес. Максимальный срок обнаружения HBsAg при гладком течении острого гепатита В не превышает 6 месяцев от начала заболевания.
HBsAg может быть обнаружен у практически здоровых людей, как правило, при профилактических или случайных исследованиях. В таких случаях исследуют другие маркеры вирусного гепатита В – анти HBсAg JgM, анти- HBсAg JgG, анти HBеAg и изучают функцию печени.
При отрицательных результатах необходимы повторные исследования на HBsAg.
Если повторные исследования крови в течение более 3 месяцев выявляют HBsAg, такого пациента относят к хроническим больным вирусным гепатитом В.
Наличие HBsAg – довольно распространенное явление. В мире насчитывается более 300 млн. носителей, а у нас в стране – около 10 млн. носителей.
Прекращение циркуляции HBsAg с последующей сероконверсией (образование анти-HBs) всегда свидетельствует о выздоровлении - санации организма.
Исследование крови на наличие HBsAg применяется в следующих целях:
для диагностики острого гепатита В:
- инкубационный период;
- острый период заболевания;
- ранняя стадия реконвалесценции;
для диагностики хронического вирусного гепатита В;
- персистирующем хроническом гепатите;
- циррозе печени;
для скрининга и выявления больных в группах риска:
- больные с частыми гемотрансфузиями;
- больные с хронической почечной недостаточностью;
- больные с множественным гемодиализом;
- больные с иммунодефицитными состояниями, в том числе СПИДом.
Оценка результатов исследования
Результаты исследования выражаются качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие HBsAg в сыворотке крови. Положительный результат – выявление HBsAg свидетельствует об инкубационном или остром периоде острого вирусного гепатита В, а также при хроническом вирусном гепатите В.
Антитела к ядерному антигену вируса гепатита В JgG (анти- HBcAg JgG )
В норме анти-HBcAg JgG в сыворотке отсутствует.
У больных анти-HBcAg JgG появляются в острый период вирусного гепатита В и сохраняются на протяжении всей жизни. Анти-HBcAg JgG – ведущий маркер перенесенного ВГВ.
Исследование крови на наличие анти-HBcAg JgG применяются для диагностики:
Оценка результатов исследования
Результат исследования выражается качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие анти-HBcAg JgG в сыворотке крови. Положительный результат – выявление анти-HBcAg JgG свидетельствует об острой инфекции, реконвалесценции или ранее перенесенном вирусном гепатите В.
В норме HBeAg в сыворотке крови отсутствует.
HBeAg можно обнаружить в сыворотке крови большинства больных острым вирусным гепатитом В. Он обычно исчезает в крови раньше HBs-антигена. Высокий уровень HBeAg в первые недели заболевания или обнаружение его на протяжении более 8 недель дает основание заподозрить хроническую инфекцию.
Этот антиген часто обнаруживается при хроническом активном гепатите вирусной этиологии. Особый интерес к определению HBeAg связан с тем, что его обнаружение характеризует активную репликативную фазу инфекционного процесса . Установлено, что высокие концентрации HBeAg соответствуют высокой ДНК-полимеразной активности и характеризуют активную репликацию вируса.
Наличие HBeAg в крови свидетельствует о высокой ее инфекциозности, т.е. присутствии в организме обследуемого активной инфекции гепатита В, и обнаруживается только в случае присутствия в крови HBs-антигена. У больных хроническим активным гепатитом противовирусные препараты применяются только при обнаружении в крови HBeAg. HBeAg – антиген – маркер острой фазы и репликации вируса гепатита В.
Исследование крови на наличие HBe-антигена применяется для диагностики:
Оценка результатов исследования
Результат исследования выражается качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие HBeAg в сыворотке крови. Положительный результат – выявление HBeAg свидетельствует об инкубационном или остром периоде острого вирусного гепатита В или продолжающейся репликации вируса и инфекциозности больного.
Анти-HBeAg в сыворотке в норме отсутствует. Появление анти-НВeAg антител указывает обычно на интенсивное выведение из организма вируса гепатита В и незначительное инфицирование больного.
Эти антитела появляются в острый период и сохраняются до 5 лет после перенесенной инфекции. При хроническом персистирующем гепатите анти-НВeAg обнаруживаются в крови больного вместе с НВsAg. Сероконверсия, т.е. переход HBeAg в анти-НВeAg, при хроническом активном гепатите, чаще прогностически благоприятна, но такая же сероконверсия при выраженной цирротической трансформации печени прогноза не улучшает.
Исследование крови на наличие анти-НВeAg применяются в следующих случаях при диагностике вирусного гепатита В:
Оценка результатов исследования
Результат исследования выражается качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие антител к HBeAg в сыворотке крови. Положительный результат – выявление антител к HBeAg, которые могут свидетельствовать о начальной стадии острого вирусного гепатита В, остром периоде инфекции, ранней стадии реконвалесценции, реконвалесценции, перенесенном недавно вирусном гепатите В или персистирующем вирусном гепатите В.
Критериями наличия хронического гепатита В являются:
Обнаружение вируса гепатита В методом ПЦР (качественно)
Вирус гепатита В в крови в норме отсутствует.
Качественное определение вируса гепатита В методом ПЦР в крови позволяет подтвердить наличие вируса в организме больного и тем самым устанавливает этиологию заболевания.
Данное исследование дает полезную информацию для диагностики острого вирусного гепатита В в инкубационном и раннем периоде развития заболевания, когда основные серологические маркеры в крови у пациента могут отсутствовать. Вирусную ДНК в сыворотке крови обнаруживают у 50% больных при отсутствии HBeAg. Аналитическая чувствительность метода ПЦР составляет не менее 80 вирусных частиц в 5 мкл, прошедшей выявление ДНК пробы, специфичность – 98%.
Этот метод имеет важное значение для диагностики и мониторинга течения хронического ВГВ. Примерно 5-10% случаев цирроза и других хронических заболеваний печени обусловлены хроническим носительством вируса гепатита В. Маркерами активности таких заболеваний является наличие HBeAg и ДНК вируса гепатита В в крови.
Метод ПЦР позволяет определять в крови ДНК вируса гепатита В как качественно, так и количественно. Определяемым фрагментом в обоих случаях служит уникальная последовательность ДНК гена структурного белка вируса гепатита В.
Обнаружение ДНК вируса гепатита В в биоматериале с помощью ПЦР необходимо для:
Исчезновение ДНК вируса гепатита В из крови – признак эффективности терапии
Обнаружение вируса гепатита В методом ПЦР (количественно)
Этот метод дает важную информацию об интенсивности развития заболевания, об эффективности лечения и о развитии резистентности к активным препаратам.
Для диагностики вирусного гепатита методом ПЦР в сыворотке крови применяются тест-системы, чувствительность которых составляет 50-100 копий в пробе, что позволяет детектировать вирус при его концентрации 5 Х 10^3 -10^4 копий/мл. ПЦР при вирусном гепатите В безусловно необходима для суждения о вирусной репликации.
Вирусную ДНК в сыворотке крови обнаруживают у 50% больных при отсутствии HBeAg. Материалом для выявления ДНК вируса гепатита В могут служить сыворотка крови, лимфоциты, гепатобиоптаты.
- Оценку уровня виремии осуществляют следующим образом:
- менее 2.10^5 копий/мл (менее 2.10^5 МЕ/мл) – низкая виремия ;
- от 2.10^5 копий/мл (2.10^5 МЕ/мл) до 2.10^6 копий/мл (8.10^5 МЕ/мл) – средняя виремия;
- более 2.10^6 копий/мл – высокая виремия.
Существует зависимость между исходом острого вирусного гепатита В и концентрацией ДНК ВГВ в крови больного. При низком уровне виремии процесс хронизации инфекции близок к нулю, при средней – хронизация процесса наблюдается у 25-30% больных, а при высоком уровне виремии острый вирусный гепатит В чаще всего переходит в хронический.
Показаниями для лечения хронического ВГВ интерфероном-альфа следует считать наличие маркеров активной репликации вируса (выявление HBsAg, HBeAg и ДНК ВГВ в сыворотке крови в течение предшествующих 6 месяцев.).
Критериями оценки эффективности лечения служат исчезновение HBeAg и ДНК ВГВ в крови, что обычно сопровождается нормализацией уровня трансаминаз и долговременной ремиссией заболевания, ДНК ВГВ исчезает из крови к 5-му месяцу лечения у 60%, к 9-му месяцу – у 80% больных. Снижение уровня виремии на 85% и более к третьему дню от начала лечения по сравнению с исходным служит быстрым и достаточно точным критерием для прогнозирования эффективности терапии.
В образцах сыворотки крови пожилых пациентов с положительным, отрицательным и неопределенным результатом исследования в иммуноферментных тест-системах планшетного формата с раздельным определением антител к структурным (Core) и неструктурным (NS3, NS4, NS5) антигенам вируса гепатита С была исследована концентрация α-фетопротеина (АФП). Показано, что концентрация АФП повышена в пробах, содержащих антитела высокой оптической плотности к структурным и неструктурным антигенам ВГС, по сравнению с концентрацией АФП в пробах, результаты исследования которых в иммуноферментных тест-системах были противоречивыми и неопределенными, а также в пробах с антителами к ВГС низкой оптической плотности. В образцах сыворотки крови пожилых людей без антител к ВГС наблюдались значительные колебания концентрации АФП. Таким образом, в лабораторной диагностике гепатита С необходима комплексная оценка серологических и биохимических маркеров ВГС-инфекции с учетом возрастной категории пациента.

антитела к вирусу гепатита С; иммуноферментный анализ; неопределенные результаты; α-фетопротеин; пожилые пациенты
Выявление антител к вирусу гепатита С (анти-ВГС) в крови пациентов методом иммуноферметного анализа (ИФА), которое является первым шагом лабораторной диагностики ВГС-инфекции, наиболее эффективно при обследовании людей без иммунодефицитного состояния в фазу развернутой продукции антител. На раннем этапе заражения ВГС и после выздоровления [8], а также при патологических и физиологических, в частности, возрастных, иммунодефицитных состояниях результаты исследования анти-ВГС в ИФА могут быть позитивными, но с низкой оптической плотностью, или противоречивыми [6]. В то же время вследствие широкого распространения и социальной значимости ВГС-инфекции необходимость в правильной интерпретации результатов исследования возникает уже на этапе первичного скрининга. Развитие гепатита С сопровождается определенными биохимическими изменениями сыворотки крови, в частности, увеличением концентрации аланинаминотрансферазы и α-фетопротеина (АФП) [3, 9]. Некоторые из биохимических маркеров повреждения печени могут быть обнаружены в сыворотке крови с неопределенным результатом исследования анти-ВГС в иммуноблоте [5]. В РФ в качестве подтверждающих тест-систем используются не только иммуноблоты, но и тест-системы для ИФА (ИФТС) в планшетном формате с раздельным определением антител к ряду антигенов ВГС. Относительно биохимической характеристики сыворотки крови с неопределенным результатом исследования анти-ВГС в планшетных ИФТС в литературе имеются единичные данные [5].
Целью представленной работы было определение концентрации α-фетопротеина в сыворотке крови пациентов пожилого возраста с различным, в том числе неопределенным, результатом исследования анти-ВГС в подтверждающих тест-системах планшетного формата с раздельным определением антител к антигенам ВГС.
Материалы и методы
Результаты были получены при исследовании 82 образцов сыворотки крови пожилых людей, направленных на определение наличия в них маркеров вирусных гепатитов.
Полученные результаты
После исследования в образцах сыворотки крови наличия анти-ВГС были выделены следующие группы:
1) при отсутствии анти-ВГС в скрининговой тест-системе образцы были признаны не содержащими анти-ВГС (группа Анти-ВГС-);
2) при выявлении в первичной скрининговой и в подтверждающей тест-системе анти-ВГС с высокой оптической плотностью (ОП не менее 2,0, КП не менее 8) образцы были признаны анти-ВГС-содержащими (группа Анти-ВГС+).
Следующие две группы были выделены при дальнейшем исследовании позитивных образцов с низкой ОП в ИФТС для первичного скрининга (ОП менее 1,4, КП менее 5), а именно:
3) при выявлении анти-ВГС с низкой ОП и соответственно с низким КП в двух подтверждающих ИФТС разных производителей и определения низкой или высокой авидности анти-ВГС образцы признавались анти-ВГС-низкопозитивными (группа Анти-ВГС низк+);
4) при выявлении анти-ВГС только в одной из двух подтверждающих ТС либо при выявлении анти-ВГС в двух подтверждающих ТС разных производителей, но при отсутствии положительного результата в ЛИА и при определении авидности анти-ВГС, результат исследования анти-ВГС рассматривался как неопределенный в ИФТС, но отрицательный в ЛИА (группа Анти-ВГС но/-).
Группу Анти-ВГС- составили 16 образцов сыворотки крови пациентов (средний возраст 74,5 ± 7,45 лет), у которых отсутствовали указания на факторы высокого риска инфицирования ВГС. В группе анти-ВГС средняя величина концентрации АФП составляла 8,25 МЕ/мл (от 3,741 до 29,71 МЕ/мл, σ = 6,266 МЕ/мл).
Группу Анти-ВГС+ составили 30 образцов (средний возраст пациентов 73,6 ± 5,5 лет). Образец №8 был получен от пациента с заболеванием печени, образец №22 - от пациента с наркоманией. В 28 из 30 образцов в подтверждающей ТС были обнаружены анти-Core и анти-NS ВГС с ОП в первичной и подтверждающей ИФТС не менее 2, КП не менее 8. В образце №18 определялись только анти-Core с ОП 2,0 и КП 8,0, в образце №7 определялись только анти-NS с ОП 2,7 и КП 10,8. Во всех образцах данной группы анти-ВГС были высокоавидными. Средняя концентрация АФП в группе Анти-ВГС+ составляла 14,725 МЕ/мл (интервал от 3,804 до 111,815 МЕ/мл, σ = 22,02 МЕ/мл).
В группу Анти-ВГСнизк+ (11 образцов, средний возраст пациентов 71,5 ± 6,4 года) образцы были отобраны согласно ранее разработанному алгоритму: либо при обнаружении только анти-Core с КП менее 2; либо при обнаружении только анти-NS ВГС (табл. 1). Средняя величина КП анти-NS в каждой ИФТС не превышала 5, однако КП анти-NS в разных ИФТС могли отличаться (образец №2). В 8 из 11 образцов авидность анти-ВГС была высокой, в трех - низкой. В 6 из 11 образцов были обнаружены только высоко- или низкоавидные анти-NS4 ВГС. Указаний на наличие факторов высокого риска инфицирования ВГС не было ни у одного пациента. Среднее значение концентрации АФП в группе анти-ВГСнизк+ было равно 7,045 МЕ/мл (от 4,06 до 24,06 МЕ/мл; σ = 5,773 МЕ/мл).
Результаты исследования 25 образцов (средний возраст пациентов 75,4 ± 7,0 лет) в ИФТС планшетного формата были противоречивыми (табл. 2). Из 25 образцов в двух (№3 и №18) были обнаружены высокоавидные анти-ВГС, в шести образцах (№№ 1, 2, 6, 9, 16, 19) авидность анти-ВГС была низкой. Все вышеперечисленные образцы в ИФТС другого производителя и в ЛИА были определены как анти-ВГС-негативные (группа Анти-ВГСно/-). Средняя величина концентрации АФП в образцах Анти-ВГСно/- была равна 11,187 МЕ/мл (от 2,941 до 83,16 МЕ/мл, σ = 16,642 МЕ/мл).
При сравнении сывороточной концентрации АФП по критерию Манна-Уитни было обнаружено, что группа образцов, не содержащих анти-ВГС, не отличается ни от одной из исследованных групп. Различия по концентрации АФП были обнаружены:
1) между группами Анти-ВГС+ и Анти-ВГСнизк+ (p = 0,024);
2) между группами Анти-ВГС+ и Анти-ВГСно/- (p = 0,045).
У пациентов пожилого возраста в г. Москве инфицирование вирусом гепатита С является наиболее частой причиной хронического гепатита (69,3% больных) [2]. При инфицировании ВГС в возрасте старше 50 лет цирроз печени формируется вдвое быстрее, чем у лиц, инфицированных до 50 лет. Осложнения ВГС-инфекции выявляются у пожилых в основном в далеко зашедших формах вследствие того, что длительная бессимптомная персистенция вируса и стертые клинические проявления заболевания приводят к позднему обращению больных к врачу [2]. Повышение специфичности лабораторной диагностики ВГС-инфекции как на раннем этапе инфицирования, так и при возрастной недостаточности иммунного ответа возможно при расширенных исследованиях анти-ВГС-позитивных образцов с низкой ОП в ИФА. Сравнивая результаты исследования проб пожилых людей с ранее полученными результатами исследования проб молодых мужчин [5], можно отметить следующее. Из общего количества образцов с неопределенными результатами исследования в ИФТС позитивными при дальнейшем исследовании признается не более 1/3 как в группе молодых мужчин, так и людей старше 65 лет. Различия между группами проявились, во-первых, в спектре выявляемых антител. В пробах, полученных от пожилых людей, в ИФТС с низкой ОП могли определяться анти-NS3, -NS4 и -NS5 раздельно и в различных сочетаниях; в ИБ/ЛИА наличие анти-ВГС в пробах данной подгруппы не подтверждалось. В пробах, полученных от молодых мужчин, практически во всех образцах с неопределенным результатом исследования анти-ВГС в ИФТС выявлялись только анти-NS4 ВГС; в дальнейших исследованиях в иммуноблоте наличие анти-ВГС не подтверждалось. Во-вторых, различие между группами выявилось по авидности антител: анти-NS4 у пожилых пациентов могли быть как высоко-, так и низкоавидными, а при обнаружении в пробе молодого пациента только анти-NS4 авидность антител не определялась. В-третьих, согласно нашим данным, изменение концентрации АФП в зависимости от результата тестирования анти-ВГС (позитивного, негативного и неопределенного) в группах проб молодых и пожилых пациентов было различным. Концентрация АФП в анти-ВГС-негативных образцах сыворотки крови молодых мужчин была ниже, чем в анти-ВГС-позитивных образцах и в образцах с неопределенными в ИФТС и неотрицательными в иммуноблоте результатами. В двух последних подгруппах концентрация АФП не различалась [5], что подтверждает вывод Rios [10] об эпидемиологической близости групп с анти-ВГС-позитивными и неопределенными результатами. В отличие от этого, группа образцов пожилых людей с отрицательными результатами тестирования анти-ВГС была крайне гетерогенной по концентрации АФП, по-видимому, вследствие разнообразных приобретенных заболеваний и наличия иных, кроме ВГС, гепатотоксических факторов, вследствие чего не отличалась ни от одной из исследованных групп по концентрации АФП. Отмеченное превышение сывороточной концентрации АФП в анти-ВГС-высокопозитивных образцах над концентрацией АФП в анти-ВГС-низкопозитивных образцах может быть обусловлено длительностью инфекционного процесса, в течение которого наиболее выраженное повышение уровня АФП наблюдается на стадии тяжелого фиброза с последующим снижением при трансформации в цирроз печени (частом осложнении хронического гепатита С у пожилых людей) [3]. Кроме того, в низкопозитивных на наличие анти-ВГС-образцах отсутствие подъема концентрации АФП может быть обусловлено начальным этапом инфекционного процесса (с анти-ВГС низкой авидности) либо выздоровлением (с остаточными анти-ВГС высокой авидности) с нормализацией биохимических показателей. Образцы с противоречивыми в ИФТС, но отрицательными в иммуноблоте и в тесте на авидность результатами, по-видимому, проявляли в ИФТС ложную позитивность.
Таблица 1
Концентрация α-фетопротеина в образцах сыворотки крови пожилых людей,
содержащих высоко- и низкоавидные анти-ВГС (соответственно ВА и НА)
с низким коэффициентом позитивности (значение КП указано).
Антитела к вирусу гепатита С в сыворотке в норме отсутствуют
Суммарные антитела к вирусу гепатита С представляют собой антитела классов IgM и IgG, направленные к комплексу структурных и неструктурных белков вируса гепатита С.
Это исследование является скрининговым для выявления пациентов с ВСГ. Суммарные антитела к вирусу гепатита С можно выявить в первые 2 недели заболевания, и их присутствие свидетельствует о возможной инфицированности вирусом или перенесенной инфекции.
Однозначный ответ на основании результатов данного теста получить невозможно, так как тест определяет суммарные антитела IgM и IgG. Если это ранний период острого вирусного гепатита С, то об этом свидетельствуют антитела IgM, а если это период реконвалесценции или состояние после перенесенного ВГС, то на это указывают антитела IgG.
Оценка результатов исследования
Результат исследования выражается качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие суммарных антител (JgM и JgG) к ВГС в сыворотке крови. Положительный результат – выявление суммарных антител (JgM и JgG) к ВГС свидетельствует о начальной стадии острого вирусного гепатита С, остром периоде инфекции, ранней стадии реконвалесценции, перенесенном вирусном гепатите С или хроническом вирусном гепатите С.
Однако обнаружение суммарных антител к ВГС недостаточно для постановки диагноза ВГС и требует подтверждения для исключения ложноположительного результата исследования. Поэтому при получении положительного результата скринингового исследования на суммарные антитела к ВГС в лаборатории проводится подтверждающий тест. Окончательный результат определения суммарных антител к ВГС выдается совместно с результатом подтверждающего теста.
Антитела к вирусу гепатита С JgM
Антитела к вирусу гепатита С JgM в сыворотке в норме отсутствуют. Наличие антител класса JgM к ВГС в крови пациента позволяет верифицировать активную инфекцию. Антитела класса JgM могут выявляться не только при остром ВГС, но и при хроническом гепатите С.
Антитела класса JgM к ВГС появляются в крови пациента спустя 2 недели после развития клинической картины острого вирусного гепатита С или обострения хронического гепатита и обычно исчезают спустя 4-6 месяцев. Снижение их уровня может свидетельствовать об эффективности лекарственной терапии.
Оценка результатов исследования
Результат исследования выражается качественно – положительный или отрицательный. Отрицательный результат исследования указывает на отсутствие антител JgM к ВГС в сыворотке крови. Положительный результат – выявление антител JgM к ВГС свидетельствует о начальной стадии острого вирусного гепатита С, остром периоде инфекции, ранней стадии реконвалесценции или активном хроническом вирусном гепатите С.
Обнаружение вируса гепатита С методом ПЦР (качественно)
Вирус гепатита С в крови в норме отсутствует.
В отличие от серологических методов диагностики ВГС, где обнаруживают антитела к ВГС, ПЦР позволяет выявить наличие непосредственно РНК ВГС в крови как качественно, так и количественно. Определяемым фрагментом в обоих служит консервативный участок генома гепатита С.
Обнаружение только антител к ВГС подтверждает лишь факт инфицирования пациента, но не позволяет судить об активности инфекционного процесса (о репликации вируса), о прогнозе заболевания. Кроме того, антитела к вирусу ГС обнаруживают как в крови больных острым и хроническим гепатитом,так и у тех пациентов, кто болел и выздоровел, а нередко антитела в крови появляются только спустя несколько месяцев после появления клинической картины заболевания, что затрудняет диагностику. Обнаружение вируса в крови методом ПЦР – более информативный метод диагностики.
Качественное выявление ВГС методом ПЦР в крови свидетельствует о виремии, позволяет судить о размножении вируса в организме и является одним из критериев эффективности противовирусной терапии.
Аналитическая чувствительность метода ПЦР составляет не менее 50-100 вирусных частиц в 5 мкл, прошедшей выделение ДНК-пробы, специфичность – 98%. Обнаружение РНК вируса гепатита С с помощью ПЦР на ранних этапах развития вирусной инфекции (возможно уже через 1-2 недели после заражения) на фоне полного отсутствия каких-либо серологических маркеров может служить самым ранним свидетельством инфицирования.
Однако изолированное выявление РНК вируса гепатита С на фоне полного отсутствия каких-либо других серологических маркеров не может полностью исключить ложноположительный результат ПЦР. В таких случаях требуется всесторонняя оценка клинических, биохимических и морфологических исследований и повторное неоднократное подтверждение наличия инфекции ПЦР.
Согласно рекомендациям ВОЗ для подтверждения диагноза вирусного гепатита С необходимо троекратное выявление РНК вируса гепатита С в крови пациента.
Обнаружение РНК вируса гепатита С методом ПЦР используется в целях:
Обнаружение вируса гепатита С методом ПЦР (количественно)
Количественный метод определения содержания РНК вируса гепатита С в крови дает важную информацию об интенсивности развития заболевания, об эффективности лечения и о развитии резистентности к антивирусным препаратам. Аналитическая чувствительность метода составляет от 5.102 копий/мл вирусных частиц в сыворотке крови, специфичность – 98%.
Уровень виремии оценивают следующим образом: при содержании РНК ВГС от 10^2 до 10^4 копий/мл – низкий; от 10^5 до 10^7 копий/мл – средний и выше 10^8 копий /мл – высокий.
Количественное определение содержания РНК ВГС в сыворотке крови методом ПЦР имеет важное значение для прогноза эффективности лечения интерфероном-альфа. Показано, что наиболее благоприятный прогноз заболевания и наибольшую вероятность положительного ответа на противовирусную терапию имеют лица с низким уровнем виремии. При эффективном лечении уровень виремии снижается.
Генотипирование вируса гепатита С - определение генотипа
Метод ПЦР позволяет не только выявить РНК ВГС в крови, но и установить его генотип. Наиболее важное значение для клинической практики имеют 5 субтипов ВГС – 1а, 1b, 2а, 2b и 3а. В нашей стране наиболее часто встречается субтип 1b, далее идут 3а, 1а, 2а.
Определение генотипа (субтипа) вируса имеет важное значение для прогноза течения ВГС и подбора пациентов с хроническим ВГС к проведению лечения интерфероном-альфа и рибавирином.
При инфицировании пациента субтипом 1b хронический ВГС развивается примерно в 90% случаев, при наличии субтипов 2а и 3а – в 33-50%. У пациентов с субтипом 1b заболевание протекает в более тяжелой форме и часто заканчивается развитием цирроза печени и гепатоцеллюлярной карциномы. При инфицировании субтипом 3а у больных более выражен стеатоз, поражение желчевыводящих путей, активность АЛТ и менее выражены фиброзные изменения в печени, чем у пациентов с субтипом 1b.
Показаниями к лечению хронического ВГС интерфероном–альфа являются:
При лечении интерфероном-альфа больных вирусным гепатитом С с субтипом 1b эффективность терапии отмечается в среднем в 18% случаев, у инфицированных другими субтипами – в 55%. Использование комбинированной схемы лечения (интерферон-альфа + рибавирин) повышает эффективность терапии. Стойкий ответ наблюдается у 28% больных с субтипом 1b и у 66% - с другими субтипами ВГС.
Этиология. Вирус гепатита С (Hepatitis С Virus, HСV) — РНК содержащий вирус, относится к семейству Flaviviridae. Является наиболее частым возбудителем трансмиссивных гепатитов в мире: причиной примерно 20% случаев острого гепатита, 60–70% хронического гепатита и примерно 30% цирроза и рака печени. На сегодняшний день известно 11 генотипов вируса и более 100 его субтипов. Термин «генотип " имеет отношение к генетическому строению вируса: по общепринятой классификации генотип обозначается числом, а подтип маленькой буквой латинского алфавита. Генотипирование необходимо проводить для определения прогноза заболевания, эффективности противовирусной терапии и определения продолжительности курса терапии. У пациентов с генотипом 1b хронизация происходит в 90% случаев, в то время как с генотипами 2а и 3а в 33–50%. Инфицирование генотипом 1b сопровождается более тяжелым течением заболевания, развитием цирроза печени и гепатоцеллюлярной карциномы. Пациенты с генотипом 3a имеют более выраженный стеатоз и поражения желчевыводящих путей, а также более высокий уровень АЛТ, чем пациенты с HCV генотипа 1b. При этом уровень фиброза более выражен у пациентов с вирусом генотипа 1b. При монотерапии интерфероном устойчивый ответ наблюдается у 18% пациентов, инфицированных HCV генотипом 1b, и у 55% — инфицированных другими генотипами. При комбинированной схеме лечения интерферон+рибаверин стойкий ответ наблюдается у 28% пациентов, инфицированных HCV генотип 1b и у 66% пациентов, инфицированных другими генотипами.
Эпидемиология. Вирус гепатита С (HСV) передается преимущественно парентеральным путем, причем процент случаев инфицирования ВГС выше среди пациентов, перенесших трансплантацию органов, гемотрансфузию, получающих множественные внутривенные инъекции (наркоманы) а также у находящихся на почечном диализе. До годов — максимальное количество заражений происходило при гемотрансфузии. Передача от матери к плоду случается достаточно редко (2,7–4,4%.), однако риск увеличивается в случае, если мать ВИЧ инфицирована (5,4–8,6%). Половой путь передачи встречается крайне редко. Однако, в 30% случаев причина заражения остается не ясной. Кроме того, необходимо учитывать, что вирус может присутствовать в таких биологических жидкостях как слюна, молоко, влагалищные выделения, сперма. Инфицирование вирусом гепатита С может завершиться полной элиминацией вируса с формированием иммунного ответа, но в большинстве случаев этого не происходит (50% — 90%) и развивается хроническая прогрессирующая инфекция, которая может приводить к циррозу с высоким риском развития гепатоцеллюлярной карциномы. Факторами, предрасполагающими к более тяжелому течению заболеванию является генотип 1 вируса, мужской пол, злоупотребление алкоголем и наличие .
Клинические проявления. Инкубационный период составляет 1–6 месяцев, острый период в 75% случаев протекает бессимптомно, в безжелтушной форме и поэтому часто не диагностируется на этом этапе.
Диагностика
Лабораторная диагностика вирусного гепатита С основывается на:
- методах непрямого выявления вируса — выявление серологических маркеров (антител к антигенам вируса). Данные методы позволяют устанавливать инфицирование вирусом, оценивать наличие защитного иммунитета, дифференцировать стадии заболевания, выявлять окончание репликации вируса;
- методах прямого выявления вируса: выявление РНК вируса в исследуемом биологическом материале методом ПЦР. Данные методы позволяют не только установить этиологию, но и оценить активность вируса — выявить репликативную стадию, установить генотип вируса.
Серологическая диагностика. Антитела класса М появляются через 4–6 недель после инфицирования, и сохраняются до 5–6 месяцев при первичном инфицировании. Уровень IgM может повышаться вновь во время следующей реактивации инфекции.
Антитела класса G появляются с 11–12 недели после инфицирования, достигают пика концентрации к 5–6 месяцу и сохраняются в крови на постоянном уровне в течение всего периода болезни и реконвалесценции, затем снижаются и могут сохраняться на минимальном уровне пожизненно. В некоторых случаях полностью исчезают. Ложноотрицательные результаты выявления антител могут быть у пациентов с ослабленным иммунитетом (), пациентов с почечной недостаточностью, при эссенциальной смешанной криоглобулинемии. Ложноположительные результаты могут наблюдаться при аутоиммунных заболеваниях (в 80% случаев — аутоиммунный хронический активный гепатит), узелковом полиартериите, наличии ревматоидного фактора, гипергаммаглобулинемии, парапротеинемии, пассивной передаче антител. Выявление антител не позволяет определить различия между текущей инфекцией и перенесенной инфекцией. В случае получения положительного результата требуется подтверждение другим методом из другого образца. В случае получения отрицательного результата серологических маркеров, но наличии клинических данных за возможное наличие HCV инфекции, необходимо проведение молекулярных методов выявления РНК вируса для подтверждения или исключения диагноза активной инфекции гепатита С. РНК вируса гепатита С выявляется в крови уже через 5 дней после инфицирования, задолго до появления антител к гепатиту С.
Молекулярные методы выявления вируса гепатита С позволяют выявить РНК в качественном (обнаружено/не обнаружено) формате, количественном (не обнаружено/обнаружено в количестве) формате, определить генотип вируса. Каждый формат позволяет решить определенные диагностические задачи. Выявление РНК вируса в качественном формате позволяет выявить репликативную стадию вируса и ответить на вопрос о активности: данное исследование проводится пациентам как с серопозитивными результатами, так и серонегативными, когда данный метод позволяет установить этиологию гепатита.
Изучение генотипа необходимо для определения прогноза заболевания. Кроме того, существуют данные о том, что преимущественный путь передачи так же зависит от генотипа вируса. Считается, что тип 1в более характерен для трансфузионного пути передачи, а 1а и 3а — при употреблении наркотиков. Кроме того, тип вируса имеет прогностическое значение для прогноза эффективности терапии и оценки длительности.
Решение о схеме лечения основывается на первоначальной вирусной нагрузке и генотипе вируса. Длительность терапии зависит от 4 факторов — начальной вирусной нагрузки, динамики снижения виремии, времени достижения нулевой вирусной нагрузки и развития фиброза.
При инфицировании генотипом 2 или 3 продолжительность терапии составляет не менее 24 недель с вероятностью формирования стойкого вирусологического ответа около 70%. При инфицировании вирусом первого генотипа (а также и 4, 5 или 6) продолжительность терапии должна составлять не менее 48 недель и вероятность стойкого вирусологического ответа колеблется в районе 45%. При наличии 1, 4, 5 или 6 генотипов обязательно необходимо определять показатель вирусной нагрузки перед стартом терапии. Вирусная нагрузка менее 400 000 МЕ/мл считается низкой, более 400 000 МЕ/мл — высокой. Необходимо повторить определение ВН через 12 недель терапии. В случае, если снижение показателя составляет не менее 2 логарифмов терапию продолжают до 72 недель. Если же ВН не снижается на 2 логарифма и более — лечение прекращают в связи с недостаточным вирусологическим ответом. Целью терапии является достижение неопределимой вирусной нагрузки, что должно быть подтверждено через 6 месяцев после окончания терапии.
Другой алгоритм принятия решения основан на времени достижения вирусологического ответа вне зависимости от генотипа вируса. Отсутствие снижения уровня вирусной нагрузки как минимум на 1 lg после недель терапии расценивается как нулевой ответ и терапия прекращается. В случае получения неопределяемого уровня вирусной нагрузки, эффект расценивается как быстрый вирусологический ответ. В данном случае при низкой первичной вирусной нагрузке срок терапии может быть сокращен, а при высокой — терапия должна быть продолжена до 48 недель. При достижении неопределяемой вирусной нагрузки к 12 неделе терапии, эффект расценивается как ранний вирусологический ответ и терапия продолжается до 48 недель. Определяемая вирусная нагрузка на 12 неделе лечения со снижением как минимум на 2 lg к первичной, свидетельствует о медленном вирусологическом ответе и терапия продолжается до 72 недель.
Алгоритмы обследования и интерпретации полученных результатов:

Оборудование: Fibroscan® 502 Touch
Что такое эластометрия или эластография печени?
Эластометрия (эласторафия) или как еще называют фибросканирование печени — современный, неинвазивный, без хирургического вмешательства, метод диагностики степени фиброза и степени жирового гепатоза, стеатоза печени. В отличии от биопсии, эластометрия (эластография) печени позволяет проводить исследование всего органа, а не отдельно взятого фрагмента, что обеспечивающий высокую достоверность результатов обследования методом эластометрии.
Эластометрия печени - цены на обследование:
Степень жирового гепатоза
Консультация по результатам
по АКЦИИ ! (Москва, метро Парк культуры)
- с 9:00 до 17:30 по будням
- с 9:00 до 15:00 в субботу
Для чего необходима эластометрия печени?
Обследование печени на аппарате Фиброскан позволяет, достоверно определить степень поражения печени, а именно - степень фиброза и степень жирового гепатоза, без хирургического вмешательства. Полученные данные о состоянии печени пациента дают возможность врачу-гепатологу поставить точный диагноз и выбрать правильную тактику лечения, или скорректировать при необходимости ранее назначенное лечение. Чем раньше поставлен точный диагноз и начато правильное лечение, тем выше шанс сохранить здоровую печень.
Как подготовиться к эластометрия печени:
- для обследования на аппарате Фиброскан (эластометрия/эластография) никакой специальной подготовки не требуется.
- для УЗИ печени рекомендуется проходить обследование натощак. Воду пить можно. Голодный промежуток должен составлять не менее 4 часов.
ВНИМАНИЕ. Эластометрия / эластография печени проводится на аппарате Фиброскан последнего поколения - FibroScan® 502 Touch.
Новый Фиброскан дает возможность отдельно определять степень фиброза печени и отдельно степень жирового гепатоза (стеатоза печени). Новые возможности диагностики состояния печени позволяют врачу учесть все факторы и назначить наиболее эффективное лечения.
Заболевания печени, в том числе и хронические вирусные гепатит В и гепатит С сопровождаются прогрессирующим нарастанием фиброза печени, что в исходе заболевания приводит к циррозу — не обратимым изменениям печени с высоким риском летальных осложнений, включая первичный рак печени. Вот почему при вирусных гепатитах необходимо как можно раньше пройти обследование.
Кому необходима эластометрия (эластография) - обследование на аппарате Фиброскан
1. Эластометрия в качестве профилактического обследования может быть рекомендована всем, кто старше 40 лет.
2. Обязательное обследование на аппарате Фиброскан для оценки степени поражения печени должно проводиться при любых заболеваниях печени:
- Вирусные гепатиты В, С, D.
- Жировой гепатоз – неалкогольный стеатогепатит.
- Алкогольная болезнь печени - алкогольный стеатогепатит.
- Аутоиммунные заболевания печени (аутоиммунный гепатит, первичный билиарный цирроз и другие).
- Синдром Жильбера и другие наследственные заболевания печени.
3. При высоком риске поражения печени необходимо проводить эластометрию (эластографию) у пациентов:
- с сахарным диабетом,
- при повышенном уровне холестерина или триглицеридов,
- с превышением нормы показателей цитолиза (АЛТ, АСТ, ГГТ),
- при нарушениях в клиническом анализе крови (снижение уровня лейкоцитов и тромбоцитов),
- при избыточном весе,
- при частом повышении уровня билирубина в крови.
- при подозрении на цирроз или при установленном циррозе.
Эластометрия печени может выявить патологии в ранней форме у тех, кто употребляет алкоголь и принимает препараты, токсичные для печени.
Оценка состояния по данным эластометрии печени должна проводиться до начала лечения и после курса терапии. При высокой степени поражения печени (F3-F4) снижение показателей фиброза печени наблюдается в течение длительного времени (несколько лет), поэтому после курса терапии необходим постоянный контроль.
Преимущества метода эластометрии / эластографии печени
Главное преимущество эластометрии печени перед другими методами исследования - наибольшая информативность и безболезненность.
До недавнего времени единственным способом оценки фиброза печени была биопсия (хирургическое вмешательство). На основе гистологического обследования биоптата, взятого из печени с помощью специальной пункционной иглы под местной анестезией хирургическим путем, патологоанатом устанавливает индекс фиброза. Степень фиброза печени от 0 до 4 баллов (по Метавир) соответствует стадии поражения печени: 0 — отсутствие фиброза, 4 — цирроз печени.
При этом заключение патологоанатома основано на изучении очень небольшого участка печеночной ткани и не всегда соответствует реальному состоянию печени в целом. Кроме того, оценка степени фиброза субъективна и зависит от квалификации и опыта патологоанатома, а, значит, точность и воспроизводимость обследования может вызывать сомнения. У биопсии есть и другие ограничения по применению: физический и психологический дискомфорт пациента, значительная болезненность и крайне редкие, но тем не менее возможные случаи летального исхода.
Эластометрия/эластография – не единственный метод, дающий информацию о степени поражения печени, однако самый достоверный. В тех случаях, когда у пациента лишний вес и из-за большой жировой прослойки, невозможно технически провести исследования на Фиброскане, проводится исследование "Фибротест" – оценка степени фиброза печени по косвенным биохимическим показателям крови.
Как проводится эластометрия (эластография) печени?
Эластометрия печени - современная не травмирующая методика, позволяет в течение 5-10 минут установить степень фиброза печени (по Метавир) по измерению эластичности печеночной ткани. Эластичность (плотность) печени — это точный физический параметр, выраженный в килоПаскалях (кПа). Измерения производятся в десятках точек, что увеличивает возможность оценить более значительную область. Степень эластичности, отражающую степень фиброза, определяется прибором без участия исследователя, что исключает субъективные ошибки (человеческий фактор) при оценке результата. Простота и комфортность обследования для пациента делает эту процедуру такой же доступной, как обследование с помощью УЗИ. Соответствие результатов, полученных при эластометрии, степени фиброза, результатам полученным при гистологическом обследовании (биопсии), было доказано на тысячах пациентов.
Возможность быстро, объективно и комфортно для пациента определять степень фиброза значительно расширяет возможности диагностики состояния печени при вирусных гепатитах. Более точная оценка состояния печени позволяет вовремя принимать решения о начале противовирусной терапии и более объективно оценивать ее результаты. Очень важно также отметить, что обычные стандартные обследования печени — биохимические (АЛТ, АСТ) и УЗИ не всегда реально соответствуют степени выраженности фиброза. Достаточно часто нормальные показатели могут быть и при высокой степени фиброза. В таких случаях неправильно принятые решения об отказе в лечении могут приводить к быстрому формированию цирроза.
Таким образом, эластометрия / эластография печени позволяет:
- Быстро оценить степень поражения печени
- Быстро принять решение о назначении противовирусной терапии при вирусных гепатитах
- Контролировать безопасность терапии и оценивать её эффективность
О чем говорят результаты фибросканирования печени?
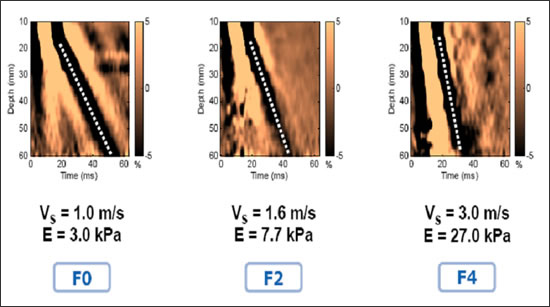
Результаты фибросканирования печени — по результатам эластометрии диагностируются следующие состояния:
F0 здоровая печень
F1 — F3 степени фиброза
F4 цирроз печени
Основная цель лечения вирусных гепатитов — это борьба с формирующимся циррозом. Именно поэтому так важно иметь возможность точно и доступно оценить степень фиброза до лечения, в процессе лечения и после лечения. Оценка эластичности печеночной ткани на аппарате Фиброскан (FibroScan) дает такую возможность врачу, а главное — пациенту.
Читайте также:

