Вирус не попал в резервуары
Обновлено: 26.04.2024
Новосибирск. 19 февраля. ИНТЕРФАКС - Международная группа ученых выяснила, почему летучие мыши не погибают от вирусных инфекций, оставаясь их носителями на протяжении своей жизни, сообщает издание Сибирского отделения РАН "Наука из первых рук".
"При этом некоторые из них доживают до 40 лет, тогда как грызуны того же размера живут всего около двух лет", - отмечает издание.
Исследование проводили американские и китайские ученые в Калифорнийском университете.
Известно, что от летучих мышей произошла передача человеку вирусов лихорадки Эбола и Марбург, SARS (атипичная пневмония, 2002-2003 гг.) и MERS (ближневосточный респираторный синдром, 2012-2015 гг.), и, вероятно, нового коронавируса Covid-2019.
Ученые установили, что летучие мыши "научились" эффективно избавляться от свободных радикалов, которые образуются при воспалительной реакции в ответ на вирусное заражение, протекающей у них гораздо слабее, чем у людей или других животных. При этом ключевой является особенность иммунной системы летучих мышей, которая в ответ на атаку вируса обеспечивает быстрое и активное высвобождение молекул интерферона - белка, отвечающего за противовирусный ответ.
Исследователи провели эксперименты на культурах клеток двух представителей летучих мышей и для сравнения обезьяны. "Они увидели, как в клетках нильского крылана (Rousettus aegyptiacus), природного хозяина вируса Марбург, и бавеанской летучей лисицы (Pteropus alecto), являющейся резервуаром вируса Хендра, молекулярные системы, отвечающие за синтез интерферона, находятся "в боевой готовности", и при вирусной атаке развивается очень быстрый интерфероновый ответ", - отмечает издание.
В то же время клетки африканской зеленой мартышки (Chlorocebus aethiops) вообще не продуцировали интерферон в этих опытах. Соответственно, при заражении клеточной культуры вирусами клетки зеленой мартышки были быстро уничтожены ими, в то время как клетки рукокрылых успешно "отгородились" от инфекции благодаря интерферону.
Благодаря интерфероновой защите клеток вирусная инфекция не "разгорается", а "тлеет" и может сохраняться в организме летучей мыши на протяжении всей ее жизни, что делает этих животных уникальным резервуаром быстро размножающихся вирусов. И когда вирус передается от летучих мышей к животным, иммунная система которых не умеет реагировать быстро и эффективно, вирус, "привыкший" к активному сопротивлению, оказывается смертельно опасным.
Согласно публикации, многие вирусы летучих мышей перешли к человеку не непосредственно, а через других животных: SARS попал к людям через малайскую пальмовую куницу; MERS - через верблюдов, Эбола - через горилл и шимпанзе, Нипах - через свиней, Хендра - через лошадей, Марбург - через африканских зеленых мартышек.
Кроме того, исследователи отмечают, что нарушение среды обитания летучих мышей, по-видимому, вызывает у животных стресс, что приводит к усиленному выделению вирусов. Поэтому экологические угрозы летучим мышам могут усилить вирусную угрозу для других животных и человека.
В настоящее время ученые работают над созданием компьютерных моделей развития вирусных болезней у летучих мышей, чтобы научиться прогнозировать возникновение их новых форм и распространение на другие виды.
Вирус SARS-CoV-2, вызвавший пандемию, вероятнее всего, попал к нам от летучих мышей с помощью посредничества другого животного — панголина. Подобное уже не раз происходило: вирус преодолевал межвидовой барьер, находил подход к человеку, а потом распространялся в человеческой популяции, провоцируя вспышки и эпидемии.
Вирусы-специалисты
Как называются общие для человека и животных болезни?
Зоонозные инфекции — то, чем вы сможете заразиться от животных. Пример зооноза, которым я сама в детстве переболела, — орнитоз. Инфекцию переносят птицы. В детстве мы постоянно возились с голубями. Однажды после этого у меня поднялась температура. Градусник два дня показывал почти 42 градуса. Поскольку все мое поведение было как на ладони, врачи быстро установили причину болезни.
Антропозоонозы — болезни, которыми мы заражаемся от животных и дальше начинаем передавать друг другу. То есть SARS-CoV-2, возбудитель COVID-19, — это типичный антропозооноз.
Сколько людей ежегодно болеют и погибают от инфекций, пришедших к нам от животных?
Порядка 2 миллионов человек погибают от зоонозов каждый год. Соответственно, болеют еще больше. Эта цифра всплывает много где, но оригинального источника я не нашла.
С какими зоонозными инфекциями мы постоянно имеем дело?
Есть болезни, которые настолько давно с нами, что мы уже забыли, что они перешли к нам от животных. Например, корь, которая сейчас возвращается. Она пришла к нам примерно 15 тысяч лет назад. В тот период человек одомашнивал крупный рогатый скот, у которого была болезнь — бычья чума. Благодаря удачной мутации вирус смог перескочить на человека, и в виде кори нигде, кроме как у людей, уже не встречается, то есть стал антропонозом.
Вирус герпеса — наш спутник уже не один миллион лет. Мы еще были совсем обезьяноподобные, а вирус герпеса уже жил в нас, ловко прятался в нервных клетках, вел себя достаточно деликатно, чтобы не убивать своих носителей, и из-за этого получал дополнительные возможности для распространения в популяции.
Люди, вероятно, подцепили герпес от какого-то другого вида приматов: у многих видов обезьян свои вирусы герпеса. Например, у азиатских обезьян есть вирус обезьяньего герпеса, который для людей смертелен почти в 80%.
То есть были вспышки среди людей?
Были единичные случаи заражения. Например, в прошлом веке исследовательница погибла после того, как обезьянья жидкость попала ей на слизистую глаза. Поднялась паника, потому что с лабораторными животными ученые постоянно свободно контактируют. Колония макак в одном из питомников после была уничтожена из-за подозрения, что они могут быть носителями вируса.
Обычно думаешь, что заразиться можно от диких видов, а тут лабораторные животные.
Вирусное комбо
Антропозоонозных болезней много, но эпидемии вызывают не все. От чего это зависит?
Обычно большой шорох возникает, когда появляется заболевание с высокой летальностью, как было, например, с Эболой. Это геморрагическая лихорадка, у нее есть чуть менее известные родственники — лихорадки Марбург и Ласса. Их переносят африканские рукокрылые. Симптоматика страшно тяжелая — высокая температура, рвота, диарея, кровотечения, при этом заболевание очень заразное. Но поскольку уровень летальности у некоторых штаммов Эболы достигает 90%, а у тех, что помягче — 20-30%, что тоже очень-очень много, на практике это не приводит к большим вспышкам, потому что очаг вымирает. Человек, который заболел Эболой, ложится и умирает, а не садится в самолет до Манхеттена. Правда, лихорадка Марбург названа так потому, что в этот немецкий город прилетел человек из Африки, и там была впервые описана симптоматика. Но человеку опять же было не до распространения возбудителя, и большой вспышки не произошло.
Какие условия должны совпасть, чтобы спровоцировать ситуацию, подобную нынешней?
Вирус должен быть очень заразным, чтобы для заражения достаточно было получить немного вирусных частиц. Иными словами, вирусу нужна хорошая хватка. У SARS-CoV-2 очень высокая эффективность присоединения его spike-белка — шипиков на коронке — к протеинам на клетках. Не у всех вирусов так.
Еще нужна высокая вирулентность — уровень вирусных частиц в организме. Их должно быть много, чтобы человек мог их выделять дальше и распространять вокруг себя. Самая гениальная штука у SARS-CoV-2 — он становится заразным до появления симптомов, его скрытая вирулентность — 3-4 дня. В какой-то момент вирусных частиц в человеке уже много, но симптомы еще не наступили.
В-третьих, вирус должен быть не слишком патогенным, чтобы быстро не убивать своего носителя, тем самым позволяя зараженному распространить инфекцию.
Родственники нового коронавируса, вызвавшие вспышки в 2002-2003 и 2012 гг., на эту роль не подошли: MERS был слишком убойный, чтобы стать проблемой для всех. Он, конечно, был очень большой проблемой, но только для тех людей, которые уже заразились. SARS вел себя, как джентльмен: у него симптомы и способность заражать появлялись одновременно.
В этом смысле новый коронавирус, конечно, выигрывает. Многие верят в конспирологическую теорию о том, что возбудитель COVID-19 создан искусственно. Недавно в том же ключе высказался и Нобелевский лауреат Люк Монтанье. Что вы на этот счет думаете?
С таким количеством наград и почтенным возрастом Люк Монтанье может себе позволить оригинальные заявления. К тому же, вирус возник в городе Ухань, где есть вирусологическая лаборатория, — от этого трудно отмахнуться, поэтому история будет всплывать еще долго. Представьте, что рядом с вами была фабрика по производству игрушек, и вот вас засыпало игрушками. Сложно поверить, что эти события никак не связаны. Но вирус — это не черный ящик. Его последовательность нуклеотидов — генетическая структура — для вирусологов очевидна. Это как составить стихотворение из фрагментов текстов, например, Пушкина и Лермонтова. Неспециалисту будет казаться, что автор у стихотворения один. Но любой мало-мальски подготовленный филолог немедленно определит, где чей текст. Естественные мутации выглядят иначе, чем искусственно составленная химера. Кроме того, наши инструменты еще не позволяют создать вирус, у которого все было бы настолько удачно подогнано.
Идеальный резервуар
От каких животных мы чаще всего заражаемся новыми инфекциями?
От обезьян, летучих мышей, грызунов, водоплавающих птиц и свиней. Последние — уже домашние животные, с природой особо не общаются. Но они — идеальный посредник между нами и разными видами животных и одновременно пробирка, в которой дикие вирусы могут приобрести новые способности, в том числе способность заражать человека. Так было, например, с вирусом Нипах. Его свиньям передали плодоядные летучие мыши. Они едят фрукты в больших количествах — под деревом, на котором питаются крыланы, всегда ужасный срач: обжеванные фрукты, все обкакано. Свиньям в таких местах очень приятно пастись. Еще сверху яблочек накидают. Таким образом крыланы передали свиньям вирус Нипах. Это случилось в Малайзии. Свиньи начали чихать и кашлять, заразилось примерно 2 миллиона животных. Какая-то часть свиней погибала, но не много. У них вирус Нипах был не особенно патогенным, но высоко вирулентным. От свиней заражались люди, у которых эта инфекция уже протекала тяжело.
Еще свиньи могут передавать человеку вирус гриппа. В 2009 году из-за этого случилась пандемия.
Природный резервуар вируса гриппа — водоплавающие птицы. Через свиней грипп попал к человеку. Вирус 2009 года назвали мексиканским. Мексиканка очень похожа на знаменитую испанку (вирус, вызвавший самую массовую пандемию гриппа в истории человечества — прим. ред.), но, по счастью, была немного видоизмененной.
Условно говоря, вирус гриппа состоит из 8 вагончиков. Эти вагончики можно переставлять местами. Достаточно переставить 2 вагончика — и это уже совсем другой вирус, на который не действуют предыдущие вакцины. Порядок постановки вагончиков определяет тип вируса. Кроме того, внутри этих вагончиков тоже бывают мутации, поэтому вирус мексиканского гриппа 2009 года был не такой смертоносный, как испанка. Он, конечно, людоед, но не настолько. Этим вирус гриппа отличается от других РНК-вирусов, у которых частые мутации сильно не меняют сам вирус. Коронавирус мутирует более медленно, чем вирус гриппа.
Почему новые болезни родом, в основном, из Азии или Африки?
Это горячие точки биоразнообразия. В этих странах очень высокая плотность биоценозов и большое количество потенциальных резервуаров для вирусов. Лучше всего вирусы, опасные для человека, живут в обезьянах, потому что они наши родственники. Обезьяны — это Африка, Азия и в меньшей степени Южная Америка. Большая часть летучих мышей живет в тропических зонах. А рукокрылые — идеальный резервуар для вирусов.
У летучих мышей очень гостеприимный иммунитет: не настолько агрессивный, как у человека. Иммунитет рукокрылых относится к патогенам более философски: ну, живет в моих клетках какой-то вирус, удваивает свои вирусные РНК, сильно много ресурсов у меня не отнимает, ну и ладно. Более того, вирус не просто живет у них внутри клетки, но и сам является противовирусной защитой, не пуская в клетку другие вирусы. Либо два вируса могут занять клетку и не пускать третьего. Часто летучие мыши инфицированы несколькими видами вирусов. Эти вирусы образуют альянсы, коалиции, воюют друг с другом — у них своя игра престолов, а мыши живут себе при этом спокойно. Наконец, способность к полету — очень мощный эволюционный фактор. Чтобы летать, нужно прокачать свои качества, избавиться от всего лишнего, стать более-менее идеальным. Во время полета у мышей ускоряется метаболизм, повышается температура, и это тоже играет роль противовирусной защиты.
Привычки и образ жизни местного населения могут способствовать появлению межвидовых болезней?
Есть гипотеза раненого охотника. Охотники пошли в лес, кого-то убили, при этом поранились, заразились и дальше начали распространять вирус сами. Так, например, случилось с ВИЧ-инфекцией в Африке.
Почему не стоит есть горилл
Вирус иммунодефицита попал к нам от обезьян?
Да, человек, вероятно, порезался при разделке шимпанзе, подцепил возбудителя ВИЧ-инфекции в обезьяньем варианте. Это случилось в начале 20 века.
И вирус мутировал?
Да, ВИЧ мутирует невероятно быстро. В какой-то момент вирус начал очень удачно колонизировать клетки человека и хорошо распространяться дальше уже через людей. Симптомы отложенные — до развития СПИДа может пройти 10-15 лет. Люди в Африке умирают по разным причинам, поэтому никого не настораживали смерти от разлада всего организма. Мощный толчок развитию эпидемии дала прививочная кампания в Африке в 20-е годы. Шприцы тогда были очень дорогими и многоразовыми. Их, конечно, стерилизовали, но не всегда в должной мере. В общем, большое количество африканцев породнили одним шприцем. В какой-то момент в этой цепочке оказался человек с ВИЧ. Свою роль сыграло и распространение проституции в бедных африканских странах. К 60-м годам это была уже достаточно распространенная в Африке болезнь, которую все еще не обнаружили.
Как же все выяснилось?
В 60-х республика Конго получила независимость и стала приглашать специалистов из разных стран помочь в строительстве нового государства. В том числе туда прилетели рабочие из Гаити — гаитян звали охотно, обе страны франкоговорящие. За годы работы многие из приглашенных гаитян заразились ВИЧ, вступая в сексуальные контакты с местным населением, а после привезли вирус к себе в страну. Оттуда ВИЧ попал в США, где, наконец, и был обнаружен.
А от кого к нам пришла Эбола?
Через обезьян — похоже, от летучих мышей. По крайней мере, родственная Эболе лихорадка Марбург передается от летучих мышей — при том не через укусы, а через контакты с выделениями. Предполагают, что и в случае с Эболой без рукокрылых не обошлось, но точно вид-резервуар еще не определили. Вероятно, что обезьяны оказали нам посреднические услуги. В лесу рядом с очагом находили мертвых горилл и шимпанзе. Для обезьян это тоже новый вирус — такой же фатальный. Люди в Африке не брезгливые, ели этих умерших животных и заражались (вероятно, заражение происходило в процессе приготовления пищи — прим. ред.).
Не только животные могут заражать людей. Человек тоже в этом смысле представляет опасность для животных?
Представьте, что вы где-нибудь в Руанде идете посмотреть на горных горилл в лес, где они живут. Если животные в настроении, то могут даже подойти к вам, чтобы пообниматься. На этот счет, кстати, есть инструкция: если горилла обняла вас, просто стойте и наслаждайтесь моментом. Она пообнимается и уйдет. Контакт достаточно близкий, поэтому по правилам люди должны приходить туда в масках, чтобы не заразить горилл человеческими болячками. Если вы чем-то болеете, например, простудились, вас не пустят к гориллам: ваша обычная простуда может вызвать смертельную эпидемию у обезьян. Но мы можем переносить опасные для животных инфекции не только в собственном организме.
Что вы имеете в виду?
Сейчас в обеих Америках вымирают амфибии — целыми видами. Несколько лет назад любители-лягушководы случайно завезли в Америку вместе с экзотическими там дальневосточными жерлянками грибок хитридию. Он вызывает смертельную для неиммунных амфибий болезнь хитридиомикоз. Лягушки Старого Света жили вместе с этим грибком более-менее мирно. А для американских земноводных грибок оказался ужасной катастрофой. Из-за этого нарушились все трофические связи: лягушки вымирают, змеям становится нечего есть, они переключаются на птиц, ящериц, которые, разумеется, страшно недовольны. В общем, происходит совершеннейший бардак.
Генетическое бессмертие
Почему убивать животных, которые переносят опасные для человека инфекции, — плохая идея?
Это нарушает биологическую саморегуляцию, ломает естественную систему сдержек и противовесов. У каждого вида свое место, своя экологическая роль: каждый кого-то кормит, кого-то ест, кому-то помогает, кому-то мешает, и все это очень важно для общего баланса. Уничтожая одних, вы даете фору другим, и неизвестно, к каким последствиям это приведет. Как правило, все становится еще хуже.
Например, рукокрылые — самый многочисленный отряд млекопитающих по количеству особей. Для нас это не очевидно, поскольку мы с ними работаем в разные смены, но количество и экологическая роль летучих мышей — огромны. Уничтожение рукокрылых приведет к вспышке численности насекомых, а это, в свою очередь, может привести к чему угодно.
В случае с человеком эти закономерности тоже работают?
Люди — джекпот для вирусов: живем кучно, общаемся много. К нам залезть и научиться на нас паразитировать — очень выигрышный билетик для вирусов. И его вытягивали уже многие ребята. Обломки вирусных геномов составляют 40-50% человеческого ДНК. Рекорд среди всех исследованных организмов.
Что это значит?
С самых ранних этапов эволюции мы постоянно заражаемся, заболеваем, но постепенно коэволюционируем и встраиваем в собственный геном множество вирусов. Для вируса это идеальный вариант — он встраивается в генетический код хозяина, и его информационная последовательность копируется с каждым делением клетки. Все, ты обрел генетическое бессмертие. Встроенный вирус будет существовать столько же, сколько существует вид-хозяин.
Но и хозяин получает бенефиты от этого симбиоза. Раньше эта почти половина нашей ДНК считалась просто мусором. Теперь на нее смотрят в том числе как на возможную противовирусную защиту. Встроенные охранники мешают новым вирусам проникать в клетку. Возможно, если бы не эти остатки древних вирусов в нашем геноме, мы бы сегодня болели гораздо больше.
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
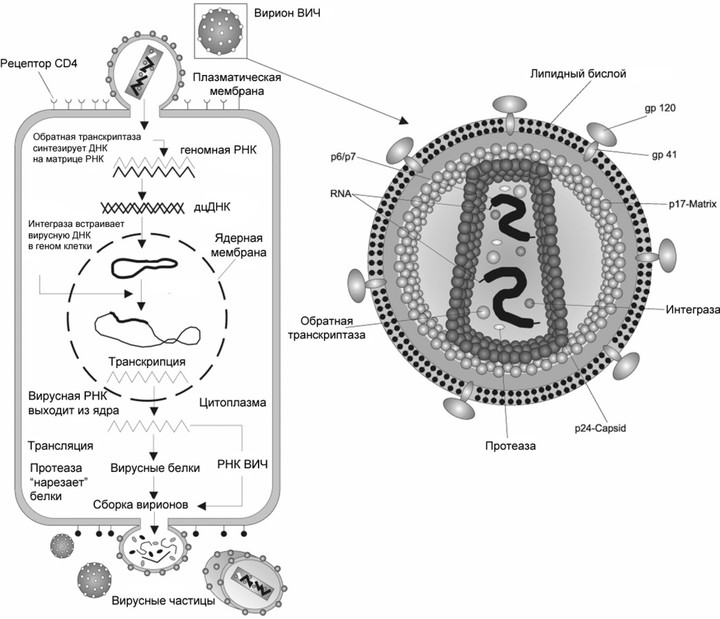
Жизненный цикл вируса, на примере вируса иммунодефицита
Как с ними бороться?
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
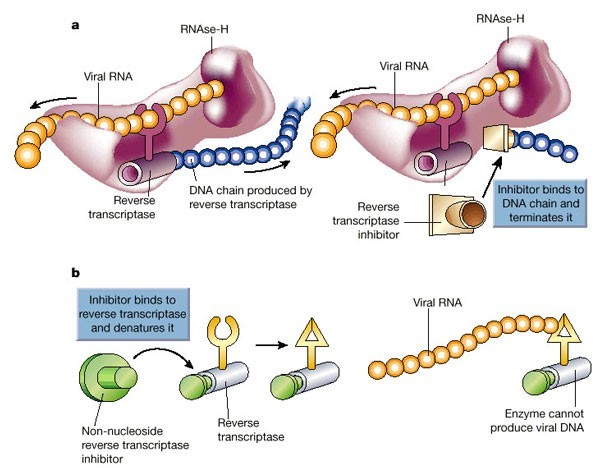
Механизм дейсвтия ингибиторов обратной транскриптазы
3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
4. Созревание
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.
Все мы хорошо знаем, что АРВТ достигла больших успехов, она весьма эффективна. Благодаря чему? Благодаря тому, что в клетке, в которой размножается вирус, есть специальные мишени для АРВТ-препаратов. Что это за мишени? Это ферменты вируса, отвечающие за проникновение в клетку, обратную транскрипцию, интеграцию и, наконец, созревание вирусных частиц.
Цель АРВТ — это стабильное снижение вирусной нагрузки. Каждый, кто лечит ВИЧ-инфекцию, хорошо знает, что сначала вирусная нагрузка снижается очень быстро. Практически за несколько недель она теоретически может упасть до неопределяемого уровня. Почему он достигается так быстро? Потому что на первом этапе применения АРВТ основной мишенью для лекарств являются СД4 лимфоциты, которые находятся, как мы понимаем, в кровотоке и легко доступны для препаратов.
Сейчас мы можем констатировать, что кроме уже названного этапа есть еще и второй этап снижения нагрузки. Этот этап связан с вирусом, попавшим в клетки-макрофаги. Лекарства сюда проникают намного хуже, намного медленнее. Тем не менее продолжение терапии позволяет несколько снизить вирусную нагрузку и в них.
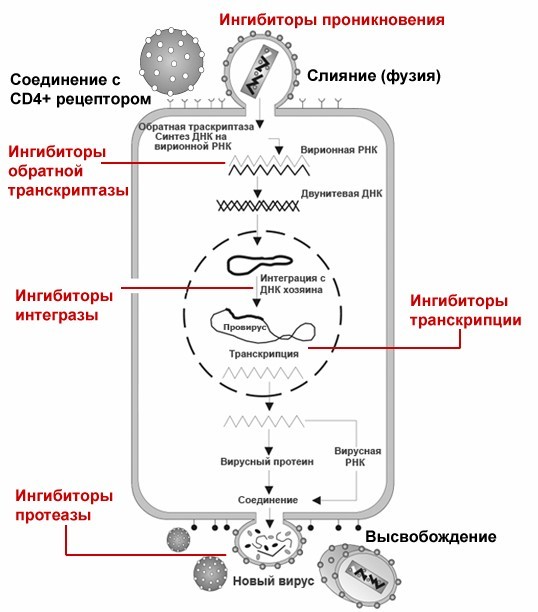
Схема работы антиретровирусной терапии.
Но что происходит с вирусной нагрузкой после того, как она стала неопределяемой? Чтобы ответить на этот вопрос, существуют так называемые ультрачувствительные методы. После того как вирусная нагрузка наконец выходит на плато, мы видим лишь единичные копии РНК вируса, но снизить ее еще больше уже не представляется возможным.
На заре такого рода исследований первой мыслью, которая пришла в голову ученым, было увеличить интенсивность терапии, чтобы достичь полного уничтожения вирусных частиц в организме. Для этого были испробованы несколько вариантов, которые были связаны с повышением дозировок, с увеличением количества препаратов в схеме, с применением новых препаратов. Но ни один из перечисленных инструментов не привел к желаемым результатам. Это, очевидно, указывало на то, что размножение вируса не является главным источником остаточной виремии. Так, к настоящему времени сформировалось представление о так называемых резервуарах ВИЧ.
Спящие хелперы
по теме
Лечение
Как устроены ВИЧ и АРВТ? Объясняем на пальцах
Резервуары бывают двух видов: анатомические и клеточные. Анатомические резервуары — это такие зоны организма, куда не проникает либо плохо проникает лекарство. Таких зон в организме немало. Прежде всего, это центральная нервная система, лимфоузлы, это ЖКТ и костный мозг.
Главный клеточный резервуар — так называемые латентно-инфицированные клетки. Дело в том, что почти все клетки-мишени вируса, в первую очередь хелперные клетки, в определенный момент своей жизни, чтобы выполнить свою функцию, приходят в состояние активации, а после того, как они ее выполнили, дают себе команду апоптоза и погибают.
Клетки памяти сохраняют способность к делению. И делятся простым митозом. Часть из них погибает, но другие могут реактивироваться. Состояние их реактивации достигается разными способами. Иногда это химическое воздействие, иногда физическое, иногда какая-то дополнительная инфекция, которая оказывается в организме.
Т-хелпер
Как только латентно инфицированная клетка оказывается реактивирована, она начинает производить новые вирусные частицы. Что и дает ту самую остаточную виремию, о которой мы говорили выше.
Что делать с этим? Существуют две стратегии излечения. Одна из них называется стерилизующей терапией, или радикацией. Другая — функциональное излечение. Радикация — это полное уничтожение всех резервуаров в организме таким образом, чтобы в нем не осталось ни одной молекулы РНК и ни одной молекулы ДНК вируса.
Функциональное излечение предполагает, что вирус в организме остается в очень небольшом количестве, но при этом излечивающее воздействие приводит к тому, что последующая терапия такому пациенту больше не требуется.
Два пути
Первый случай радикации, о котором мы все уже слышали, — это, конечно, так называемый Берлинский пациент.
Для того, чтобы вирусу присоединиться к клетке, ему нужны два рецептора: один СД4, а другой CCR5. Полноценный CCR5 рецептор кодирует ген CCR5 дикого типа. Но бывает, что в составе этого гена встречается делеция, то есть потеря части хромосомы. Она называется дельта32. В этом случае у человека формируется неполноценный рецептор, а вирус не может присоединиться к клетке-мишени.
Люди с такой мутацией встречаются, и если эта мутация у них в гомозиготе, то они полностью защищены от инфицирования ВИЧ — за редкими исключениями.
Берлинскому пациенту, который был гетерозиготен по дельта32, в результате острого миелогенного лейкоза пришлось сделать полное облучение организма и химиотерапию. АРВТ временно пришлось отменить. После переливания стволовых клеток дельта32 двенадцать лет назад в его организме не удалось встретить ни РНК, ни ДНК вируса.
Так человечество столкнулась с первым случаем полного излечения от ВИЧ-инфекции.
Макрофаг
Уже в этом году, летом, мы услышали еще о двух таких пациентах. У них ситуация была попроще. Лимфома Ходжкина. Лечение было менее тяжелым, им не делали полного облучения, да и химиотерапия была не такая тяжелая. Однократно каждому из них перелили стволовые клетки. В итоге: Лондонский пациент находится в ремиссии уже более двух лет, а Дюссельдорфский — приближается к году.
Считается, что это тоже случаи полного излечения. Но для всех пациентов такая терапия не подойдет. Несмотря на то, что инициатива продолжается и существует целая программа, которая собирает коллекцию стволовых клеток дельта32. На данный момент собрана коллекция потенциальных доноров: около 40 тысяч человек. Безусловно, не всем удастся подобрать донора.
Модификация этого подхода — генная терапия, которая предполагает, что можно взять клетки у человека, уже инфицированного ВИЧ, и вырезать ген CCR5, получив клетки, аналогичные стволовым клеткам дельта32.
В целом, теоретически, это вполне возможно сделать. Такие технологии недавно были использованы на мышах. Более того, в этом году подобную геннотерапевтическую манипуляцию, хоть эксперимент и был воспринят научным сообществом неоднозначно, провели на человеческих эмбрионах. Это знаменитые китайские близнецы.
Впрочем, тут же, появилось несколько публикаций о том, что отсутствие гена CCR5 не совсем безразлично для организма, и люди, у которых такой рецептор отсутствует, подвержены многим другим рискам.
по теме

Лечение
Здесь речь идет о реактивации латентных клеток, чтобы сделать их доступными для АРВТ. На первый взгляд, идея очень хорошая, но на пути этой стратегии уже встретилось немало трудностей. Хотя в некоторых экспериментах объем резервуаров все-таки удавалось снизить, вирусная нагрузка остаточной виремии у пациентов сохранилась. То есть уничтожить вирус в организме врачам так и не удалось.
Основная проблема связана с тем, что резервуары неоднородны. Все клетки в организме, которые имеют на своей поверхности соответствующие рецепторы, могут быть инфицированы. Но они все разные. И разработать препарат, который одинаково работал бы со всеми ними, ученым еще не удалось.
Лабиринт из тупиков
Как этого добиться? На эту тему сейчас проходят исследования. Некоторые из них касаются ограничения процесса инициации транскрипций, в котором принимает участие белок, носящий название Tat. Это самый главный вирусный трансактиватор транскрипций. А также клеточные белки, которые связаны с этим же этапом.
Некоторые связаны с идеей блокирования окружения провирусной ДНК и изменением структуры хроматина. Новые препараты, работающие по этой технологии, так называемые ингибиторы фактора LEDGF/p75, скоро будут апробированы в клинике.
Итак, проблема полного излечения ВИЧ волнует сейчас очень многих ученых, но мы находимся в начале этого сложного лабиринта, который рано или поздно приведет нас к искомой цели.
В каком состоянии находится проблема на данный момент в целом? В этом лабиринте, как вы понимаете, много тупиков. И некоторые из этих тупиков уже пройдены, а это тоже очень важно. Важно понимать, куда ходить не стоит, потому что по мере того, как ошибочные решения будут исключаться, мы, наверное, найдем правильный ответ и придем к искомой цели.
Лично мне кажется, что сейчас настает очень интересный момент. Накопление новых данных идет с огромной скоростью. Во всем мире еженедельно публикуется множество исследований и многие выглядят очень и очень перспективно. А стало быть, в ближайшие несколько лет нам можно ожидать прорыва.
16. Обязан ли я раскрыть информацию о своем диагнозе?
Одна из причин, почему стоит сказать своим сексуальным партнерам, что у вас ВИЧ, — это защитить их от инфицирования вирусом. Если вы используете презерватив или ваша вирусная нагрузка ниже определяемого уровня, а ваш партнер использует ДКП, то эта предосторожность может показаться лишней. Также это может не иметь большого значения с точки зрения охраны здоровья или межличностных отношений. Однако существует еще юридическая причина, по которой раскрытие этой информации может быть очень важным. Во многих штатах (***также как и в России) действуют законы, обязывающие информировать о своем ВИЧ-статусе, а в некоторых штатах эта обязанность действует независимо от того, стал ли партнер в результате контакта ВИЧ-положительным или нет. Вам необходимо знать о том, какие законодательные акты действуют в вашем штате, чтобы не нарушать закон.
17. Теперь я буду вынужден пользоваться презервативом всю оставшуюся жизнь?
Нет. Вы можете заниматься сексом без презерватива, если риск небольшой, особенно если ваша вирусная нагрузка ниже определяемого уровня, а ваш партнер использует средства ДКП. Иеремия Джонсон, координатор по профилактике, исследованию и политике ВИЧ в Группе по активному лечению, указывает на два исследования — HPTN 052 и PARTNER. По результатам данных исследований не было выявлено ни одного нового случая инфицирования во время контактов с ВИЧ-положительными партнерами, у которых вирусная нагрузка была ниже определяемого уровня. В Сан-Франциско было проведено исследование Kaiser по изучению серодискордантных пар в течение нескольких лет. За это время не было выявлено ни одного случая передачи ВИЧ-инфекции, если ВИЧ-отрицательный партнер использовал ДКП.
18. Значит, я могу выбросить презервативы?
Не стоит этого делать (если только у них не истек срок годности). Даже если вы и ваши сексуальные партнеры уверены, что для профилактики ВИЧ-инфекции не требуется дополнительной защиты, существует полдюжины других инфекций, передающихся половым путем. Презерватив может защитить от этих заболеваний. Помните, множество людей с ЗППП даже не подозревают о них. Гонореей или сифилисом может иметь очень серьезные последствия для здоровья. В прошлом году среди в основном ВИЧ-положительных геев произошла вспышка сифилиса с поражением глаз, которая привела к слепоте некоторых из них. Факт наличия ВИЧ не защищает вас от инфицирования другими болезнями (или даже другим штаммом ВИЧ). Более того, это делает вас более уязвимым к таким заболеваниям.
19. Как быть с оральным сексом?
20. Могу ли я завести детей?
Да. Лекарственные препараты могут свести риск передачи ВИЧ от матери ребенку во время беременности и родов менее чем к одному проценту. Перед оплодотворением необходимо очистить от вируса сперму ВИЧ-положительного донора. Основным отличием будет то, что вам понадобится специалист по ВИЧ, оплодотворению и деторождению. С недавнего времени врачи рекомендуют ДКП для профилактики инфицирования партнера в парах, которые пытаются зачать ребенка. Если вы хотите усыновить ребенка или оформить опекунство, то для ВИЧ-положительных родителей существуют защитные меры, благодаря которым ваши интересы не будут ущемлены.
21. Что именно мне нужно сообщать медицинским работникам при необходимости консервативного лечения?

22. Повлияет ли ВИЧ-положительный статус на возможность операции по перемене пола, пластической операции или шунтирования желудка?
Нет. Ранее считалось, что хирургическое вмешательство увеличивает риск осложнений. Но в 2006 году в журнале Американской медицинской ассоциации были опубликованы результаты исследования по сравнению ВИЧ-положительных и ВИЧ-отрицательных пациентов, перенесших оперативное вмешательство. Было выявлено, что уровень осложнений после операции был одинаковым в обеих группах пациентов. Кроме того, сейчас медицинские работники лучше осведомлены о ВИЧ-инфекции, чем раньше, а это способствует уменьшению страха при работе с пациентами. Но вам, возможно, придется приложить больше усилий, чтобы найти хирурга, который работает с ВИЧ-положительными пациентами. А если вы транссексуал, то врача, который сможет работать как с вашим доктором-специалистом по ВИЧ, так и с вашим хирургом, делающим операции по смене пола.
23. А что насчет гормональной терапии для транссексуалов (или у женщин в период менопаузы)? Как препараты против ВИЧ воздействуют на уровень эстрогена или тестостерона?
Согласно проекту Well Project, по данным некоторых исследований, как ВИЧ-инфекция, так и некоторые лекарства для её лечения могут повлиять на уровень гормонов. Однако существуют препараты для лечения ВИЧ-инфекции, которые не будут мешать вашей гормональной терапии. Вместе с врачом вы сможете подобрать правильный курс лечения, который позволит контролировать ВИЧ-инфекцию, продолжить гормональную терапию и сохранить желаемую половую принадлежность.
24. Необходим ли мне специалист по ВИЧ?
Да. Очень важно как можно быстрее найти врача, который специализируется на работе с людьми, живущими с ВИЧ. Специалиста могут посоветовать сотрудники центра, где вам диагностировали ВИЧ-инфекцию, либо вы можете обратиться за рекомендацией в поликлинику. Найти специалиста по ВИЧ, который соответствует вашим запросам, — самый первый шаг, который необходимо сделать после постановки диагноза. Этот человек в буквальном смысле будет вашим спасателем.
25. Как наркопотребителю уменьшить риск передачи ВИЧ и гепатитов?
Уменьшить риск заражения ВИЧ при парентеральном введении любого препарата можно: Используя при каждом введении препарата новый, ранее никем не использованный шприц и иглы, или только свой "персональный" шприц и иглу, которыми никто более не пользовался. Можно достигнуть, каждый раз используя новый стерильный инструментарий. Наиболее эффективным методом, предупреждающим передачу ВИЧ со шприцами и иглами, является использование шприцев, саморазрушающихся после однократного использования. Повторное использование таких шприцев невозможно и поэтому они уже не могут участвовать в передаче инфекции. Используя при введении препарата шприц и иглу, прошедшую предварительную обработку длительным кипячением или дезинфицирующими средствами. Используя для введения раствор препарата, приготовленного в условиях исключающих попадание крови другого лица. Кипячением раствора препарата непосредственно перед введением, не промывая свой индивидуальный шприц в одной емкости со шприцами, использованными другими людьми.
26. Если по какой-либо причине у меня началось кровотечение, должен ли я беспокоиться о людях, которые мне помогают?
Одно предостережение: сотрудники скорой медицинской помощи должны использовать универсальные меры предосторожности при работе с пациентом. Но если вы попадаете в серьезную автомобильную аварию или происходит другой несчастный случай, то лучше сообщить им о своем ВИЧ-положительном статусе (отказ со стороны медицинских работников в предоставлении медицинской помощи из-за вашего статуса является незаконным, в соответствии с Федеральным законом о защите прав граждан США с инвалидностью).

Мифы сложно искоренить, поэтому начните с рассказа о том, как ВИЧ не передается. Вирус не живет вне человеческого тела, поэтому вы не можете инфицироваться им в туалете или при совместном пользовании чашками либо столовыми приборами. Вы не инфицируетесь ВИЧ при поцелуе или через плевок, так как вирус не передается со слюной. Также он не передается через пот или мочу. Вы не можете инфицироваться в бассейне, горячей ванне, сауне, от укуса комара или грызуна, во время нанесения татуировки, а также после пирсинга уха или тела. Для инфицирования другого человека необходима достаточная концентрация вируса. В такой концентрации ВИЧ может содержаться только в четырех физиологических жидкостях: кровь, сперма, влагалищное отделяемое и грудное молоко. По данным Центров по контролю и профилактике заболеваний, передача вируса от ВИЧ-положительного человека возможна при контакте одной из этих жидкостей со слизистой оболочкой или поврежденной тканью либо при непосредственном попадании в кровоток (из иглы или шприца).
28. Есть ли лекарство от ВИЧ?

29. Прошло 30 лет, почему до сих пор нет лекарства?
30. Что потребуется для лечения?
Читайте также: