Врожденный порок сердца и гепатит
Обновлено: 12.05.2024
Врожденные пороки сердца (ВПС) у детей – патологии, частота которых среди новорожденных в странах Европы и СНГ составляет от 0,8 до 1%.
Что провоцирует / Причины Врожденных пороков сердца (ВПС) у детей:
ВПС у ребенка – наследственное заболевание. Тяжесть зависит от того, насколько выражена генетическая склонность, и насколько повлияли на плод неблагоприятные факторы среды.
Неблагоприятные факторы среды:
- химические вещества (спирты, кислоты, циклические соединения, соли, тяжелые металлы и пр.)
- ионизирующая радиация
- действие лекарств (аминазин, акрихин, винкристин, антагонисты фолиевой кислоты, брунеомицин и пр.)
Врожденные пороки сердца у детей могут быть частью синдрома с множественным поражением органов и систем, который вызван аномалиями хромосом или мутацией каких-либо генов. Такая форма требует обследования ребенка и его родных людей в генетическом центре.
Структура врожденных пороков сердца у новорожденных детей
| ВПС | Частота % |
| Дефект межжелудочковой перегородки | 25-30 |
| Открытый аортальный проток | 12 |
| Дефект межпредсердной перегородки | 10 |
| Стеноз клапана легочной артерии | 10 |
| Тетрада Фалло | 5-10 |
| Стеноз аортального клапана | 5 |
| Коарктация аорты | 5 |
| Общий артериальный ствол | 5 |
| Транспозиция магистральных сосудов | 5 |

Факторы риска рождения ребенка с врожденными пороками сердца:
- возраст отца более 45 лет, возраст матери более 35 лет родителей
- профессиональные факторы, негативно отражающиеся на здоровье матери или отца
- прием антибиотиков (особенно в первом триместре беременности)
- тяжелый токсикоз
- прием гормональных, сульфаниламидных препаратов
- вирусные заболевания, перенесенные беременной (яркий пример – краснуха)
Патогенез (что происходит?) во время Врожденных пороков сердца (ВПС) у детей:
- увеличение количества венозной крови, поступающей в большой круг кровообращения при наличии сброса крови из правых отделов сердца в левые
- степень оксигенации крови в легких
- степень использования кислорода тканями
Цианоз влияет на изменения периферической крови: полицитемию и гипергемоглобинемию. Хроническая кислородная недостаточность вызывает изменение ногтевых фаланг – пальцы напоминают барабанные палочки.
Существует 3 фазы течения врожденных пороков сердца:
Первая фаза – происходят реакции адаптации и компенсации на нарушения динамики кровообращения. Если гемодинамика нарушена значительно, появляется нестойкая гиперфункция миокарда, аварийный вариант по В. В. Ларину и Ф. 3. Меерсону, поэтому легко развивается декомпенсация.
Вторая фаза – относительной компенсации. Физическое развитие ребенка улучшается, как и его моторная активность.
Третья фаза – терминальная. Она наступает при исчерпывании компенсаторных возможностей и развитии дистрофических и дегенеративных изменений в сердечной мышце и паренхиматозных органах. Различные заболевания и осложнения приближают развитие этой фазы болезни, которая обязательно оканчивается летальным исходом.
Ф. 3. Меерсон и его коллеги выделяют 3 стадии компенсаторной гиперфункции сердца:
1. Аварийная
Увеличивается интенсивность функционирования структур миокарда. Появляются признаки острой сердечной недостаточности. Появляется изменение обмена.
2. Вторая стадия
Фиксируют нормальную интенсивность функционирования структур миокарда. Прогрессируют нарушения обмена, структуры и регуляции сердца.
3. Стадия прогрессирующего кардиосклероза и постепенного истощения
Снижается интенсивность синтеза нуклеиновых кислот и белков в гипертрофированном миокарде.
В периоде относительной компенсации постепенно развивается синдром капилляротро-фической недостаточности системы гемомикроциркуляции, приводящий к несоответствию транскапиллярного кровотока сердечному выбросу. Как следствие этого появляются метаболические расстройства в тканях, а также дистрофические, атрофические и склеротические изменения во внутренних органах.
Симптомы Врожденных пороков сердца (ВПС) у детей:
Классификация
Различают больше 100 видов врожденных пороков сердца у детей. Существует также большое количество классификаций, в том числе МКБ-10. Часть исследователей делят ВПС на синие и белые. При синих у ребенка наблюдается синий оттенок кожи, а при белых кожа бледная. Пороки синего типа включают транспозицию магистральных сосудов, тетраду Фалло, атрезию легочной артерии и т.д. Пороки белого типа: дефект межжелудочковой перегородки, дефект межпредсердной перегородки и пр.
Рекомендуется как можно раньше выявлять пороки сердца, чтобы своевременно оказать помощь ребенку. Распознать ВПС у младенцев можно по таким признакам:
- после рождения у малыша оттенок кожи и губ бледный или синюшный
- синюшность может появляться при крике грудничка или при кормлении материнским молоком
- конечности могут быть прохладными
- шумы при прослушивании сердца (не во всех случаях)
- признаки сердечной недостаточности
При врожденных пороках сердца у детей наблюдаются изменения на электрокардиограмме, при эхокардиографическом исследовании, при рентгенографическом обследовании. На протяжении первых 10 лет жизни малыш с ВПС может выглядеть здоровым, даже кожа будет нормального оттенка. Но дальше ребенок начинает отставать в физическом развитии, у него появляется одышка при физических нагрузках, кожа синеет или бледнеет. Тогда рекомендуется срочно обратиться к врачу.
Диагностика Врожденных пороков сердца (ВПС) у детей:
Врачи обращают внимание на проявленные симптомы, которые были описаны выше, и такие факторы:
-
с ретракцией ребер
- цианоз и его реакция на оксигенотерапию
- разница артериального давления на руках и ногах
- характер пульса
- наличие сердечных шумов или их отсутствие на фоне разлитого цианоза
- кардио- и гепато-мегалия
При диагностике используют рентген и ЭХО-кардиографию, ФКГ, ЭКГ, клинический анализ крови. Среди специальных методов исследования при подозрении на ВПС у детей – ангиография и зондирование сердца.
Если ребенок без подозрения на ВПС попадает к кардиологу, у него могут выявить сердечные шумы. У старших детей выявляют мягкий систолический шум в шестом межреберье, который становится более интенсивным после физической нагрузки, при лихорадке и изменении положения тела. Может быть также машинообразный шум во втором межреберье слева от грудины – при открытом артериальном протоке. Пансистолический шум с эпицентром в четвертом-пятом межреберьях слева от грудины выявляют при ДМЖП и митральной регургитации у ребенка. Если есть диастолически шумы, необходимо дополнительное кардиологическое обследование.
Эхокардиография – метод кардиологического обследования, который дает детальную информацию о характере сердечных аномалий и внутрисердечной гемодинамике. раньше вместо этого метода применялась катетеризация сердца. Этот метод не применяется изолировано, его нужно сравнивать с результатами ФКГ, ЭКГ и пр.
Врач при диагностике после определения основных гемодинамических нарушений должен уточнить анатомический вариант порока сердца. Далее уточняют фазу течения порока, ищут вероятные осложнения, которые могли возникнуть.
Лечение Врожденных пороков сердца (ВПС) у детей:
ВПС лечат хирургическими методами и терапевтическими. Последние часто являются вспомогательными. Плод обследуют еще до рождения, тогда же решается вопрос о применении хирургических методов лечения врожденных пороков сердца у детей. Роды в таких случаях рекомендуется проводить в родильных отделениях при кардиохирургических больницах.
Терапевтическое лечение применяют, если операцию можно перенести на более поздние сроки. Что касается так называемых бледных пороков, лечение зависит от того, насколько оказывает влияние на состояние ребенка порок с течением месяцев и лет. Есть большие шансы, что понадобится терапевтическое лечение.
Профилактика Врожденных пороков сердца (ВПС) у детей:
Вопрос о продолжении рода должен приниматься обдуманно и взвешенно. Если есть информация, что в вашей семье или в роду мужа кто-то страдал пороками сердца, учитывайте вероятность того, что ребенок родится с врожденным пороком сердца (ВПС). Беременная должна донести эту информацию до врача, который ее наблюдает, чтобы он был более внимательным, искал у плода признаки ВПС. Во время беременности обязательно нужно проходить УЗИ.
К каким докторам следует обращаться если у Вас Врожденные пороки сердца (ВПС) у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Врожденных пороков сердца (ВПС) у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
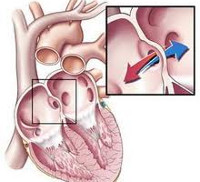
Общие сведения
Врожденные пороки сердца - весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).

Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
“У моего ребенка медотвод - прививки мы не делаем”. К сожалению, мы часто слышим такое. Иногда медотводы оформляют узкие специалисты (которые не являются чаще всего экспертами в вакцинации), иногда сами родители, иногда педиатры, не очень хорошо владеющие вопросом. Давайте разбираться на основе официальных медицинских руководств - когда есть причины для реального медотвода от прививок, а в каких случаях эти медотводы ложные.
Когда действительно прививки делать нельзя?
- температура выше 40 С;
- в месте введения вакцины – отек и покраснение более 8 см в диаметре;
- анафилактический шок и другие тяжелые генерализованные аллергические реакции;
- энцефалит;
- вакциноассоциированный полиомиелит;
- стойкие неврологические нарушения.
- Иммунодефицитное состояние (первичное). Однако детей с первичным иммунодефицитом можно безопасно вакцинировать инактивированными вакцинами в периоде компенсации.
- Иммуносупрессия, злокачественные новообразования.
- Вес ребенка при рождении менее 2000 г.
- Келоидный рубец, в т. ч. после предыдущей дозы.
- Прогрессирующие заболевания нервной системы
- Афебрильные судороги в анамнезе.
- Тяжелые формы аллергических реакций на аминогликозиды.
- Анафилактические реакции на яичный белок (кроме краснушной вакцины).
Часто ли выявляют эти противопоказания?
Нет. Например, вероятность возникновения местной выраженной реакции после введения вакцины Пентаксим составляет не более 1%, а вероятность развития лихорадки свыше 40*С на нее же - не более 0,1%. Вероятность развития поствакцинального анафилактического шока описывается в литературе как единичные случаи на миллион введенных доз вакцин.
Сам список противопоказаний за последние десятилетия сильно сократился, потому что повысилось качество вакцин, и, как результат, снизилась их реактогенность (возникновение нежелательных реакций после введения). В принципе медицинская наука стала больше знать о причинах “осложнений” и перестала связывать их напрямую с вакцинацией.
Что делать, если противопоказания у ребенка все же выявлены?
Нужно обратиться к педиатру или аллергологу, чтобы вместе разобраться в ситуации и подобрать альтернативные вакцины и/или дополнительную терапию для снижения риска вакцинации.
А есть временные противопоказания?
Да. Это острые инфекционные и неинфекционные заболевания - плановые прививки проводятся сразу после купирования симптомов или через 2-4 недели после выздоровления.
Также к временным противопоказаниям относятся обострения хронических заболеваний. Вакцинация откладывается до наступления ремиссии – полной или максимально достижимой, самостоятельной или на фоне лекарств (педиатр может назначить поддерживающее лечение, поможет правильно подобрать время для прививки).
Мой ребенок заболел ОРВИ, на сколько отложить плановую прививку?
Отечественные рекомендации говорят, что при не тяжелых ОРВИ, острых кишечных инфекциях прививку можно сделать сразу после нормализации температуры.
Американские рекомендации призывают не откладывать вакцинацию при легком течении инфекционных заболеваний, даже сопровождающихся лихорадкой в пределах 38,3 С.:
“Легкие заболевания - не повод откладывать вакцинацию. Если даже у ребенка есть насморк или кашель, средний отит или легкая диарея, он может быть привит. Важно привить ребенка вовремя (даже если он плохо себя чувствует), чтобы защитить от более серьезных заболеваний. Вакцины не делают легкое заболевание хуже, иммунная система ребенка способна работать на два фронта одновременно: создавать иммунитет после прививки и бороться с ОРВИ.”
Что такое ложные медотводы?
Это состояния, при которых доктора отказывают детям в вакцинации без каких-либо серьезных на то оснований. Любая выявленная патология (зачастую несуществующая), либо минимальные отклонения в анализах или инструментальных исследованиях становятся поводом не искать возможности безопасно привить ребенка, а оформить “медотвод” на длительный срок или навсегда. Цитируем официальный документ Минздрава: “Использование педиатром ложных противопоказаний должно рассматриваться как свидетельство его некомпетентности в вопросах иммунопрофилактики со всеми вытекающими отсюда мерами.”
Вот список ЛОЖНЫХ медотводов от прививок
Перинатальная энцефалопатия. Это собирательный диагноз, объединяющий временные остаточные проявления нетяжелого повреждения ЦНС во время беременности и родов: изменение мышечного тонуса, нарушения сна, запаздывание формирования психических и моторных навыков. Для безопасной вакцинации достаточно будет осмотра неврологом в диспансерные сроки для исключения прогрессирующего процесса.
Стабильные неврологические состояния (эпилепсия с адекватной терапией, ДЦП, синдром Дауна и др.) - риск поствакцинальных реакций и осложнений не превышает таковой в обычной популяции.
Не тяжелая анемия - не повод запрещать или откладывать прививки. Параллельно с вакцинацией проводится лечение анемии. Анемия тяжелой степени может стать временным медотводом от вакцинации для выявления ее причин и подбора терапии.
“Дисбактериоз” - это не медотвод и даже не диагноз в практике современного врача. Изменения состава микрофлоры в анализе кала не является поводом ни для диагноза, ни для откладывания прививок.
Увеличение тени тимуса на рентгенограмме. Обычно это случайная находка при рентгенографии грудной полости. Является вариантом нормы или результатом временной послестрессовой гиперплазии тимуса (например, после ОРВИ). На эффективность вакцинации не влияет, риск осложнений от нее не увеличивается.
Аллергические заболевания. За исключением анафилактических реакций на предыдущие введение конкретных вакцин или на их компоненты, аллергопатология - это не постоянное противопоказание. Прививки вводятся на фоне максимально достижимой ремиссии (хотя бы даже на фоне применения лекарственных препаратов, иногда иммуносупрессивных).
Аллергия на белок куриного яйца любой степени тяжести - не противопоказание к введению вакцины против кори-краснухи-паротита по западным протоколам (США, Великобритания, Австралия). Однако в российских инструкциях к вакцинам от кори в противопоказаниях значатся гиперчувствительность/ тяжелые аллергические реакции/ анафилаксия на белок куриного яйца.
Врожденные пороки развития, в т. ч. пороки сердца - также частые ложные медотводы.
Лечение хронического заболевания, в том числе антибактериальными и гормональными препаратами - как правило, не препятствие для прививок. Иногда, при системной гормональной терапии, вопрос решается совместно с аллергологом. Местная гормональная терапия (кожная, ингаляционная) не должна быть поводом для медотвода.
Тяжелые заболевания в анамнезе. Младенцы, перенесшие после рождения тяжелые заболевания (сепсис, пневмония, выраженная желтуха) и поправившиеся, прививаются в обычном или догоняющем режиме.
Неблагоприятный семейный анамнез - не повод для отвода от прививок. Например, поствакцинальные сильные реакции или осложнения у родителей, братьев, сестер не предрасполагают ребенка к аналогичным последствиям. Исключением может быть вакцинация БЦЖ.
Почему ложные медотводы - это плохо?
Потому что такая перестраховка оставляет ребенка уязвимым к тяжелым инфекциям. Более того, по данным исследований, риск тяжелого течения инфекций у детей с хронической патологией повышен и сильно перевешивает риск неблагоприятных исходов вакцинации.
Многие хронические заболевания являются не противопоказанием, а наоборот, показанием к плановой вакцинации в полном объеме и прививкам сверх нац.календаря. Например, ребенку с бронхиальной астмой крайне важно иметь полный курс защиты от коклюша, получать ежегодные прививки от гриппа и быть привитым обоими типами пневмококковых вакцин.
Нам поставили медотвод. Что делать?
К сожалению, врачи в РФ по прежнему часто выдают необоснованные медотводы от прививок - под маской заботы о ребенке. Педиатры Фэнтези специализируются на вакцинации детей с ограниченными возможностями здоровья и особыми потребностями. Наши доктора опираются в своей работе на современные медицинские руководства. На приеме доктор разберется в вашей ситуации, найдет способы организовать максимально безопасную вакцинацию, составит индивидуальный календарь прививок.
Внимание: не забудьте принести предыдущие медицинские заключения и прививочный сертификат!
Вакцинация детей в Фэнтези. Как мы это делаем?
Следуя всем правилам предельно безопасной вакцинации, мы серьезно снижаем процент детей, у которых прививка вызывает пусть и минимальное ухудшение состояния:
- Соблюдаем самые строгие международные стандарты JCI на каждом этапе подготовки и проведения вакцинации.
- Используем импортные вакцины (насколько позволяет ситуация в нашей стране) - с минимальными побочными эффектами.
- Неукоснительно соблюдаем условия хранения препаратов.
- Педиатр обязательно осматривает малыша перед прививкой. Как правило, никакое дополнительное обследование (анализы) не требуется. Почему перед прививкой не нужно сдавать анализы?
- Отслеживаем состояние ребенка после прививки.
- Следим за календарем вакцинации и приглашаем вас на прививки по графику.
- Используем антистресс-методы: игрушки, интерактивные книжки, мыльные пузыри, Божью коровку Buzzy (специальное отвлекающее устройство). Детям старше 5-ти лет мы также можем предложить надеть VR-очки и посмотреть 3D-фильм.
Что еще почитать про вакцинацию?
В этом разделе - наши педиатры отвечают на самые частые и важные вопросы родителей про прививки, а также разбирают аргументы антипрививочников.
Гепатит С – болезнь печени, вызываемая у ребенка или взрослого человека вирусом гепатита С.
Эпидемиология
95 случаев посттрансфузиоиного и парентерального гепатита из 100 в США и Западной Европе вызвано ВГС (вирусом гепатита С). Болезнь возникает часто после переливания крови, содержащей вирус, плазмы, антигемофильного фактора, фибриногена и прочих препаратов крови. Также болезнь может быть вызвана внутривенными вливаниями иммуноглобулиновых препаратов больным детям с иммунодефицитами. Среди острых гепатитов гепатит С является ведущим среди пациентов отделений трансплантации органов, в центрах гемодиализа, в центрах плазмафереза, онкологических стационарах и т. д.
Гепатит С передается исключительно через кровь, вместе с кровью. Потому большой риск заразиться при переливании крови или ее препаратов, если кровь была недостаточно проверена. Риск заражения присутствуют при любых инъекциях или операциях с применением нестерильных инструментов. Гепатит С передается при бытовом контакте при наличии микротравм. Есть вероятность заражения плода от больной матери через плаценту. Младенец может подхватить гепатит С во время рождения или после него, если есть даже небольшие повреждения кожных покровов. Предполагают вероятность передачи ВГС половым путем.
Что провоцирует / Причины Гепатита С у детей:
Вирус гепатита С принадлежит к семейству флавивирусов, его диаметр составляет 22-60 нм. ВГС может быть обнаружен в крови, в экстрактах печени человека или шимпанзе, которые были заражены в процессе экспериментов.
ВГС отличается от других типов гепатита тем, что находится в малых количествах в сыворотке крови заболевшего ребенка. Специфические антитела дают слабый иммунный ответ не вовремя.
Вирус гепатита С можно убить с помощью хлороформа и формалина. Также при повышении температуры среды до 60° С ВГС гибнет за 10 часов. Кипячение позволяет уничтожить ВГС за 2 минуты. Препараты крови для уничтожения вируса стерилизуют ультрафиолетовыми лучами.
Патогенез (что происходит?) во время Гепатита С у детей:
В механизме поражения печеночных клеток при гепатите С ведущую роль играет иммунный цитолиз, реализуемый Т-клеточной цитотоксичностью, направленной против инфицированных гепатоцитов. Исследователи допускают возможность прямого цитопатического воздействия ВГС на клетки печени.
Хронические формы гепатита С могут возникнуть из-за ослабленных способностей мононуклеаров крови к продукции у-интерферона, изменения соотношения иммупорегуляторных субпопуляций Т-хелперов и Т-супрессоров с преобладанием последних и связанного с этим недостаточно эффективного Т-клеточного и гуморального иммунного ответа на действие возбудителя и инфицированных гепатоцитов. Также большую роль в формировании хронических форм гепатита С играет повышенная способность антигена ВГС маскироваться в иммунные комплексы, что приближает это заболевание к иммунокомплексным. Под иммунокомплексными болезнями подразумевают группу заболеваний, которые возникают как следствие отложения иммунных комплексов в разных органах и тканях человека, включая стенки кровеносных сосудов и клубочки почек.
Патоморфология
Не наблюдается строго специфичных изменений в печени при гепатите С. При острой форме гепатита С менее выражено портальное воспаление. Это воспаление клеток печени, окружающих портальную зону. Портальная зона — область, где в ткань печени входят артерия, вена и желчевыводящий проток. Реже случаются очаговые некрозы, более выражен стеатоз (если сравнивать гепатит С с другими формами). Стеатоз печени также известен как жировая инфильтрация печени. Он выражается в накоплении жира в тканях печени.
При хроническом гепатите С усиливается портальная и перипортальная воспалительная реакция с накоплением мононуклеарных элементов. Также может быть выявлен легкий фиброз с тенденцией к септальной пролиферации (разрастание ткани организма путём деления клеток).
В гепатоцитах наблюдаются диффузные дистрофические изменения от легких до тяжелых, включая баллонную дистрофию и некроз.
Хронический процесс в печени может проявляться в морфологической картине сходной с таковой при персистирующем гепатите. Но чаще всего это активный гепатит с относительно редкими мостовидными некрозами и умеренной лимфоидной инфильтрацией.
Симптомы Гепатита С у детей:
Клинические проявления
От 7 до 8 недель длится инкубационный период при гепатите С. Если заражение массивное, срок сокращается до нескольких дней. Если же в организм попало незначительное количество вируса, инкубационный период составит 26 недель. Заболевание имеет плавное, не острое начало. Начинается недомогание, вялость, тошнота, температура тела может повыситься незначительно. В некоторых случаях больные дети жалуются на боли в животе, возможна также рвота. Моча темнеет, и кал становится обесцвеченным через несколько суток. У всех заболевших детей отмечают увеличение печени, а в некоторых случаях и селезенки. У 15-40% больных детей отмечают желтуху, это сравнительно низкий процент.
Если желтухи нет, в таких случаях наиболее ярко проявляются такие симптомы как астенизация, недомогание и увеличение печени. Усилена активность АлАТ и АсАТ в сыворотке крови (в 100% случаев), в части случаев повышено содержание общего билирубина за счет прямой фракции. Редко бывает снижение протромбина, явления диспротеинемии и т. д. От тяжести поражения печени зависят показатели функциональных печеночных проб.
Классификация гепатита С проводится по тем же параметрам, что и у других гепатитов. Болезнь может быть типичной и атипичной. По параметру тяжести гепатит С классифицируют на легкий, среднетяжелый и тяжелый, а также злокачественный. По течению гепатит С делят на острые, затяжные и хронические формы.
Течение
Только в 10-20 случаях из 100 встречается острое течение гепатита С у детей, в остальных случаях заболевание протекает в хронической форме. При переходе в хроническую стадию отмечается гиперферментемия и относительно нормальное общее состояние ребенка. Жалобы отсутствуют. Но печень может быть слегка увеличена и уплотнена. Когда хронический гепатит сформировался, у больных появляется повышенная утомляемость, слабость в теле, диспепсические явления (расстройства пищеварительного тракта). Осмотр позволяет зафиксировать изменения в сосудах, например, телеангиэктазии, пальмарную эритему. Во всех случаях печень увеличена, часто наблюдается увеличение селезенки. Несмотря на малую выраженность клинической симптоматики, патологический процесс в печени морфологически в большинстве случаев соответствует хроническому активному гепатиту, нередко с признаками формирующегося цирроза.

Диагностика Гепатита С у детей:
Диагностировать ВГС помогает анализ крови, при котором методов ИФА в сыворотке крови находят специфические антитела к структурным и неструктурным белкам вируса. Также метод ПЦР позволяет обнаружить РНК вируса, что дает возможность поставить точный диагноз – гепатит С у детей.
Лечение Гепатита С у детей:
Лечат гепатит С у детей по общим принципам, как и другие виды гепатитов вирусного характера. Больному ребенку показан постельный режим, специальная диета, средства для снятия симптомов. При злокачественных формах болезни врачи назначают прием кортикостероидных гормонов. Больные с хроническими формами гепатита применяют для лечения препараты рекомбинантного интерферона, например, интрон А, виферон, роферон А и прочие – по назначению лечащего врача.
Чтобы снять токсическую нагрузку на печень, проводят энтеросорбционную терапию с помощью таких препаратов как энтеродез или энтеросгель. Для длительной энтеросорбции используют селективный энтеросорбент, который имеет выраженные гидрофобные свойства.
Детям с хроническим вирусным поражением печени (HBV и HCV) прописывают комбинированную терапию с применением препаратов с противирусной активностью с различным механизмом действия. Если ребенок более хронической формой гепатита В, рекомендованы ламивудин и циклоферон или виферон и пиклоферон.
Больным необходима патогенетическая терапия – направленная на механизмы развития заболевания. При хроническом гепатите С применяют урсосан – уреодезоксихолиевую кислоту. Она обладает корригирующим действием на основные звенья патогенеза, предопределяющие хроническое течение инфекции. Урсосан дает иммуномодулирующий, антихолестатический, антиоксидантный, антифибротический эффекты. Препарат применяют в дозе от 10 до 15 мг на кг тела больного ребенка в сутки во время приема интерферонов. Или же проводя монотерапию урсосаном (для лечения применяется лишь 1 препарат). Курс может длиться от 3-6 месяцев до 1 года.
Профилактика Гепатита С у детей:
Основные принципы профилактики совпадают с таковыми при гепатите В. Необходимо применять лишь одноразовые шприцы во избежание попадения зараженной крови в организм здорового ребенка. При проведении любых процедур, включащих инъекции родители должны строго следить за инструментарием (в т.ч. за шприцами), которые использует персонал медицинского заведения. Одноразовыми должны быть системы для инфузий, катетеры.
Следует придерживаться правил стерилизации мединструментария – хирургического, стоматологического и др. Это поможет снизить заболеваемость как гепатитом С, так и гепатитом В.
Чтобы снизить заболеваемость среди реципиентов препаратов кроки, нужно проводить тестирование препаратов крови на анти-HCV и активность трансаминаз. Положительные образцы исключаются.
К каким докторам следует обращаться если у Вас Гепатит С у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Гепатита С у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

