Где впервые открыли лек во против туберкулеза
Обновлено: 25.04.2024

19 октября 1943 года был выделен стрептомицин - первое эффективное лекарство от туберкулёза.

Не прошло и 10 лет, как эту победу вознаградили Нобелевской премией – но присудили её не тому, кто получил антибиотик, и не тому, кто начал им лечить.
Золман из Одессы
Лауреат этой премии не был ни врачом, ни физиологом. Он был воплощением американской мечты. Зельман Ваксман, эмигрант, сошедший с парохода без копейки в кармане, стал богат и знаменит на весь мир.
Зельманом он тоже стал в Америке. На родине, в местечке Новая Прилука под Винницей, его звали Золман Яковлевич. Уехал он из Российской империи в 1910 году. Не от погромов уезжал, и не от охранки, а оттого, что после смерти матери не желал смотреть на родные места.
Случилось всё скоропостижно. 20-летний Золман жил в Одессе с компанией весёлых друзей-земляков, готовился поступать в университет. Все они были влюблены в красавицу Машу, каждый сделал ей предложение. И вдруг телеграмма: матери очень плохо. Земский доктор диагностировал кишечную непроходимость. Нужен хирургический стационар. Была ужасная ночь в поезде до Киева, где врачи оперировать отказались – слишком поздно привезли, и вообще это неизлечимо. Две недели мать умирала в муках на глазах у Золмана. Похоронив её и поставив на могиле памятник, он сел в поезд, идущий за границу.
Удивительный мир бактерий
Поначалу жил в Нью-Джерси на ферме своих дальних родственников. Ваксман хотел стать врачом и подал документы в Колумбийский университет. Но если в Одессе ему было трудно поступить из-за квоты на инородцев, то здесь просто не хватало денег. Бесплатно жить на ферме и учиться Ваксман мог только в расположенном поблизости Ратгеровском сельскохозяйственном колледже. Там была специальность микробиология – сравнительно близко к медицине, что примиряло Зельмана с судьбой.
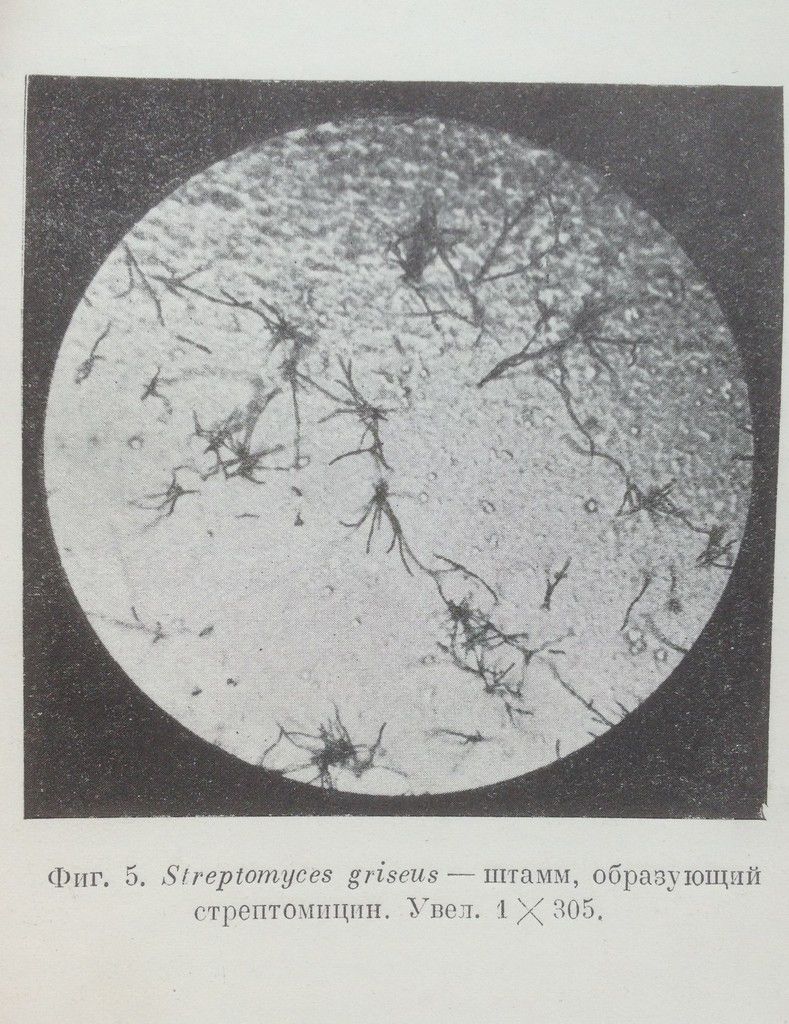
Микроорганизм, продуцирующий стрептомицин. Фото, продемонстрированное Ваксманом на лекции в Москве 12 августа 1946 года
Известный, но бедный
Систематика почвенных бактерий дала Ваксману имя в науке. Он как профессор читал лекции в своём колледже, который стал университетом. Женился на старой знакомой, эмигрировавшей одновременно с ним. К 1924 году им уже хватало денег на билеты в Европу, и Ваксманы отправились навестить своих в Новой Прилуке.
Эра антибиотиков
Многие актиномицеты давали угнетавшие палочку Коха антибиотики, но эти антибиотики были ядовиты. Иногда казалось, что ничего не выйдет, пока студент Алберт Шатц не испробовал мазок, взятый из горла цыплёнка. Живший там стрептомицес давал вещество, убивавшее грамотрицательные бактерии, и не слишком ядовитое для мышей. Такой же стрептомицес нашли через несколько дней в сильно унавоженной почве. На агаре эта культура никакого антибиотика не вырабатывала. Шатц догадался ввести в питательную среду мясной бульон как замену навозу или слизистой цыплёнка – и получил в достаточном количестве стрептомицин.
Застрявшая машина
К нему сразу же проявили интерес ветеринар Уильям Фелдмен и терапевт Корвин Хиншоу, из клиники Мейо, самой передовой хирургической больницы США. Фелдмен заведовал у Мейо разведением подопытных животных. Однажды они с Хиншоу возвращались на попутной машине с какого-то совещания в другом городе. Пошёл сильный снег и машина застряла. Разговорились и решили вместе перепробовать все новые антибактериальные препараты, чтобы подобрать наконец лекарство от туберкулёза. Для этого была снята ферма, где разводили свинок, которым Фелдмен с Хиншоу кололи по очереди то культуру палочек Коха, то антибиотики.

Кристаллический стрептомицин. Фото из лаборатории Зельмана Ваксмана, 1944 год.
Начальство заметило их отлучки с работы, и велело прекратить эксперимент. Но двое продолжали – по ночам, в выходные и отпуска. Хиншоу всё время менялся с коллегами часами, чтобы вовремя добраться к своим свинкам. Он уже был под угрозой увольнения, когда получил от Мерка ваксмановский стрептомицин и начал с ним работать.
Стрептомицин – это серьёзно
Ещё до конца испытания стало ясно, что стрептомицин сметает грамотрицательные бактерии без остатка, с умеренным побочным действием. Фелдмен и Хиншоу приступили к лечению людей. Начали с цистита, после победы над ним спасли от туберкулёзного менингита маленькую девочку, и наконец 20 ноября 1944 года взялись за умиравшую от лёгочного туберкулёза 21-летнюю девушку Патрисию Томас, лежавшую в клиническом санатории. К апрелю 45-го наступило полное выздоровление.
В августе 1946 года он прилетел в Москву читать лекции о стрептомицине в Академии Наук. И узнал, что забирать ему некого: немцы уничтожили всё еврейское население местечка. В живых осталось только трое.
Смерть Оруэлла
Помощь Фелдмену пришла с совершенно неожиданной стороны. В тот самый октябрь 43-го, когда Шатц получил стрептомицин, в шведском городе Мальмё химик Карл-Густав Росдаль синтезировал пара-аминосалициловую кислоту (ПАСК). Идею подал работавший в Швеции датский врач Йёрген Леманн, уже знаменитый тем, что он инъекцией первого антикоагулянта впервые уничтожил послеоперационный тромб.
Тот, кто любит аспирин
Леманн прочитал, что туберкулёзная палочка очень любит аспирин, и получив его, потребляет вдвое больше кислорода. И подумал: раз микроб так охотно втягивает в себя аспирин (ацетилсалициловую кислоту), надо приделать к молекуле этой кислоты такое дополнение, чтобы наевшейся бактерии не поздоровилось. Леманн придумал, чем дополнить, и выяснилось, что никто на свете не умеет ПАСК синтезировать. Росдаль потому и взялся: его увлекала сложность задачи.
Но чудеса, которые творил ПАСК, искупали всё. 24-летнюю пациентку Сигрид Леманн вылечил от туберкулёза даже на месяц раньше, чем Фелдмен и Хиншоу спасли Патрисию. А главное открытие было, что против комбинации стрептомицина с ПАСК резистентности не возникало. Именно такое комбинированное лечение помогло Фелдмену.
Тем временем Шатц узнал про выплачиваемые Ваксману роялти и предъявил на них свои права в суде. В 1950 году стороны договорились в досудебном порядке, из 20-процентных отчислений Ваксману осталось 10%, Шатцу полагалось 3%, остальное поделили между Ратгеровским исследовательским центром и стипендиатами. Так Шатц вырвался из бедности, но приобрёл в научном мире репутацию сутяги. Он больше не мог найти работу в Штатах и уехал в Латинскую Америку.
Нобелевский скандал
В 1951 году Нобелевский комитет распространил среди лауреатов опросный лист, чтобы собрать имена номинантов на следующий год. Почти все упомянули авторов метода лечения туберкулёза: Ваксмана, Фелдмена, Хиншоу и Леманна.
В США прибыла делегация шведских академиков собирать информацию. Фелдмену и Хиншоу дали отвод их собственные руководители. По словам Хиншоу, его начальник сказал гостям, что эти двое самовольно бегают с работы на какую-то ферму, хотя им запрещено возиться с заразными свинками. И Нобелевская премия создаст им большие проблемы.
Однако в учёном кругу история произвела тягостное впечатление на молодёжь. Новое поколение считало, что давать премию одному только руководителю – это приравнивать науку к военному делу, где вся слава достаётся полководцу. Такой порядок оправдан в армии. Он стимулирует офицеров стремиться к новым званиям. Но для учёных с их разделением труда это не работает.
Второе письмо королю
В конечном счёте премии стали присуждать не только теоретику – голове эксперимента – но и тому экспериментатору, который выполнил основную работу. Так вышло, например, с парами Сезар Мильштейн – Георг Кёлер (1984, премия за открытие моноклональных антител) и Андрей Гейм – Константин Новосёлов (2010, открытие графена).
Постарались загладить несправедливость и в отношении обиженных.
Когда клинику торакальной хирургии Каролинского института возглавил Оке Ханнгрен, в юности спасённый Леманном от туберкулёза (Оке буквально кормили пара-аминосалициловой кислотой), Леманн получил от института почётную медаль.
В Ратгерском университете по прошествии многих лет сочли, что достижения, равного получению стрептомицина, у них не было. Разыскали пенсионера Алберта Шатца и также наградили его почётной медалью.
Шатц опять написал королю Швеции, теперь уже Карлу XVI Густаву, и просил заменить формулировку на сайте той, что провозглашалась во время церемонии вручения.
Сегодня новые методы диагностики и лечения помогают врачам своевременно ставить диагноз и предпринимать эффективные ответные меры против этой болезни. Однако так было не всегда, и многие известные люди в своё время погибли из-за несвоевременного и неправильного лечения.
Что такое туберкулёз
Туберкулёз – это широко распространённое в мире заболевание, вызываемое бактерией типа Mycobacterium tuberculosis, которая чаще всего поражает лёгкие человека.
Передаётся заболевание воздушно-капельным путём, заразиться можно от инфицированного даже при разговоре, а также при кашле, чихании или использовании бытовых предметов, бывших в употреблении больного.
Из истории болезни
О заразности туберкулёза знали ещё наши давние предки – упоминания о болезни встречаются в законодательных документах древних вавилонян. В начале XIX века врачи, изучающие причины и развитие чахотки, начали предпринимать первые попытки лечения инфекции.
Так, в 1822 году англичанин Джеймс Карсон попытался вылечить больного с помощью искусственного введения воздуха в плевральную полость (т. н. искусственный пневмоторакс).
В 1882 году итальянский медик Карло Форланини начал на практике применять искусственный пневмоторакс. В России же он был впервые применён в 1910 году.
Открытие возбудителя туберкулёза принадлежит немецкому микробиологу Роберту Коху, который объявил об обнаружении микобактерии Mycobacterium tuberculosis (названной в его честь бациллой Коха) в 1882 году. Наука признала значимость его открытия, и в 1905 году учёный был удостоен Нобелевской премии в области физиологии и медицины.
Позднее учёный смог выделить чистую культуру т. н. бациллы Коха и вызвать с её помощью туберкулёз у подопытных животных. В начале 1890-х Коху удалось получить туберкулин – экстракт туберкулёзных культур, который он представил научному сообществу, как эффективное диагностическое средство при выявлении туберкулёза.
Занимались исследованием туберкулёза и в России. В 1904 году российский учёный Алексей Абрикосов обнародовал исследования, в которых описал картину состояния лёгких на рентгенограмме при начальных стадиях заболевания туберкулёзом.
В 1919 году французские учёные Кальметт и Герен создали вакцинный штамм микобактерии туберкулёза для проведения вакцинации. Применили его впервые в 1921 году.
Клинические и экспериментальные исследования свойств вакцины доказали, что она относительно безвредна, а смертность от туберкулёза среди вакцинированных с рождения детей ниже, чем среди невакцинированных. Широко применяться вакцина стала с середины 1930-х годов, а с середины 1950-х годов вакцинация новорождённых детей стала обязательной процедурой.
Вакцинация как профилактическое средство прошла испытание временем.
Что же касается лечения инфекции, то с 1930-х годов при тяжёлых формах заболевания стали применять эктомию части лёгкого – частичное удаление поражённого участка лёгкого пациента.
Кроме того, в 1943 году американскому микробиологу Зельману Васкману удалось получить первый противомикробный антибиотик стрептомицин, за что учёный был удостоен Нобелевской премии в 1952 году. Первое время после начала применения препарата он был очень эффективен против микобактерий, однако спустя десятилетие он утратил свой клинический эффект и в настоящее время применяется редко.
Тем не менее открытие стрептомицина начало антибактериальную эру в лечении заболевания. С 1954 года начинают использоваться такие препараты, как изониазид и тибон, с 1967 года – одного из самых эффективных противотуберкулёзных средств – рифампицина.

Совершенно новый подход к контролю туберкулёза был создан, во многом благодаря голландскому доктору Карелу Стибло, который в 1974 году предложил принципы т. н. стратегии ДОТС (DOTS) – по сути, противотуберкулёзной химиотерапии с применением специальных препаратов. Так, в 1994 году эта стратегия была рекомендована ВОЗ для применения в странах, для которых проблема заболеваемости туберкулёзом является весьма актуальной.
DOTS до сих пор является основополагающей схемой лечения, хотя современные учёные и медики отчасти модифицировали её, включив препараты нового поколения для более эффективной борьбы с заболеванием.
Знаменитые люди – жертвы туберкулёза
Чахотка описана не в одном литературном произведении, где сюжетная линия часто переплетается с болезнью героев, причём самой болезни авторы порой придавали поэтический и благородный оттенок. Примером таких произведений могут послужить романы Достоевского и Толстого, Чехова и Короленко, Дюма-сына, Манна, Ремарка и многих других.
Не щадила болезнь и самих талантливых авторов. В самом расцвете творческих сил ушли от нас известный русский критик Виссарион Григорьевич Белинский (скончался в возрасте 37 лет), публицист и критик Николай Добролюбов (совсем юным, в возрасте 25 лет), поэт Алексей Кольцов (скончался в возрасте 33-х лет), поэты Иван Никитин и Семён Надсон, живописцы Фёдор Васильев и Мария Башкирцева.
Эти и многие другие известные личности ушли из жизни до того, как были изобретены прогрессивные и более эффективные методы лечения, такие как DOTS, хирургические способы удаления поражённых участков внутренних органов, госпитализация в специальные противотуберкулёзные диспансеры.
Цифры и факты
На 41 % снизились показатели смертности от туберкулёза по сравнению с уровнем 1990 года.
Более 50 млн пациентов успешно излечились от туберкулёза начиная с 1995 года.
Туберкулёз является второй самой распространённой причиной смертности от инфекционного заболевания на Земле, уступая только ВИЧ/СПИДу.
Примерно каждый четвёртый случай смерти ВИЧ-инфицированных людей происходит из-за туберкулёза.
Случаи заболевания туберкулёзом есть в каждой стране мира, однако больше половины из них приходится на азиатские и африканские страны.
Из-за неправильного или ненадлежащего использования противотуберкулёзных препаратов развивается форма туберкулёза, устойчивая к лекарствам. Она называется МЛУ-ТБ. Лечение в таких случаях будет сложное и дорогое.
Риск возникновения туберкулёза у курильщиков в 2,5 раза выше, чем у некурящих людей. Более того, до 20 % глобальной заболеваемости туберкулёзом связывается с курением табака.
Треть населения мира имеет в организме латентный (неактивный) туберкулёз. Это означает, что пока он не перейдёт в активную фазу (если вообще перейдёт), он не является заразным.

Прививку вакциной БЦЖ новорожденным делают в первые дни жизни, еще до выписки из роддома. Эта вакцина используется очень давно, с середины 1950-х годов. БЦЖ до сих пор остается единственным средством профилактики тяжелой формы туберкулеза и его осложнений. В нашей статье — подробнее об этой прививке, ее эффективности и о том, почему она так важна.
БЦЖ: что это?
Вакцина БЦЖ используется для профилактики тяжелых форм туберкулеза. Также она защищает от наиболее опасных осложнений, если человек все-таки заболевает.
Туберкулез — распространенное инфекционное заболевание (рис.1). В мире ежегодно им заболевает до 10 млн. человек, и до 1,4 млн. чел. умирает от этой болезни. В России заболеваемость туберкулезом снижается в последние годы. В 2019 году она составила 41,2 чел. на 100 000 населения, а смертность — 5,2 чел. на 100 000 населения. Несмотря на это, туберкулезная инфекция остается опасной, и вакцинация БЦЖ важна для защиты от нее.
Вакцина БЦЖ является живой. Она содержит живые вакцинные штаммы. Их получают, используя ослабленные бычьи туберкулезные палочки Mycobacterium bovis.
M. bovis — микобактерии туберкулезного комплекса, способные вызывать туберкулез у человека так же, как и основной возбудитель заболевания, палочка Коха (Mycobacterium tuberculosis). Бычья туберкулезная палочка и палочка Коха имеют ряд сходств и различий. M. bovis вызывает схожий иммунный ответ, и ее можно ослабить в лабораторных условиях. Это позволяет использовать штамм для изготовления живой аттенуированной вакцины.
Еще в 1908 году во Франции началась разработка БЦЖ. Вакцина получила название по первым буквам фамилий ее создателей, Альбера Кальмета и Камиля Герена: Бацилла Кальметта-Герена, Bacillus Calmette—Guérin или BCG. Ее протестировали в 1921 году, но испытания оказались неудачными. Позже она была передана в СССР. С 1950 годов началось массовое использование БЦЖ для вакцинации в СССР и других странах. Сейчас ведется разработка новых вакцин, но пока БЦЖ остается единственным средством иммунопрофилактики туберкулеза.
В странах, где уровень заболеваемости туберкулезом является высоким, ВОЗ рекомендует прививать всех здоровых новорожденных в первые дни жизни. Россия относится к числу таких стран. В регионах, где заболеваемость туберкулезом снижается или является низкой, вакцинация от туберкулеза проводится селективно, только для групп риска.
Кому и когда делают?
Российский национальный календарь прививок рекомендует проводить вакцинацию от туберкулеза всем здоровым новорожденным детям в первые дни жизни.
Далее для диагностики туберкулеза и выявления инфицирования микобактериями у детей ежегодно выполняют пробы Манту. Это подкожное введение туберкулина — фильтрата убитых культур микобактерий туберкулеза, прошедших специальную обработку. После пробы на месте укола может появиться покраснение или папула (уплотнение). По ее размерам оценивают реакцию на туберкулин (рис. 2). Если проба отрицательная (в месте укола нет сильного покраснения, припухлости), значит ребенок здоров, и врач может рекомендовать ревакцинацию.
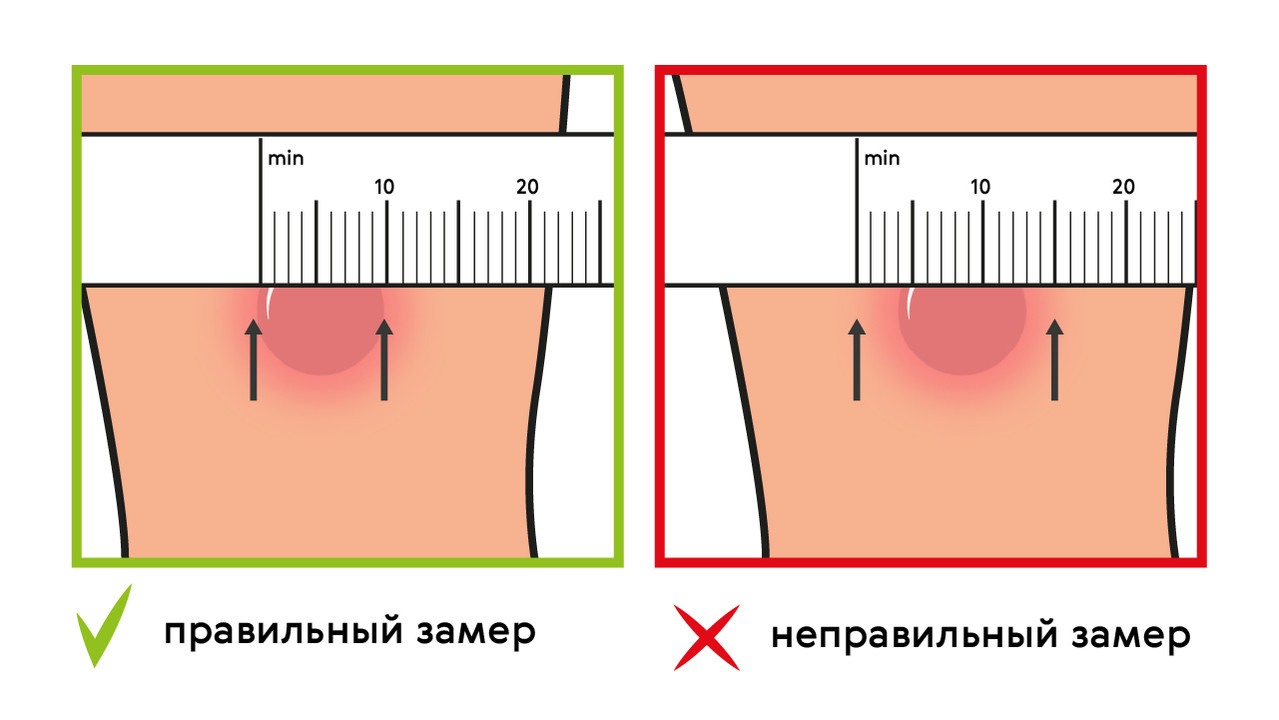
Рисунок 2. Оценка реакции на туберкулиновую пробу. Источник: МедПортал
Вакцинация против туберкулеза может проводиться и для взрослых, но она не так эффективна, как в детском возрасте. Сделать прививку рекомендуют, если человек собирается ехать в страну с высокой заболеваемостью туберкулезом, или ему предстоит контакт с больными. Вакцинация при этом выполняется только если туберкулиновая проба дала отрицательный результат.
Проведение БЦЖ: по календарю и индивидуально
При отсутствии противопоказаний здоровых детей прививают по национальному календарю профилактических прививок два раза:
- на 3-7 сутки жизни до выписки из роддома;
- в 6-7 лет, если туберкулиновая проба является отрицательной.
Если есть противопоказания, прививку делают не в роддоме, а позже, после выписки. В этом случае для ребенка составляют отдельный график иммунизации, планируя ее так, чтобы БЦЖ вводилась отдельно от всех остальных вакцин. Вакцинацию от туберкулеза важно провести как можно раньше. Если ребенок ослаблен, имеет дефицит веса или противопоказания к введению вакцины БЦЖ, его прививают вакциной БЦЖ-М с уменьшенным содержанием живых микобактерий. Это снижает риск осложнений.
Особенности вакцинации
Вакцинацию против туберкулеза важно проводить как можно раньше, в первые несколько суток после рождения. Это позволит быстрее активировать иммунитет. Если иммунизация выполняется позже, прививку БЦЖ нельзя совмещать с другими вакцинами. За месяц до и в течение месяца после вакцинации против туберкулезной инфекции не должно быть других прививок. Исключение — прививка против вирусного гепатита B, которую выполняют в роддоме в первые сутки жизни ребенка.
При использовании вакцины БЦЖ особенно важна правильная техника введения препарата. Его вводят на определенную глубину, строго внутрикожно. Неправильная глубина введения провоцирует местные осложнения и снижает эффективность вакцинации. Лучше, если прививку будет делать медперсонал в роддоме. Медсестры в родильных домах постоянно проводят такую вакцинацию и делают ее правильно, а кроме того, ребенок некоторое время после прививки будет оставаться под постоянным контролем врачей. Специальная подготовка для проведения прививки БЦЖ не нужна.
Противопоказания к проведению
Прививку от туберкулеза нельзя делать при наличии следующих противопоказаний:
- вес при рождении меньше 2000 г;
- наличие острых заболеваний (включая внутриутробную инфекцию, тяжелые поражения нервной системы, гнойно-септические и другие заболевания);
- злокачественные новообразования;
- первичный иммунодефицит;
- применение иммунодепрессантов или лучевой терапии (вакцинация выполняется спустя 6 месяцев или более после завершения терапии);
- генерализованная БЦЖ-инфекция у других детей в семье;
- ВИЧ-инфекция у ребенка или у его матери (если она не принимала антиретровирусную терапию).
Вакцинация в этих случаях проводится после снятия противопоказаний. Для нее может использоваться вакцина БЦЖ-М, для которой риск осложнений меньше.
Какие осложнения могут быть после вакцинации БЦЖ
Осложнения после этой прививки делятся на две категории:
- Тяжелые осложнения, связанные с генерализацией (распространением) инфекции. Вакцина БЦЖ — это, как уже отмечалось выше, живая культура. Поэтому она может вызывать специфические (т.е. связанные с развитием туберкулезного процесса) осложнения. Как правило, такие осложнения бывают связаны с неправильным отбором детей на прививку. Однако хотелось бы подчеркнуть, что риск подобных осложнений гораздо меньше, чем риск заболевания у невакцинированного ребенка.
- Более легкие осложнения, связанные, в том числе, с нарушением техники введения вакцины или с некачественной вакциной.
Среди основных возможных осложнений после БЦЖ:
При появлении любого из вышеперечисленных осложнений, а также других необычных явлений, следует немедленно обратиться к врачу.
Вакцинация от туберкулеза: за и против
Вакцина БЦЖ применяется давно, и у нее есть ряд недостатков, но пока она остается самым эффективным способом профилактики туберкулеза.
При этом именно эффективность иммунопрофилактики вызывает больше всего споров:
- Вакцина БЦЖ не предотвращает заражения туберкулезной инфекцией.
- Если человек уже инфицирован микобактериями туберкулеза, вакцина не защищает от перехода болезни в активную форму. По данным ВОЗ, носителями микобактерий туберкулеза является треть людей во всем мире.
- Сформированный вакциной иммунитет слабеет за несколько лет. Ревакцинация не всегда эффективна, и из-за этого взрослые люди уязвимы и к первичному заражению, и к переходу латентной формы туберкулеза в активную форму.
- Вакцина БЦЖ у детей предотвращает до 80% тяжелых форм туберкулезной инфекции.
- Вакцинация на 65% снижает количество случаев смерти, связанных с туберкулезом. Заболеваемость туберкулезным менингитом снижается на 64%, диссеминированным туберкулезом (с образованием множественных очагов поражения тканей легких) — на 78%.
- Даже в случае заражения у тех, кто был привит, болезнь протекает намного легче, с меньшим количеством осложнений.
Спорной является и безопасность вакцины БЦЖ. Ее применение действительно может давать ряд осложнений, но они возникают очень редко. Чаще встречаются местные реакции, связанные с нарушением техники введения препарата, но даже они мало распространены.
Заключение
Туберкулезная инфекция остается распространенной и опасной болезнью. Прививка вакциной БЦЖ — один из самых надежных способов ее профилактики. БЦЖ является единственным средством иммунизации, и важно сделать эту прививку как можно раньше.

Почему дети заболевают туберкулезом, и где происходит встреча с инфекцией
Первичным туберкулезом часто заболевают дети, оказавшиеся в очаге инфекции, когда микобактерии активно выделяет кто-то из его близкого окружения – родственники, педагоги. Особенно опасно, если это лекарственно устойчивая бактерия, потому, что ребенок сразу инфицируются именно лекарственно устойчивой палочкой. Поэтому следует принять все меры, чтобы ребенок меньше инфицировался, а если инфицировался, то не заболел.
Кто в группе риска
Если у взрослых в развитии туберкулеза значительную роль играют социальные и поведенческие факторы, то для детей более актуальны медицинские. Так, больные сахарным диабетом, по данным ВОЗ, заболевают туберкулезом в 4-5 раз чаще. Вероятность заболеть повышается у детей с хроническими заболеваниям легких, желудочно-кишечного тракта, а также у больных, которые получают гормональную терапию или лекарственные препараты, подавляющие иммунитет. Так, в Клинических рекомендациях по лечению ревматоидного артрита у детей, есть раздел, касающийся профилактики туберкулеза у детей, получающих иммуносупрессивную терапию (например, генно-инженерные препараты). Иммунодиагностика таким детям должна проводиться не реже двух раз в год. В группу повышенного риска входят дети с ВИЧ-инфекцией, у которых нет иммунной защиты – вероятность развития туберкулеза при ВИЧ-инфекции увеличивается в 30-40 раз.
Какие формы туберкулеза встречаются у детей
Латентная форма
В большинстве случаев это латентная форма, активная форма в этом возрасте встречается в 5-6% случаев. Латентная форма туберкулеза может скрывать признаки заболевания длительное время.Несмотря на то, что ребенок с такой формой болезни практически ее не ощущает и не заразен для окружающих, инфекция медленно разрушает его организм, а болезнь переходит в хроническую стадию.
Активная форма
Специфика детского туберкулеза стоит в том, что в большинстве случаев дети не являются бактериовыделителями, поскольку поражаются внутригрудные лимфатические узлы, находящиеся внутри организма, а не легкие. От генерализованных форм детей защищает прививка БЦЖ.
Петрификат
Иногда детский организм самостоятельно справляется с болезнью, и ее локальная форма не выливается в большое заболевание. Следы перенесенного туберкулеза в виде кальцинатов в легочной ткани врачи уже видят на снимках постфактум. Но это все равно не полное излечение – в легком у ребенка формируется так называемый петрификат – очаг, который представляет собой спящую микобактерию, покрытую известковой оболочкой. И как только в организме происходят какие-то изменения, и падает иммунитет, инфекция активизируется. Особенно опасно это для подростков, у которых из-за гормональной перестройки туберкулез протекает очень стремительно.
Клинические проявления
Явные симптомы туберкулеза – кашель, кровохарканье – говорят о том, что это уже далеко зашедшая стадия,наступила деструкция и идет распад легочной ткани. А на начальном этапе болезнь проходит скрыто. Самые первые проявления совершенно не примечательны и характерны для многих заболеваний – это беспричинное похудание, отсутствие или снижение аппетита, слабость, недомогание.Иногда могут проявиться признаки, схожие с симптомами простуды. Насторожить родителей должен кашель, который, несмотря на лечение, продолжается дольше 2-3 недель. А также любые признаки интоксикации – повышение температуры, ночная потливость, затяжные катаральные явления. Если это состояние не проходит за 7-14 дней, стоит сделать Диаскинтест. Положительный результат пробы служит главным сигналом наличия заболевания.
Скрининг
Кожные пробы проводятся и для скринингового наблюдения, необходимого для того, чтобы вовремя выявить факт инфицированности. Регулярный скрининг – выявление живых (проснувшихся или недавно попавших в организм) микобактерий очень важен еще и потому, что у детей туберкулез долго протекает бессимптомно. И скрининг позволяет поймать тот момент, когда ребенок уже проконтактировал с микобактерией туберкулеза, и предпринять необходимые профилактические меры, а также отобрать детей для углубленной диагностики на выявление уже развившегося заболевания в его начальной стадии.
Самый старый скрининговый метод, долго остававшийся единственным – хорошо всем известная проба Манту. Сегодня появился еще один метод скринингового наблюдения с помощью кожных проб – Диаскинтест. Новая кожная проба более специфична, чем проба Манту, которая реагирует, как на саму туберкулезную инфекцию, так и на вакцину БЦЖ (поствакцинальная аллергия), а иногда и на другую инфекцию, присутствующую в организме. Проба Манту очень чувствительна, но дает много ложноположительных результатов. А вот Диаскинтест помогает выявить только саму активную размножающуюся вирулентную туберкулезную инфекцию. И в этом его ценность.
Почему не отменяют пробу Манту
На сегодняшний день в стране действует приказ Минздрава № 124н, согласно которому всем школьникам с 7 лет следует ежегодно проводить Диаскинтест. Но для детей до 7 лет остается проба Манту, которая необходима для принятия решения о ревакцинации. Дело в том, что после проведения новорожденному вакцинации БЦЖ в организме ребенка формируется поствакцинный иммунитет. Этот иммунитет постепенно угасает. Но пока он полностью не угас, ревакцинацию проводить ни в коем случае нельзя. Наличие этого иммунитета у ребенка можно определить только по пробе Манту (она будет положительной).
Диаскинтест же будет оставаться отрицательным у пациентов, которым делали вакцину БЦЖ, ведь он на нее, в отличие от Манту, не реагирует. Диаскинтест реагирует только тогда, если в организме есть именно инфекционные бактерии, способные вызвать заболевание, а не бактерии, содержащиеся в вакцине. То есть, по Диаскинтесту нельзя судить, нуждается ли ребенок в ревакцинации или нет.
Возможны три ситуации:
- Если и Диаскинтест, и проба Манту у ребенка в 6-7 лет отрицательные – значит в организме нет защиты от инфекции, и нет палочек Коха – то есть необходима ревакцинация.
- Если Диаскинтест отрицательный, а проба Манту положительная – то в организме ребенка есть защита от инфекции и дополнительно ревакцинацию проводить не надо.
- Если Диаскинтест положительный – то у ребенка состояние латентной туберкулезной инфекции, то есть в организме есть микобактерии туберкулеза, способные вызвать болезнь и высока вероятность развития заболевания. Ревакцинация противопоказана, необходимо дообследование, наблюдение фтизиатра, профилактического лечение после исключения активного заболевания.
Так как после 7-ми летнего возраста ревакцинация не проводится, то и делать пробу Манту после 7 лет нет необходимости.
Дифференциальная диагностика
Окончательный диагноз ставится не просто, и очень зависит от фазы заболевания. Но вначале проводится дифференциальная диагностика – для того, чтобы окончательно убедиться, что это туберкулез, а не что-либо другое. А также, чтобы не пропустить болезнь при отрицательных результатах других диагностических тестов (при аутоиммунных заболеваниях или иммуносупрессивной терапии). Обычно это тест T-SPOT.TB (по крови из вены) и мультиспиральная компьютерная томография.
Существует еще один альтернативный диагностический тест QuantiFERON. Однако, он уступает T-SPOT.TB, особенно в сложных случаях (при обследовании детей раннего возраста, стариков, ВИЧ-инфицированных, при иммуносупрессивной терапии). Эти тесты можно проводить и в качестве скринингового обследования. И этой возможностью по желанию (и за свой счет) могут воспользоваться родители, которые не хотят делать своим детям кожные пробы. В общелечебной сети приоритет отдается более простым и доступным методам.
Отказ от скрининга = отказ от лечения
Кожные пробы – это не прививка, а всего лишь скрининговый инструмент. При этом ребенку не вводятся ни живые, ни инактивированные микробы. И уж тем более никого не заражают туберкулезом, как любят пугать антипрививочники. В состав используемого в пробе Манту туберкулина входит вытяжка из микобактерий туберкулеза, содержащая белки, липиды и иные компоненты. Препарат Диаскинтест включает в себя только два белка – антигены возбудителя туберкулеза.
Врачи терпеливо разъясняют это родителям, но не всегда могут их переубедить. Поэтому такие люди должны знать: используя свое право на отказ от скрининга, они автоматически отказывают своему ребенку в праве на лечение. Как можно лечить не выявленную болезнь?
Кроме того, они ограничивают своему ребенку доступ в детский коллектив. Пункт 5.7 действующих с августа 2014 года СанПиНов указывает на то, что дети, не прошедшие иммунодиагностику, не допускаются в образовательные организации – детские сады и школы. Это не противоречит и федеральному закону №27-ФЗ об образовании, в котором прописано, что выбирая особый вид медицинской услуги, родители выбирают и соответствующий вид образовательной услуги. Например, домашнее обучение.
Почему первую прививку БЦЖ делают ребенку уже в роддоме
Отказываться от вакцинации маленьких детей от туберкулеза сразу после рождения очень опасно – сразу после рождения ребенка его сопротивляемость инфекции практически нулевая. А, выйдя из роддома, он попадает в среду, в которой не защищен от встречи с инфекцией. К тому же, еще три месяца уходит на развитие иммунного ответа. Конечно, бывают случаи, когда у новорожденного ребенка есть противопоказания для прививки. И тогда, когда он подрастет, прежде, чем вводить вакцину БЦЖ, ребенку делают кожную пробу, чтобы выяснить, не подхватил ли он уже инфекцию. Прививать детей от туберкулеза можно только до двух лет. И только после Манту с отрицательным результатом.
Прививка БЦЖ не защищает полностью от туберкулеза, но предотвращает развитие у детей его тяжелых, смертельных форм. Ее цель – ограничить развитие заболевания лимфатической системой, которая хорошо развита у детей раннего возраста (чем старше становится ребенок, тем хуже справляются лимфоузлы с защитной функцией, поэтому у подростков развивается уже легочный туберкулез). Ревакцинация проводится в семилетнем возрасте. Но к этому возрасту отрицательную пробу Манту имеют уже не более половины детей. Остальные уже не подлежат ревакцинации. По этой же причине прививку БЦЖ не делают взрослым – к 20 годам практически все люди уже инфицированы, и вакцинировать уже некого.
Читайте также:

