Гиперплазия желудка и хеликобактер пилори
Обновлено: 10.05.2024
Какие классификации гастрита существуют в настоящее время?
Каковы схемы лечения хронического гастрита?
Понятие
В РФ статистических данных относительно распространенности хронического гастрита нет. В странах с развитой статистикой хронический гастрит фиксируется у 80—90% больных, причем атрофический гастрит встречается в 5% случаев — у лиц моложе 30 лет, в 30% случаев у лиц в возрасте от 31 до 50 лет и в 50—70% случаев — у лиц старше 50 лет.
Согласно выводам ленинградской школы гастроэнтерологов, этиологические факторы развития первичного (или собственного) хронического гастрита носят экзогенный характер (Helicobacter pylori (НР), желчные кислоты и лизолецитин в желудочном содержимом, погрешности в диете, курение и злоупотребление алкоголем, длительный нервно-психический стресс, продолжительный прием лекарственных средств, повреждающих слизистую оболочку, профессиональные вредности: металлическая и хлопковая пыль, пары концентрированных щелочей и кислот и т. д. (их около 30)) и эндогенный характер (наследственная предрасположенность, хронические инфекции, аутоимммунные заболевания, патология эндокринной системы, болезни обмена веществ, хроническая пищевая аллергия; хронические заболевания сердца, протекающие с декомпенсацией по большому кругу кровообращения и последующей тканевой гипоксией слизистой оболочки желудка и т. д. (их около 45)).
Патогенез хронического гастрита представлен бактериальными, иммунологическими и нейрогуморальными нарушениями, проявляющимися на уровне слизистой оболочки желудка в виде поверхностного и атрофического гастрита. Учитывая, что патогенез хронического гастрита для каждой формы и типа заболевания имеет свои особенности, необходимо рассмотреть классификацию хронического гастрита и в первую очередь остановиться на морфологической классификации. Согласно последней, выделяют острый, хронический, а также особые формы хронического гастрита.
Острый гастрит, как правило, является следствием острой инфекции и острого повреждения слизистой оболочки желудка химическими и токсическими факторами (концентрированными щелочами и кислотами, большими дозами алкоголя и т. д.). Эти формы гастрита нередко протекают с тяжелыми осложнениями, в связи с чем лечением острого гастрита занимаются не гастроэнтерологи, а инфекционисты, наркологи, хирурги.
Пилорическая метаплазия фундальных желез внешне напоминает пилорические железы желудка. Однако имеется и различие — отсутствие шеечных отделов желез, высокая устойчивость к атрофии, G-клетки встречаются крайне редко, на порядок больше суммарного белка. Пилорическую метаплазию обнаруживают, как правило, при атрофическом гастрите на месте зажившей эрозии или язвы. Реснитчатая метаплазия — это скопления клеток поверхностного или железистого эпителия, имеющего длинные и тонкие реснички. Впервые она была описана профессором Шивасаки в 1986 г. Эту метаплазию часто обнаруживают на участках с кишечной метаплазией, однако ее связь с раком желудка не подтверждена.
В 1993 г. профессор C. Doglioni с соавт. впервые описал панкреатическую метаплазию слизистой оболочки желудка. Клетки панкреатической метаплазии похожи на ацинарные клетки поджелудочной железы. В подслизистом слое и мышечной оболочке желудка часто обнаруживают гетеротопическую ткань поджелудочной железы, которую обозначают как хористома. Хористома и панкреатическая метаплазия клеток поверхностного эпителия представляют собой разные структуры. Связи панкреатической метаплазии с опухолями желудка не установлено.
Истинным предраковым изменением слизистой оболочки желудка считается дисплазия эпителия, при этом выделяют три степени дисплазии [1]: слабую, умеренную и выраженную (или тяжелую). Наиболее опасной в плане трансформации в рак желудка считается тяжелая дисплазия эпителия. Слабая и умеренная дисплазии эпителия трудно отличимы от воспалительной дисплазии, обнаруживаемой в краях эрозий и язв (при воспалительной дисплазии, в отличие от истинной, в эпителии обнаруживаются многочисленные лейкоциты). При заживлении эрозий и язв воспалительная дисплазия исчезает, а истинная всегда остается. Проспективное мультицентровое изучение дисплазии [4] дало основание для объединения слабой и умеренной дисплазии в одну группу.
В классификации оставлены только две степени — слабая и тяжелая. При слабой дисплазии, выявленной у больных старше 60 лет на фоне выраженного гастрита, рекомендуется проведение повторных ЭГДС и биопсий каждые 6—12 месяцев [1]. Тактика ведения больных с тяжелой дисплазией определена в монографии Л. И. Аруина и соавт. [1]. При обнаружении тяжелой дисплазии больному необходимо в течение 10 дней повторить ЭГДС одним и тем же эндоскопистом со взятием множественных биопсий. При определении тяжелой дисплазии вновь рекомендовано каждые три месяца в течение года делать ЭГДС со взятием многочисленных биопсий. Если при одном из иследований в биопсиях тяжелой дисплазии не обнаружено, динамическое наблюдение с трехмесячным проведением ЭГДС в течение года тем не менее следует продолжить. Ибо известно, что тяжелая дисплазия эпителия трансформируется в рак in situ в сроки от трех месяцев до 20—30 лет [1]. Существует другая классификация дисплазий эпителия, в которой выделяют дисплазию низкой степени и дисплазию высокой степени [1]. Известно, что дисплазия — это истинная неоплазия, только без признаков инвазии.
В 2000 г. появилась новая классификация дисплазий слизистой оболочки желудка — согласованная Международная (Венская) классификация эпителиальных неоплазий пищеварительного тракта [2].
Лимфоцитарный гастрит возникает на фоне аутоиммунного хронического гастрита тела желудка (или смешанного хронического пангастрита) и характеризуется многочисленными интраэпителиальными лимфоцитами, которые обнаруживаются среди клеток поверхностного эпителия (на 100 эпителиальных клеток фиксируется 30 и более лимфоцитов, в норме они не определяются). Патогенез этой формы гастрита до конца неясен. Полагают, что это особая иммунологическая реакция на НР, который в слизистой оболочке желудка не обнаруживается.
Гранулематозный гастрит характеризуется наличием мелких гранулем в собственной пластинке слизистой оболочки желудка на фоне поверхностного или атрофического гастрита. Чаще всего речь идет о болезни Крона, саркоидозе, болезни Вегенера желудочной локализации. Аналогичную картину могут дать паразиты или инородные тела желудка.
Эозинофильный гастрит возникает на фоне поверхностного или атрофического гастрита и характеризуется очаговыми и/или диффузными скоплениями эозинофилов в собственной пластинке слизистой оболочки желудка. Этот гастрит встречается, как правило, при аллергических заболеваниях и аллергозах. Нередко в качестве причинного фактора выступают пищевые аллергены или паразиты.
Инфекционный гастрит характеризуется очаговыми и/или диффузными скоплениями бактерий (гастроспириллы), вирусов (цитомегаловирусы), грибов (типа Candida) и моноцитарной реакцией на них в собственной пластинке слизистой оболочки желудка.
С 1968 г. отечественные гастроэнтерологи при постановке диагноза берут на вооружение клинико-морфологический подход, предполагающий выделение хронического гастрита с сохраненной, повышенной функцией желудка (в теле желудка — неизмененная слизистая оболочка, поверхностный гастрит), с умеренной или выраженной секреторной недостаточностью (в теле желудка — мультифокальный или очаговый, диффузный атрофический гастрит).
Для оценки Сиднеевской классификации в конце 1994 г. в Хьюстоне (США) была выделена рабочая группа, в которую вошли 20 ведущих морфологов-гастроэнтерологов, специализирующихся в области изучения патологии желудка. В результате Сиднеевская классификация была принята в качестве основной. Дополнения же сводились к следующему:
Согласно предложенным классификационным дополнениям, в качестве основной формы хронического гастрита выделяют аутоиммунный хронический гастрит тела желудка, который характеризуется очаговым или диффузным атрофическим гастритом тела желудка и неизмененной слизистой оболочкой или поверхностным гастритом антрума желудка (НР-негативный). У этой группы больных определяются: аутоантитела типа IgG к париетальным клеткам (в 95% случаев), аутоантитела типа IgG к ферменту К/Na-АТФазе в париетальной клетке (в 70% случаев) с развитием умеренной или выраженной секреторной недостаточности; аутоантитела типа IgG к внутреннему фактору Кастла
Клинические проявления хронического гастрита
Клиническая картина хронического гастрита характеризуется как местными, так и общими расстройствами, как правило, появляющимися в периоды обострений. Местные признаки характеризуются симптомами желудочной диспепсии (тяжесть и чувство давления, полноты в подложечковой области, появляющиеся или усиливающиеся во время еды или вскоре после еды; отрыжка, срыгивание, тошнота, неприятный привкус во рту, жжение в эпигастрии, нередко изжога, свидетельствующая о нарушении эвакуации из желудка и забросе желудочного содержимого в пищевод). Эти проявления чаще возникают при определенных формах хронического антрального гастрита, которые ведут к нарушению эвакуации из желудка, повышению внутрижелудочкового давления, усилению желудочно-пищеводного рефлюкса и обострению всей перечисленной симптоматики.
При хроническом гастрите тела желудка проявления встречаются нечасто и сводятся преимущественно к тяжести в эпигастральной области, возникающей во время или вскоре после еды.
Все эти проявления могут служить основой для диагностики хронического гастрита либо оценки стадии болезни или ее осложнений.
Диагностика хронического гастрита включает:
- эндоскопический метод со взятием диагностических биопсий;
- морфологические методы: гематоксилином и эозином, гистохимические окраски, окраска по Гимзе без дифференцировки на НР, иммуноморфологический с окраской антисыворотками к гастрину, соматостатину и гистамину;
- методы, направленные на выявление НР: морфологический, уреазный (кло-тест, дыхательный), иммуноморфологический на антигены НР, иммунологический, бактериальный с посевами на среды;
- радиоиммунологический метод с определением в крови гастрина и пепсиногена 1;
- иммунологический метод с применением иммуносорбентов: АТ к париетальным клеткам, АТ к ферменту К/Na-АТФазы в париетальных клетках, АТ к внутреннему фактору Кастла, АТ к НР;
- определение кислотной продукции: фракционное желудочное зондирование, виды рН-метрии;
- лабораторный метод: общий анализ крови, определение уровня уропепсина в моче.
Примеры формулировки диагноза
- Острый геморрагический гастрит [К 29.0].
- Хронический гастрит антрума желудка (хронический антральный гастрит) хеликобактерный* с повышенной секреторной функцией* (или нормальной секреторной функцией*) в фазе обострения (затухающего обострения или ремиссии) [К.29.5].
- Хронический гастрит тела желудка (хронический фундальный гастрит) аутоиммунный* с умеренной (или выраженной) секреторной недостаточностью* в фазе обострения (затухающего обострения или ремиссии) [К 29.5].
- Хронический смешанный пангастрит хеликобактерный*
- нормальной секреторной функцией* (или умеренно выраженной секреторной недостаточностью*) в фазе обострения (затухающего обострения или ремиссии) [К 29.5].
Принципы лечения хронического гастрита
Учитывая наличие клинически и морфологически различающихся форм хронического гастрита, способы лечения также варьируют в зависимости от этиологии, морфологии, стадии болезни.
Диетические мероприятия должны включать в себя: назначение щадящей диеты в период обострения заболевания, подразумевающей механические, химические, объемные ограничения. Эти ограничения действуют только в период обострения; по мере его купирования питание должно становиться полноценным с соблюдением стимулирующего принципа в период ремиссии у больных с подавленной или с пониженной кислотной продукцией.
Лечение отдельных форм хронического гастрита
Аутоиммунный фундальный атрофический гастрит (тип А)
Условно выделяют следующие стадии болезни:
- начальную;
- развернутую (активную, прогрессирующую);
- стадию стабилизации процесса;
- стадию осложнений (ахилию с проявлениями нарушенного желудочного пищеварения; с нарушением моторики выходного отдела желудка; с нарушением кроветворения и развитием В12-дефицитной анемии иногда в сочетании с фуникулярным миелозом; с выраженной гиперфункцией и гиперплазией антральных G-клеток и развитием нейроэндокринных опухолей (карциноидных).
Если диагноз аутоиммунного фундального гастрита подтвержден и фиксируется начальная стадия болезни с сохраненной секреторной функцией желудка при серьезном нарушении иммунных процессов, может быть предпринята попытка лечения глюкокортикоидными гормонами (короткими курсами, средними дозами, не превышающими 30 мг преднизолона в сутки при условии проведения иммунных тестов). При отсутствии эффекта проведения повторного курса такой терапии нецелесообразно, так как повторное или продолжительное лечение глюкокортикоидными гормонами индуцирует атрофию слизистой оболочки желудка [3].
Подобная возможность лечения сохраняется и в прогрессирующей стадии болезни, а также у больных с сохраненной секреторной функцией желудка.
На стадии стабилизации процесса, при отсутствии клинических проявлений, больные в лечении не нуждаются.
При развитии осложнений при нарушенном желудочном пищеварении может быть назначен желудочный сок по одной столовой ложке на полстакана воды, небольшими глотками во время еды в сочетании с полиферментными препаратами (лучше креон или панцитрат).
При развитии В12-дефицитной анемии проводится лечение витамином В12 (начальный курс по 2000 мкг, восемь—десять инъекций ежедневно). Эта норма, по существу, покрывает годовую потребность в витамине В12. При анемии с явлениями фуникулярного миелоза ежедневная доза увеличивается до 400—500 мкг. В периоде ремиссии проводится поддерживающая терапия по 100 мкг два раза в неделю. Спустя четыре—шесть месяцев от начала лечения витамином В12 может развиться или проявиться дефицит железа, в этом случае в комплекс терапевтических мер необходимо ввести препараты железа (короткими курсами).
При установлении факта гиперфункции и гиперплазии антральных G-клеток необходимо фиксировать внимание на очаговых фовеолярных гиперплазиях слизистой оболочки желудка и, при обнаружении карциноидных опухолей — удалить их (способ удаления должен соответствовать локализации, размерам, активности и распространенности в толщу стенки).
Хронический антральный гастрит, НР-ассоциированный (тип В)
Хронический химико-токсикоиндуцированный или желчный рефлюкс-гастрит (тип С)
Этот диагноз объединяет большую группу больных, включающую пациентов с резецированным желудком, людей, получавших нестероидные противовоспалительные препараты, а также пациентов с рефлюксом дуоденального содержимого, страдающих алкогольной болезнью. Терапия зависит от основного причинного фактора. Так как желчные кислоты и лизолецитин оказывают повреждающее действие только при наличии соляной кислоты, то, в зависимости от выраженности клинических проявлений, могут быть использованы блокаторы кислотной секреции (выбор которых зависит от кислотной продукции). При рефлюкс-гастрите препаратом выбора является магалфил 800 (в суточной дозе 3200—4800 мг или четыре—шесть таблеток); полные лечебные дозы больной получает до фиксации стадии ремиссии, затем необходимо продолжить прием препарата в поддерживающих дозах: одну-две таблетки в сутки (связывающая способность препарата желчных кислот не уступает холестирамину). Следовательно, в данной ситуации магалфил 800 является препаратом выбора. Если решается вопрос о целесообразности длительного лечения НПВС и обнаруживается НР-ассоциированный, антральный гастрит, то следует провести эрадикационное лечение — это уменьшает количество осложнений, либо проводить данную терапию на фоне блокаторов кислотной продукции. Симптоматическая терапия проводится по обычным принципам и включает как диетические мероприятия, так и прием прокинетиков (мотилак, мотилиум), нормализацию пассажа химуса по кишечнику, использование препаратов поглощающих газ (кремний-содержащих), нормализацию дисбиоза и стула при наклонности к запору.
Прочие формы хронического гастрита
Литература.
О. Н. Минушкин, доктор медицинских наук, профессор
И. В. Зверков,
УНЦ МЦ УД Президента РФ, Москва
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
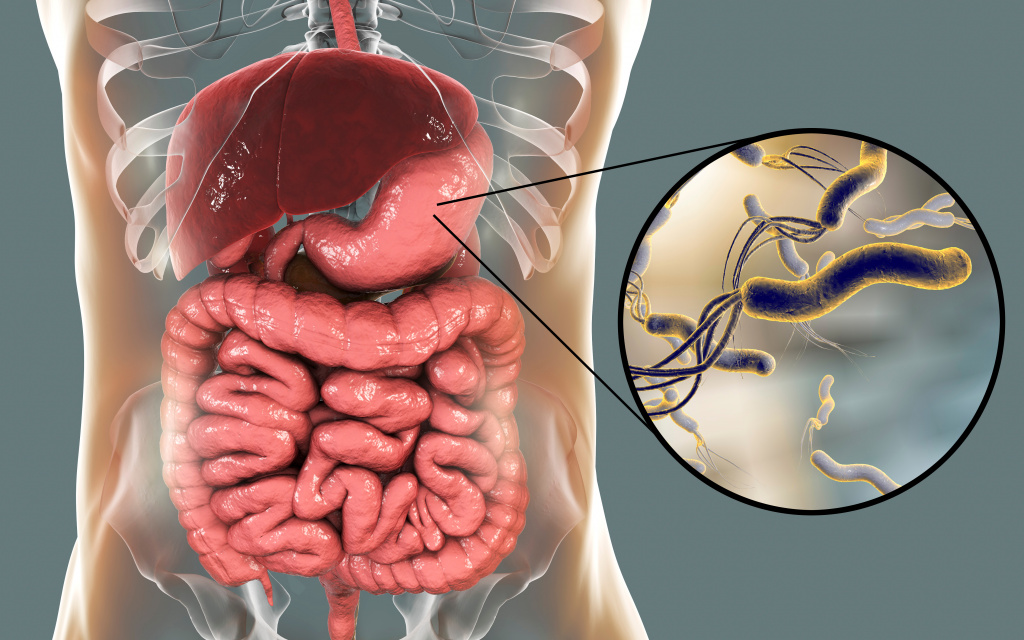
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.

Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Даже те, у кого со здоровьем всё в порядке, хорошо знают о существовании этой бактерии. А уж если возникают проблемы с желудком, что по весне –не редкость, пытаются понять не виноват ли в этом пресловутый Хеликобактер
В борьбе за выживание
Считается, что в активе Хеликобактера целый букет болезней. Острый и хронический гастрит, в том числе эрозивный, дуоденит, язвенная болезнь желудка и двенадцатиперстной кишки, всё больше данных, что хроническое воспаление слизистой является одной из главных причин развития рака и злокачественной лимфомы желудка.
В чём же причина настолько агрессивного поведения бактерии к организму-хозяину, засчёт которого она существует? Всё просто - в желании выжить. Кислая среда желудка губительна для всего живого, и чтобы создать вокруг себя зону, свободную от кислоты, Хеликобактер активно синтезирует уреазу, - фермент, который расщепляет мочевину с образованием аммиака, а тот, в свою очередь нейтрализует кислоту, создавая комфортный для бактерии pH. Но вместе с этим аммиак поражает клетки слизистой, вызывая их воспаление и гибель. Дополнительное влияние оказывают не менее агрессивные ферменты - муциназа, протеаза и липаза, а также аутоиммунная реакция организма, при которой лимфоциты по ошибке атакуют собственную слизистую.
Быстрый и проворный
В начале 80-х годов прошлого века австрийский паталагоанатом Перт Робин Уоррен обнаружил на слизистой оболочке желудка колонии ранее неизвестных бактерий. И отметил чёткую закономерность - там, где обитали незнакомцы, присутствовало воспаление - гастрит, эрозии или язвы.
Открытием заинтересовался стажёр Барри Маршалл – ему даже удалось вырастить в лаборатории культуру этих бактерий. Так были получены образцы Helicobacter pylori, одного из самых известных микроорганизмов 20-го века. А затем в ходе эпидемиологического исследования учёные доказали - заселение желудка этой бактерией всегда связано с воспалением слизистой, и чаще всего с язвенной болезнью.
Из блефа в аксиому
Как это часто бывает в медицине, тотальное неприятие версии инфекционной природы язвенной болезни, сменилось возведением её в непреложную истину. Проблему язвенной болезни посчитали решённой, ведь стоит провести эрадикацию (уничтожение) возбудителя, как сразу же исчезнет основной фактор риска. Учёные разработали два вида терапии - трёх и четырёхкомпонентную, в зависимости от количества применяемых лекарств и сроков лечения. Две-три недели и результаты обследования показывают - Хеликобактера в организме больше нет. Хотя, сначала его необходимо обнаружить.
Я иду искать
подготовка к гастроскопии с биопсией на Helicobacter pylori:
-Гастроскопия с тестом на Хеликобактера предусматривает 3-х дневную диету с исключением продуктов, раздражающих пищеварительный тракт (нельзя жареные, копченые, соленые, жирные и острые блюда).
-Запрещаются газированные напитки, кофе, алкоголь. Желательна диета на основе легкоусвояемых продуктов (каши на воде, отварное мясо, йогурты, овощные салаты и т. д.).
-Последний прием пищи – не позднее, чем за 12 часов до проведения гастроскопии.
-За 3 часа до начала исследования необходимо отказаться от сигарет. За 2 часа до процедуры следует прекратить приём жидкости и лекарств.
- перед процедурой не следует чистить зубы, применять ополаскиватели или освежители для полости рта, а также жевательные резинки.
Лечим всех или есть исключения?
Если инфекция обнаружена, стоит ли как можно быстрее начинать лечение? В начале 2000-х любой гастроэнтеролог ответил бы - конечно. Но как мы говорили, часто вслед за отрицанием новой теории приходит время восторженного поклонения, а затем, по мере накопления опыта, всё становится на свои места. Так получилось и в этот раз.
Данные многочисленных исследований показали, что распространённость Хеликобактера очень высокая, им инфицированы до 50 процентов населения развитых стран. Но болеют далеко не все: в 90 процентах случаев бактерия не оказывает на слизистую желудка значимого воздействия, симптомы гастрита или язвы отсутствуют. Значит, у остальных защитные свойства слизистой оболочки выражены настолько хорошо, что продукты жизнедеятельности бактерии для неё не опасны.
И наоборот: у больных с язвенной болезнью желудка Хеликобактер обнаруживается в 50 процентов случаев, с язвенной болезнью двенадцатиперстной кишки – около 60. Значит, существуют и другие причины для поражения слизистой и об абсолютном доминировании Хеликобактера речь не идёт.
Как же поступить тем, кто страдает от хронического гастрита или язвенной болезни, или узнал о наличии Хеликобактера случайно, в ходе обследования?
Если же бактерия есть, а признаков воспаления нет, вопрос об её уничтожении вызывает сомнение. Во-первых, двух или трёхнедельный курс антибиотиков способен вызвать неприятные побочные эффекты - активацию грибковой инфекции в виде молочницы или кандидоза полости рта, дисбактериоз кишечника, от которого затем придётся долго избавляться. Кроме того, чтобы лечение оказалось эффективным, лекарства придётся пить всем членам семьи, включая пенсионеров и маленьких детей - близкие родственники неминуемо являются носителями той же самой бактерии, и даже если вы пройдёте лечение, то через посуду и поцелуи вы обязательно подхватите Хеликобактера заново.
Иногда может быть полезен
Некоторые специалисты ориентируются на концентрацию возбудителя по результатам биопсии - если его слишком много, то предлагают пройти лечение, даже если отсутствуют симптомы воспаления. Другие рекомендуют определять штамм Хеликобаткера с помощью ПЦР и в случае выявления наиболее агрессивных вариантов в любом случае начинать лечение. Как бы то ни было, мнение о том, что Хеликобактер вызывает повреждение не у всех, чьи желудки населяет, в последние годы перевесило чашу весов. И сейчас во многих лабораториях мира идут исследования по выявлению врождённых или приобретённых методов защиты от Хеликобактера, которые могут присутствовать у некоторых из нас.
Получены данные, что людям с пониженной кислотностью бактерии причиняют меньше вреда, возможно, уменьшая количество вырабатываемой уреазы, у некоторых бактерию под контролем долгие годы держит иммунитет, и она не в силах реализовать все свои патогенные свойства. Тем более, в последнее десятилетие начали появляться данные, свидетельствующие об отрицательном эффекте тотальной стерилизации пациентов от Хеликобактера.
Так, в экспериментах на грызунах доказано, что инфицирование их Хеликобактером приводило к значительному уменьшению симптомов бронхиальной астмы. Если же мышей излечивали с помощью антибиотиков, симптомы астмы снова усиливались.
Крупный эксперимент, проходивший в течение 12 лет и включающий в себя более 10 тысяч испытуемых, показал, что наличие в организме Хеликобактера с цитотоксин ассоциированным геном (один из штаммов бактерии) в 2 раза снижает риск заболеть раком лёгких или получить ишемический инсульт, хотя и несколько увеличивает вероятность рака желудка.
Доказано, что Хеликобактер стимулирует работу иммунной системы, в частности Т-хелперов, играющих важную роль в профилактике аутоиммунных заболеваний.
ВЫВОДЫ ЗДОРОВЬЯ:
-Хеликобактер живёт рядом с человеком более 15 тысяч лет и населяет желудки практически половины из нас. За это время многие мирно с ним сосуществуют.
-Нередко либо слишком агрессивный штамм бактерии, либо слабые защитные механизмы слизистой, а чаще сочетание этих факторов, приводят к развитию воспаления слизистой желудка и двенадцатиперстной кишки.
-Самый точный метод диагностики, особенно если вас часто беспокоят изжога, отрыжка, боли в животе, то есть характерные для поражения слизистой симптомы - ФГДС (гастроскопия) с биопсией на
Helicobacter pylori. Если подтвердится и наличие Хелкобактера, и воспалительные изменения - надо проводить лекарственную эрадикацию и избавляться от бактерии.
-Большинство случаев язвенной болезни желудка и двенадцатиперстной кишки по-прежнему связаны с Хеликобактером, при обнаружении язвы с большой долей вероятности потребуется пройти курс антибиотиков.
В 1% случаев длительное инфицирование Хеликобактером заканчивается развитием рака желудка.
Стопроцентной точностью обладает лишь один тест – гастроскопия с биопсией на Хеликобактер (так называемый HP –тест).
Многие специалисты считают положительным свойством Хеликобактера его способность противостоять другим кишечным инфекциям.
Cреди способов заражения Хеликобактером не только поцелуи и использование общей посуды с инфицированным, но и занос бактерий с помощью медицинских инструментов. Поэтому важно быть уверенным в хорошей дезинфекции гастроскопов, например, записаться на исследование в утренние часы.
Еще не так давно считалось, что гастрит вызывают неправильное питание, еда всухомятку, стрессы и отсутствие горячего супа на обед. Потом ученые обнаружили связь этой болезни с бактерией хеликобактер пилори — и с тех пор подход к лечению заболеваний ЖКТ кардинально изменился.
Можно ли заразиться через посуду в ресторане, вызывает ли хеликобактер рак и нужно ли избавляться от бактерии, которая живет в организме 80% белорусов, рассказал врач-гастроэнтеролог с 40-летним опытом работы Георгий Матвеевич Усов.

Георгий Усов,
врач-гастроэнтеролог высшей категории
Минского клинического консультативно-диагностического центра,
кандидат медицинских наук
— Что такое хеликобактер? Это патогенная бактерия или условно-патогенная?
— Хеликобактер пилори (Helicobacter pylori) — бактерия, которая была открыта австралийскими учеными Робином Уорреном и Барри Маршаллом. За это открытие в 2005 году они получили Нобелевскую премию.
Хеликобактер — патогенная бактерия. Наличие ее в организме человека приводит к поражению слизистой оболочки желудка и двенадцатиперстной кишки и развитию таких заболеваний, как хронический гастрит, язва желудка и двенадцатиперстной кишки, рак желудка, мальтома желудка.
Сегодня хеликобактер — самая распространенная хроническая инфекция в мире.
— Какие факторы в таком случае провоцируют развитие гастрита, язвы, рака? И могут ли эти болезни возникнуть без участия хеликобактера?
— При наличии хеликобактера у всех людей выявляется какое-либо заболевание желудка. Выявление конкретного заболевания зависит от штамма хеликобактера. Штаммы H. руlori, имеющие в своем составе определенные генотипы, предрасполагают к развитию язвенной болезни и рака желудка. И если язвой желудка и двенадцатиперстной кишки или онкологическими заболеваниями заболевают не все инфицированные люди, то гастритом — все.

Верно и то, что данные болезни могут возникать и без хеликобактер пилори.
- Кроме гастритов, связанных с хеликобактером, имеются гастриты, связанные с забросом содержимого двенадцатиперстной кишки в желудок, так называемые рефлюксные (химические) гастриты, гастриты, связанные с образованием антител к слизистой оболочке желудка (аутоиммунные гастриты).
- Причиной язв может быть прием нестероидных противовоспалительных препаратов, ацетилсалициловой кислоты, изредка нервные факторы, погрешности в еде.
- Причиной раковых заболеваний могут быть погрешности в питании, канцерогенные вещества, поступающие в пищу, курение, наследственная предрасположенность и др.
— Как передается эта бактерия человеку? Можно ли заразиться от животных? А в ресторане через посуду?
— Путь передачи хеликобактера контактно-бытовой. Бактерия передается:
- через недостаточно чистую посуду, когда люди едят из одной тарелки или пьют из одной чашки, едят пищу друг у друга;
- в семье, когда родители пробуют пищу перед тем, как дать ее ребенку, или облизывают соску малыша;
- в случае использования людьми одной зубной щетки;
- через губную помаду;
- при отсутствии мытья рук после туалета и перед едой;
- через сексуальные поцелуи.
Хеликобактер также выявлен у кошек и собак, вследствие чего существует возможность заражения человека от них. Что касается ресторана, то, если грязная посуда плохо обрабатывается, появляется высокая возможность заражения хеликобактером.
— Какой процент людей в Беларуси живет с хеликобактером? Почему этот показатель выше, чем в Западной Европе и США?
— Качественных эпидемиологических исследований по распространению хеликобактера среди населения Беларуси не проводилось. Проводились лишь относительно небольшие исследования среди населения отдельных областей и отдельных групп населения.
Считается, что распространенность хеликобактера среди белорусов составляет около 70-80%.
Среди населения РФ по ряду исследований в отдельных российских регионах распространенность составляет от 65 до 90%. Данный показатель выше, чем в Западной Европе и США, в связи с недостаточно качественным соблюдением гигиены в нашей стране.

— Какие симптомы должны заставить человека сдать анализ на хеликобактер? Какие из них неочевидные, не связанные напрямую с ЖКТ?
— Диспепсические расстройства (боли, жжение в эпигастральной области — верхних отделах живота, тошнота, плохой аппетит, тяжесть в эпигастральной области, рвота и т. д.) требуют обследования на хеликобактер.
В некоторых случаях хеликобактер может быть причиной также:
- железодефицитной анемии;
- халитоза (плохого запаха изо рта);
- крапивницы.
Однако следует помнить, что данные заболевания могут возникать и по множеству других причин.
— Какие анализы на выявление хеликобактер существуют? Какие из них самые объективные?
— Существует несколько разновидностей анализов.
- Гистологическое исследование биопсийного материала из слизистой желудка, причем следует исследовать слизистую как антрального отдела, так и тела желудка.
- Быстрый уреазный тест. Тест выполняется в момент гастроскопии. Биопсия слизистой берется из полости желудка, помещается в среду, содержащую мочевину и такой индикатор, как феноловый красный. Уреазы преобразуют мочевину в аммиак, вследствие чего повышается рН среды, и желтый цвет образца (отрицательный) меняется на красный (положительный).
- С13-уреазный дыхательный тест на немецкой аппаратуре, достоверность которого более 92%.
- Российская модификация дыхательного теста — хелик-тест, достоверность которого, по данным ряда российских авторов, составляет от 30 до 80%.
- Определение антител к хеликобактеру IgM и IgG в крови.
- Исследование антигенов хеликобактера в кале.

Самыми объективными из анализов являются гистологический тест, С13-уреазный дыхательный тест на аппаратуре немецкой фирмы FAN, исследование антигенов хеликобактера в кале и быстрый уреазный тест. Исследование крови на антитела к хеликобактер пилори приемлемо при первичном исследовании до лечения хеликобактера. В то же время для контрольного исследования оно не годится, так как антитела к хеликобактеру остаются повышенными в течение нескольких лет в крови после излечения от хеликобактера, давая ложноположительный результат.
Хелик-тест из-за низкой достоверности нигде в мире, кроме нескольких стран СНГ, не применяется.
— Что делать, если анализ положительный? Влияет ли, например, количественное значение антител в крови на степень опасности бактерии для здоровья?
— При положительном анализе на хеликобактер решается вопрос о проведении антихеликобактерной терапии. На степень опасности для здоровья количественное значение хеликобактера существенного значения не имеет, ибо высокая обсемененность хеликобактером в ряде случаев в наших исследованиях приводила к значительно меньшим изменениям слизистой оболочки, чем низкая, или существенно не отличалась. Причина — в индивидуальной резистентности (восприимчивости) организма к хеликобактеру.
При незначительных превышениях IgA желательно провести другой метод исследования хеликобактера, например С13-уреазный дыхательный тест или исследование кала на антигены хеликобактера, чтобы подтвердить или опровергнуть положительный результат.

— Всегда ли положительный анализ говорит о необходимости лечения? В каких случаях хеликобактер не лечат?
— Раньше считалось, что лечение хеликобактера следует проводить, только если имеются клинические проявления заболевания. Сейчас в связи с выявлением существенной роли хеликобактера в развитии рака желудка лечение рекомендуют проводить всем больным с хеликобактерной инфекцией.
В некоторых странах, в частности, Японии, лечение хеликобактера проводится всем больным бесплатно. При этом тем людям, которые отказываются лечиться от хеликобактера, при развитии у них рака желудка не оплачивают страховку.
У лиц с язвами желудка и двенадцатиперстной кишки санация хеликобактера приводит к уменьшению появления новых язв в три раза.
Лечение хеликобактера НЕ проводят:
- больным с аллергией и/или непереносимостью препаратов, предназначенных для лечения хеликобактера;
- тем, у кого все схемы лечения оказались неэффективными;
- отказывающимся от лечения пациентам.
На мой взгляд, больным с хроническим гастритом, у которых имеются лишь незначительные изменения слизистой оболочки желудка, от лечения можно временно воздержаться.
Лечение детей не проводят: существует большая вероятность повторного заражения из-за нахождения в детском коллективе и развития ряда побочных реакций, особенно при повторном лечении. Для детей желательно выделение отдельной посуды и соблюдение правил личной гигиены.

— Какое лечение назначается?
— Излечиться от хеликобактера полностью возможно только при назначении антибиотиков и блокаторов протоновой помпы (антисекреторных лекарственных средств — прим. ред.), усиливающих эффект антибиотиков, в ряде случаев в сочетании с препаратами висмута.
В последнее время выявлено бактерицидное действие некоторых пробиотиков в отношении хеликобактера.
Например, существует препарат, содержащий инактивированные бактерии пробиотического штамма Lactobacillus reuteri. Однако подобные препараты полностью от хеликобактера не излечивают.
— Должны ли параллельно лечиться домашние? Может ли такое быть, что у одного из членов семьи есть хеликобактер, а у остальных — нет?
— Да, лечение взрослых членов семьи при наличии у них хеликобактера должно проводиться, детям из-за указанных выше причин — нет. При этом наличие хеликобактера у всех членов одной семьи необязательно. Это зависит от индивидуальной резистентности организма к бактерии. В исследованиях и клинической практике неоднократно были случаи, когда хеликобактер не обнаруживался у отдельных членов семьи. Поэтому лечению всегда должны предшествовать анализы.
Читайте также:

