Плесневые грибы паразиты человека
Обновлено: 13.05.2024
По данным научных публикаций последних лет, на фоне затянувшейся пандемии COVID-19 отмечается тенденция к росту грибковых осложнений как в острый период, так и после выздоровления от коронавирусной пневмонии. Особенно если заболевание протекало в тяжелой форме и пациент долго лечился в стационаре.

Михаил Анатольевич, почему именно в период пандемии COVID-19 обострилась проблема инвазивных микозов?
На самом деле эта проблема всегда чрезвычайно актуальна для некоторых категорий пациентов, состояние которых связано с иммуносупрессией. В частности, это пациенты с онкологическими, гематологическими заболеваниями, после трансплантации гемопоэтических стволовых клеток (ГСК) или органных трансплантаций, страдающие сахарным диабетом 1-го и 2-го типа, перенесшие обширные хирургические вмешательства, длительно находящиеся в ОРИТ с центральным венозным катетером, на ИВЛ.
В таких случаях всегда есть риск бактериальных и грибковых осложнений. Обычно вначале развивается бактериальная инфекция, которую начинают лечить антибиотиками, после чего происходит присоединение грибковой микрофлоры. Все это характерно и для пациентов с COVID-19, тяжелые формы которого связаны с нарушением местных и системных механизмов иммунной защиты. Усугубляет ситуацию неадекватное назначение антибиотиков и системных глюкокортикостероидов (ГКС).
Какие именно виды грибковой микрофлоры становятся причиной инвазивных микозов?
На первом месте дрожжевые грибы преимущественно рода Candida, и это далеко не самый трудный вариант в плане диагностики и лечения, главное вовремя выявить и быстро назначить адекватную антимикотическую терапию. Несколько реже встречаются глубокие поражения плесневыми грибами, как правило рода Aspergillus. Однако в период пандемии COVID-19 появляется все больше публикаций о возрастании удельного веса плесневых грибов в структуре системных микозов.
Предрасполагающим фактором, очевидно, является повреждение вирусом SARS-CoV-2 легочного эпителия, что облегчает проникновение плесневой микрофлоры в легкие, поскольку заражение грибами рода Aspergillus происходит в основном ингаляционным путем при вдыхании спор.
Мукормикозы . это весьма агрессивные, быстро развивающиеся инфекции с поражением внутренних органов и тканей, высокой летальностью.
А почему в Индии было так много случаев поражений глаз, что некоторым пациентам пришлось даже удалять органы зрения?
Это уже были далеко зашедшие состояния, когда грибной мицелий пророс физиологические пазухи черепа и орбиту глаза. Все это в случае мукоровых грибов происходит очень быстро в течение 2–3 недель, они способны прорастать сквозь любую ткань, включая кость. Если на такой стадии не удалить глаз, то идет распространение в головной мозг и гибель пациента.
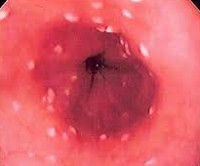
Клинические проявления при заражении мукоровыми грибами разнообразны. Чаще всего это риноцеребральный мукормикоз с поражением гайморовых, фронтальных и орбитальных пазух черепа, перфорацией неба и носовой перегородки, орбиты, параличом лицевых мышц. Инвазия гриба в организм человека также приводит к некрозу тканей, что визуально выглядит в виде поражений черного цвета. В тяжелых случаях системного мукормикоза диссеминированные некротические поражения могут затрагивать практически все внутренние органы, с летальностью 100 %.
При легочном мукормикозе наблюдаются прогрессивное множественное появление инфильтратов в легких, выраженная гипертермия, мокрота с кровью, прогрессирующая пневмония. Летальность при легочной форме составляет до 65 %. Встречаются также поражения ЖКТ (с развитием некротических язв, перфорацией кишечника и перитонитом) и кожных покровов (с изъязвлениями, глубокими абсцессами, черными некротическими поражениями).
Опасен ли человек с мукормикозом для окружающих?
Нет. Заражение мукоровыми грибами (мукормицетами), как и другими плесневыми грибами, может произойти ингаляционным путем при вдыхании спор или при приеме в пищу пораженных мукоровой плесенью продуктов, в редких случаях — через поврежденные кожу или слизистые оболочки. Причем вероятность развития заболевания напрямую зависит от состояния иммунитета.
У больного мукормикозом даже при выраженных поражениях не происходит такого бурного роста и созревания мицелия, чтобы в окружающую среду выделялись споры гриба, поэтому нельзя сказать, что он может стать источником заражения для окружающих, за исключением каких-то уж совсем казуистических случаев.
Резкий рост инвазивного мукормикоза этим летом в Индии неслучайно совпал именно с ростом и пиком заболеваемости COVID-19 в этой стране. Сошлись сразу несколько факторов: ослабленные люди с COVID-19 и после выздоровления, жара, мягкий влажный климат, в котором плесневые грибы чувствуют себя вольготно, и особенности культуры, бытовых условий и образа жизни в данной стране.
Вы имеете в виду несоблюдение санитарных норм и правил?
Около 8 лет назад, задолго до пандемии COVID-19, мне пришлось побывать в служебной командировке в Индии. С коллегами из Центра экспертиз и испытаний в здравоохранении и Республиканского центра гигиены, эпидемиологии и общественного здоровья мы посетили завод по производству медицинского оборудования в городе Хайдарабад, чтобы на месте проинспектировать условия производства, а также посмотреть, как это оборудование применяется в медицинской практике. На заводе все было отлично, как и в гостинице, где мы остановились, а вот от остального я (а моя квалификация по диплому — врач-гигиенист-эпидемиолог) испытал культурный шок.
Скопление людей, мотоколясок при отсутствии правил дорожного движения, в 30-градусную жару уличные торговцы продают с деревянных лотков сырое куриное мясо, вдоль дорог лежит мусор, некоторые люди живут в настоящих лачугах, готовят еду и спят на улице, порой просто на земле. В центре города расположено большое озеро ядовито-зеленого цвета, в котором не рискуют купаться даже местные жители. Очень запомнились обезьяны, которые свободно бегали по деревьям возле нашей гостиницы.
Расположенный в городе Институт медицинских наук тоже удивил своими контрастами. Это и обшарпанные стены и потолки с обваливающейся штукатуркой, обилие переплетенных электропроводов, мебель и лифтовое оборудование из прошлого века, и в то же время много вполне современной медицинской техники. К слову, лабораторные исследования там проводились на вполне достойном уровне. В целом же индийцы очень добродушные и общительные люди, оказавшие нам радушный прием.

Михаил Черновецкий в лаборатории Института медицинских наук города Хайдарабад (Индия, 2012).
Мукоровые грибы представляют опасность только для стран с жарким влажным климатом?
В природных условиях мукоровые микромицеты широко распространены по всему миру, в большинстве случаев это сапрофитные микроорганизмы, находящиеся на омертвевших клетках растений, в почве, компосте, остатках пищи. При этом в ряде стран мукоровые грибы используются в местной кухне.
Всего в настоящее время описано свыше 867 разновидностей мукоровых грибов (мукормицетов), среди которых наибольшее этиологическое значение имеют Rhizopus oryzae (arrhizus) и Lichtheimia corymbifera.

Дыня с колониями Rhizopus orysae.
Встречаются ли эти опасные разновидности плесневых грибов в Беларуси?
Высеваний из крови плесневой микрофлоры за это время было 19, в том числе у одного пациента это был Mucor spp. и у одного Rhizopus spp., остальные преимущественно Fusarium spp. и несколько аспергилл. Если же взять бронхоальвеолярный лаваж, биоптаты бронхов и легких, то процентное соотношение другое: примерно в 60 % случаев высевались плесневые грибы (в том числе аспергиллы и мукормицеты), а в 40 % — дрожжевая флора. Сейчас эти данные уточняются и готовятся к публикации.
Как выглядит эта плесень в окружающей среде? Она опасна только для людей с ослабленным иммунитетом?
Это как раз и может быть мукоровая плесень, хотя белый, постепенно чернеющий мицелий характерен и для других видов плесеней. При этом некоторые виды мукоровых грибов могут иметь и другой цвет колоний, например, голубовато-зеленоватого оттенка. Для точной диагностики необходимо вырастить в лаборатории на специальных питательных средах эту плесень и затем изучить под микроскопом ее микроморфологические свойства.

Помидор, пораженный мукоровой плесенью.
Различные виды плесеней, в том числе Aspergillus spp., часто встречаются в сырых прохладных помещениях, на отсыревших книгах и бытовых предметах, опавшей листве деревьев, поражают зерновые сельхозкультуры. В обычной жизни людям часто приходится вдыхать споры аспергилл, но иммунитет человека вполне справляется с этим.
Конечно, при многочасовой работе без респиратора с пораженным плесенью зерном на зернохранилище или при отмывании без средств индивидуальной защиты грибкового мицелия стен при ремонтных работах вполне возможно развитие аспергиллеза у человека и с нормальным иммунитетом, что проявляется в основном поражением легких. А вот для иммуносупрессивных лиц, в том числе находящихся в ОРИТ или недавно перенесших в тяжелой форме COVID-19, вдыхание большого количества спор Aspergillus всегда несет больший риск инвазивного микоза, который в короткий период времени может поразить легкие и другие внутренние органы. Об этом нужно помнить.
Есть ли какие-то клинические признаки, по которым врач может быстро заподозрить присоединение вторичной грибковой инфекции и развитие инвазивного микоза?
Когда на фоне лечения инфекционного заболевания с применением антибактериальной терапии состояние пациента не улучшается, держится упорная лихорадка, то обязательно нужно задуматься о вероятности присоединившейся грибковой микрофлоры. Чтобы исключить эти подозрения, необходимо выполнить забор крови и ее посев с целью выделения грибковой гемокультуры.
В нашем центре, учитывая контингент пациентов, гипертермия сразу является поводом для исследования на наличие в крови возбудителей инфекций, а назначение антибиотиков проводится строго по клиническим протоколам с учетом антибактериальной чувствительности. Такой принцип действует и при назначении противогрибковой терапии — при помощи специальных тестов определяем минимальную ингибирующую концентрацию антимикотиков к выделенной грибковой микрофлоре.
Подробнее о том, как проводится лабораторная диагностика инвазивных микозов с применением как традиционных микробиологических исследований, так и дополнительных биомаркерных, масс-спектрометрических и молекулярно-генетических методов, смотрите здесь.
Микозы желудочно-кишечного тракта — патологические состояния, развившиеся вследствие поражения пищеварительных органов дрожжеподобными, плесневыми, диморфными грибами. Проявляются изменением вкуса, появлением налетов на видимых слизистых, диспепсией, жидким стулом, болевыми ощущениями разной локализации. Диагностируются с помощью эзофагогастродуоденоскопии, колоноскопии, электрогастрографии, микробиологического исследования биоптата, ИФА, РИФ, ПЦР. Для лечения используют антимикотики, пробиотики, иммуномодуляторы в сочетании с комплексной терапией основного заболевания, осложнившегося грибковой инфекций.
МКБ-10
Общие сведения

Причины микозов желудочно-кишечного тракта
Возбудителями микотической инфекции органов ЖКТ становятся плесневые, дрожжеподобные, диморфные грибы, в большинстве случаев являющиеся естественными комменсалами человеческого организма. 9 из 10 микозов пищеварительного тракта провоцируется Candida albicans — условно-патогенным микроорганизмом, который высеивается у 65-70% населения. Микотический процесс также может развиться в результате размножения так называемых кандид non-albicans (С. guilliermondii, С. kefyr, С. krusei, С. tropicalis и др.). Некандидозные формы микотических желудочно-кишечных болезней, вызванные возбудителями бластомикоза, гистоплазмоза, кокцидиомикоза, криптококкоза, паракокцидиомикоза, споротрихоза, возникают при диссеминации грибов из очагов на коже, в респираторном тракте, других органах. Аспергиллез пищеварительных органов, интестинальный зигомикоз диагностируются редко, обычно – при наличии тяжелой сопутствующей патологии.
Манифестации микозов часто предшествуют другие патологические состояния, способствующие патологической активации условно-патогенной флоры за счет снижения местной защитной реакции слизистой ЖКТ, угнетения иммунных сил организма. Специалисты в сфере гастроэнтерологии и микологии выделяют следующие предпосылки к развитию желудочно-кишечного микотического заболевания:
- Физиологическая иммунная недостаточность. Естественное снижение иммунитета наблюдается у беременных, связано с необходимостью поддержания гестации. Незрелость иммунной системы характерна для новорожденных, риск инфицирования возрастает при недоношенности и наличии генитального кандидоза у матери. В пожилом возрасте отмечается инволютивное угасание защитных сил.
- Патологический иммунодефицит. Несостоятельность иммунной системы лежит в основе ВИЧ-инфекции и ее клинически выраженной формы — СПИД. Нарушения иммунитета отмечаются при дисплазии тимуса, других первичных иммунодефицитах, онкогематологических и лимфопролиферативных болезнях (лейкозах, лимфогранулематозе, неходжкинских лимфомах), сахарном диабете, голодании.
- Ятрогенные факторы. Иммунная функция угнетается при использовании кортикостероидов, цитостатиков, других химиопрепаратов у пациентов, перенесших трансплантацию органа, принимающих лечение по поводу онкопатологии, ревматоидного артрита, СКВ, гломерулонефрита, других системных болезней. Развитию микозов способствует антибактериальная терапия.
- Повреждения слизистой оболочки ЖКТ. Инвазии грибов более подвержены больные, страдающие атрофическим гастритом, ахалазией кардии, бульбитом, гастроэзофагеальной рефлюксной болезнью, дисбиозом, болезнью Крона, другой желудочно-кишечной патологией. Инфицирование облегчается при ожогах, травматизации эпителия зубными протезами, твердой пищей, интубационной трубкой.
Патогенез
Механизм развития микозов желудочно-кишечного тракта основан на нарушении баланса между реактивностью организма и факторами патогенности грибов — протеолитическими ферментами инвазии (коагулазой, каталазой, козеиназой, фосфолипазой), фибриллярными белковыми комплексами, эндотоксинами. При иммунодефиците уменьшается активность интраэпителиальных лимфоцитов, В-клеток кишечника, снижается цитотоксичность Т-клеточных элементов, нарушается секреция интерферона, фагоцитоз. В результате возбудители микозов быстро обсеменяют эпителий, легко проникают через собственную пластинку слизистой, агрегируются в пейеровых бляшках.
При травмах, химических ожогах, заболеваниях пищеварительных органов, изменениях кислотности и ферментативного состава желудочного, кишечного соков ситуация усугубляется наличием участков пораженной слизистой, замедленной регенерацией эпителиальных клеток, нарушением защитной функции естественных секретов. У пациентов, принимающих антибиотики, дополнительным патогенетическим фактором становится гибель облигатных микроорганизмов (кишечной палочки, аэробных лактобацилл, анаэробных бифидобактерий), которые являются естественными антагонистами грибов и сдерживают их неконтролируемое размножение.
Классификация
При систематизации форм микотической инфекции ЖКТ учитывают вид возбудителя, локализацию и распространенность патологического процесса. С учетом этиологии различают кандидоз, являющийся самым частым видом микозов, и редкие формы грибкового поражения (аспергиллез, криптококкоз, зигомицетоз и др.). При поражении одного отдела пищеварительного тракта говорят о фокальном микозе, при массивном распространении инфекции — об инвазивном диффузном, при отсутствии признаков инвазии — о микотическом дисбиозе. Наиболее часто используют классификацию микозов по локализации поражения, в соответствии с которой выделяют:
- Орофарингеальные поражения. В структуре микотических инфекций ЖКТ занимают первое место. Обычно встречаются у новорожденных и пациентов с иммунодефицитными состояниями (СПИД, гемобластозы).
- Микотический эзофагит. Диагностируется у 1-7% больных. Чаще развивается при сниженном иммунитете. Может протекать как в поверхностной, так и в эрозивной форме с повышенной кровоточивостью.
- Микотические поражения желудка. Составляют до 5,2% микозов ЖКТ. Выявляются при гастродуоденальных язвах, хронических гастритах. В ряде случаев определяются ассоциации грибов и хеликобактера.
- Микозы кишечника. Обычно возникают на фоне микотического поражения верхних отделов пищеварительного тракта. Как правило, диагностируются у больных, получающих массивную антибиотикотерапию.
- Микотическая инфекция гепатобилиарной системы. Осложняет дискинезию желчных путей, холестаз, холецистолитиаз, лямблиоз. Диагностируется редко, в том числе из-за низкой настороженности.
Симптомы микозов ЖКТ
Клиническая картина заболевания различна в зависимости от распространенности поражения. При орофарингеальной локализации микоза у пациента возникают боли во время приема пищи, неприятный привкус во рту, на слизистой оболочке щек и языка появляются белые налеты. Поражение пищевода и желудка характеризуется болью при глотании, дисфагией, изжогой, отрыжкой, тошнотой и рвотой, дискомфортом в эпигастральной области, снижением аппетита. При прогрессировании заболевания в процесс вовлекаются нижележащие отделы желудочно-кишечного тракта, что клинически проявляется диареей с примесями слизи и крови, болезненностью в левой подвздошной области. Возможны нарушения общего состояния: субфебрильная температура тела, слабость, снижение трудоспособности, резкое уменьшение веса.
Осложнения
Вследствие проникновения микроорганизмов из пищеварительного тракта в забрюшинную клетчатку могут возникать гнойно-воспалительные процессы — парапроктит, паранефрит, межкишечные или поддиафрагмальные абсцессы. У пациентов со сниженной реактивностью организма имеется склонность к генерализации микозов с развитием септицемии, приводящей к распространению грибков на другие органы. Наиболее опасно микотическое поражение гепатобилиарной системы, которое может вызывать желтуху и печеночную недостаточность. При тяжелом течении заболевания формируются некрозы стенки кишечника, иногда – с перфорацией. Возможны профузные желудочно-кишечные кровотечения, пенетрация язв в соседние органы.
Диагностика
Постановка диагноза микозов желудочно-кишечного тракта затруднена из-за полиморфности и неспецифичности клинической картины заболевания, которая сходна с проявлениями других патологий пищеварительной системы. Для диагностики грибкового поражения требуется комплексное обследование пациента. Наиболее информативными являются следующие методы:
В клиническом анализе крови наблюдаются неспецифические признаки воспалительного процесса: повышение СОЭ, незначительный лейкоцитоз, может выявляться снижение уровня эритроцитов и гемоглобина, что обусловлено кровотечениями. Для исследования структуры всех слоев стенки пищеварительного тракта выполняется эндоскопическая ультрасонография. Дифференциальная диагностика осуществляется с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), злокачественными новообразованиями, псевдомембранозным энтероколитом, желудочно-кишечным туберкулезом. Помимо осмотра гастроэнтеролога пациенту могут потребоваться консультации инфекциониста, онколога, фтизиатра.
Лечение микозов ЖКТ
Основными задачами являются терапия расстройства, вызвавшего активацию микотической флоры, и этиопатогенетическое воздействие на возбудителя грибковой инфекции. Лечение болезней пищеварительного тракта, иммунодефицитных и других патологических состояний проводят по протоколам соответствующих заболеваний. Для подавления грибкового процесса используют:
- Антимикотики. По результатам наблюдений, наиболее эффективной является терапия триазолами. Средства этой группы угнетают систему цитохрома P-450 и синтез эргостерола клеточных мембран, нарушая рост и репликацию кандид и криптококков. В качестве альтернативы с учетом особенностей возбудителя могут применяться полиены, аллиламины, эхинокандины.
- Пробиотики. Препараты, в которых содержатся непатогенные и нетоксигенные микроорганизмы, позволяют восполнить естественную микрофлору кишечника, нормализовать ее состав после проведенной антибактериальной терапии. Апатогенные бактерии стимулируют кишечный иммунитет, оказывают антагонистический эффект по отношению к грибам, нарушают их адгезию к слизистым.
При отсутствии противопоказаний проводится неспецифическая иммунотерапия стимуляторами естественного иммунитета (высокополимерные полисахаридные комплексы, регенеранты, производные пиримидина), Т- и В-лимфоцитов (полипептидные экстракты вилочковой железы, культур клеток костного мозга, селезенки). Возможно дополнительное использование растительных иммуномодуляторов, витаминно-минеральных комплексов.
Прогноз и профилактика
Исход болезни зависит от степени повреждения пищеварительных органов, состояния иммунной системы пациента, своевременности диагностики и терапии. Прогноз сомнительный при генерализации процесса и наличии тяжелых сопутствующих заболеваний. Для предупреждения развития микозов необходимо не допускать неоправданного применения антибактериальных средств, назначать профилактические курсы противогрибковых препаратов при длительном лечении цитостатиками, кортикостероидами, другими медикаментами с иммунодепрессорным эффектом, осуществлять диспансерное наблюдение за пациентами с иммунодефицитом.
2. Грибковые поражения желудочно-кишечного тракта/ Омаров Т.Р., Омарова Л.А.// Русский медицинский журнал – 2016 - №11.
3. Микозы пищеварительного тракта (обзор)/ Лесовой В.С., Липницкий А.В., Очкурова О.М.// Проблемы медицинской микологии – 2004 – Т.6, №2.
Кандидоз кишечника – инфекционное поражение пищеварительного тракта, вызванное собственной грибковой флорой пациента (Candida spp.) на фоне значительного ослабления иммунитета. Клинические проявления кандидоза кишечника варьируют в зависимости от формы заболевания: разжижение стула, повышенный метеоризм, неопределенные боли в животе, язвенный колит и грибковый сепсис. Диагноз ставится на основании эндоскопического исследования, гистологического и культурального анализа биоптатов, кала. Лечение включает три основных направления: назначение антимикотиков, нормализацию микрофлоры кишечника и коррекцию иммунного статуса пациента.

Общие сведения
Кандидоз кишечника – грибковое поражение слизистой оболочки пищеварительного тракта. Является актуальной проблемой современности, так как диагностика и определение критериев данного заболевания представляют сложность для многих клиницистов. Связано это с повсеместной распространенностью грибов рода Candida, в том числе и в организме здоровых людей (носительство грибов рода Candida в кишечнике присуще 80% населения). Инвазивный кандидоз кишечника практически никогда не встречается у людей с нормально функционирующим иммунитетом, почти всегда это оппортунистическая инфекция, связанная с иммунным дисбалансом организма.
Кроме того, для многих специалистов бывает достаточно сложно дифференцировать транзиторное кандидоносительство и неинвазивный кандидоз кишечника (именно он составляет подавляющее большинство всех клинических случаев кандидоза пищеварительной системы). Разграничить два этих состояния возможно только при наличии современного диагностического оборудования. Для установления правильного диагноза необходимо наличие трех диагностических критериев: выявление одного или нескольких факторов риска, эндоскопические признаки кандидоза кишечника, положительный результат культурального исследования. Таким образом, тактика назначения антимикотиков при первом обнаружении в посевах грибов рода Candida, без дальнейшего обследования, является ошибочной.

Причины кандидоза кишечника
Специалисты в области гастроэнтерологии выделяют две патогенетические формы кандидоза кишечника – инвазивную и неинвазивную. В клинической практике чаще встречается неинвазивный кандидоз кишечника на фоне дисбактериоза и смешанной кишечной инфекции (грибково-бактериальной, грибково-протозойной и др.). Висцеральная форма развивается на фоне выраженной нейтропении (практически полное отсутствие нейтрофильных лейкоцитов) и поздних стадий СПИДа.
Факторы риска
Для формирования кандидоза кишечника необходимо наличие хотя бы одного из предрасполагающих факторов:
- физиологического снижения иммунитета (период новорожденности или пожилой возраст, сильный стресс, беременность);
- врожденного иммунодефицита (синдром Di George, Nezelof и др.);
- онкопатологии, особенно в период полихимиотерапии;
- аутоиммунных и аллергических заболеваний (усугубляет угнетение иммунитета лечение кортикостероидными гормонами);
- приема иммунодепрессантов после трансплантации органов;
- тяжелых эндокринных заболеваний, соматической патологии, требующей интенсивной терапии;
- длительного лечения антибактериальными препаратами резервного ряда;
- синдрома первичного иммунодефицита;
- выраженного дисбаланса питательных веществ в рационе (особенно недостатка белка и витаминов).
В клинической практике чаще встречается кандидоз кишечника, обусловленный сочетанием нескольких из перечисленных факторов.
Патогенез
При неинвазивной форме грибы рода Candida начинают неконтролируемо размножаться в просвете кишки, не проникая в толщу ее слизистой. При этом выделяются специфические грибковые токсины, образуются ядовитые продукты ферментации, оказывающие раздражающее действие на слизистую оболочку кишечника. Перечисленные токсические агенты провоцируют дальнейшее усугубление дисбиоза, формирование микотической аллергии, вторичного иммунодефицита.
Патогенез инвазивного кандидоза кишечника иной. При условии ослабления местного и общего иммунитета грибы рода Candida интимно прикрепляются к эпителию кишечника (они имеют тропность к плоскому многослойному эпителию), затем внедряются в его толщу, трансформируясь в нитчатую форму. При наличии выраженной супрессии клеточного иммунитета Candida проникают в кровоток и распространяются по организму, вызывая висцеральный кандидоз (поражение печени, поджелудочной железы).
Симптомы кандидоза кишечника
Кандидоз кишечника встречается в трех основных клинических формах: инвазивный диффузный, инвазивный фокальный и неинвазивный. Критериями диагностики инвазивного диффузного кандидоза кишечника являются тяжелое состояние пациента на фоне выраженной интоксикации, повышение температуры тела, сильная боль в животе, диарея, примесь крови в стуле, системные проявления микоза (поражение печени, поджелудочной железы, селезенки, желчного пузыря и др.). Если эта форма кандидоза кишечника является случайной находкой во время обследования по поводу других заболеваний, в первую очередь следует думать о дебюте СПИДа или сахарного диабета. Инвазивный диффузный кандидоз кишечника не характерен для людей с нормально функционирующей системой иммунитета.
Инвазивный фокальный кандидоз кишечника может осложнять течение язвенной болезни двенадцатиперстной кишки, неспецифического язвенного колита. Заподозрить данную форму кандидоза можно у пациентов с упорным и затяжным течением фонового заболевания, не поддающегося стандартной терапии. Для этого варианта микоза характерна локальная инвазия нитчатой формы Candida в местах нарушенной эпителизации (на дне язв кишечника). При этом в окружающих тканях, других отделах кишки друзы грибов не выявляются. Клиническая картина соответствует основному заболеванию, а псевдомицелий обнаруживается случайно при гистологическом исследовании биоптатов.
Неинвазивный кандидоз кишечника является наиболее распространенной формой данного заболевания. Эта патология не ассоциируется с проникновением грибов в толщу кишечной стенки, а связана с массивным размножением Candida в просвете кишки. При этом выделяется огромное количество токсичных метаболитов, которые оказывают как местное, так и общее резорбтивное действие. Сегодня установлено, что неинвазивный кандидоз составляет примерно треть всех случаев дисбиоза кишечника. Клинически неинвазивный кандидоз кишечника протекает на фоне удовлетворительного состояния пациента, сопровождается умеренными явлениями интоксикации, дискомфортом в животе, метеоризмом, неустойчивым стулом. Часто у таких больных обостряются различные аллергические заболевания. Эту форму кандидоза зачастую путают с синдромом раздраженного кишечника.
Диагностика
Диагностика кандидоза кишечника затрудняется отсутствием типичных клинических признаков, а также достаточно специфичных и чувствительных методов выявления грибов рода Candida в образцах тканей и кале. В общем анализе крови при тяжелых формах заболевания определяется уменьшение количества лейкоцитов, лимфоцитов, эритроцитов. Обязательна консультация врача-эндоскописта для выбора оптимального метода исследования кишечника. Во время эндоскопии обычно обнаруживают неспецифические признаки поражения слизистой, поэтому решающее значение в постановке диагноза имеет эндоскопическая биопсия и морфологическое исследование биоптатов.
Трудности диагностики заключаются в том, что псевдомицелий грибов можно выявить не во всех пробах материала, поэтому достаточно часто встречаются ложноотрицательные результаты. Визуально при диффузном инвазивном кандидозе кишечника определяются признаки язвенно-некротического поражения слизистой, а при неинвазивном – катаральное воспаление. Диагностическим критерием инвазивного кандидоза кишечника служит наличие кандидозного псевдомицелия в биоптатах и отпечатках слизистой оболочки кишки.
Всем пациентам с грибковым поражением кишечника обязательно проводится анализ кала на дисбактериоз, бактериологическое исследование кала. Чаще всего эти анализы выявляют смешанную флору: не только грибы рода Candida, но и кишечную палочку, клебсиеллы, стафилококки и др. Выявление более 1000 колониеобразующих единиц на грамм патологического материала свидетельствует в пользу кандидоза кишечника и исключает носительство грибковой флоры. Основной задачей культурального исследования является установление вида возбудителя, определение чувствительности выделенной микрофлоры к антимикотикам.
Лечение кандидоза кишечника
Консультация гастроэнтеролога при кандидозе кишечника позволяет выявить факторы риска данного заболевания, определить объем необходимых исследований. Так как кандидоз кишечника не имеет специфических клинических признаков, заподозрить эту патологию бывает достаточно сложно. При наличии лабораторных свидетельств кандидоза кишечника выбор тактики лечения зависит от клинического варианта, наличия сопутствующей патологии, переносимости антимикотических препаратов. Обязательными звеньями лечебного процесса при кандидозе кишечника являются: коррекция фонового заболевания, приведшего к снижению иммунитета и активации грибковой флоры; назначение целевого противогрибкового средства; модуляция иммунитета.
Пациенты с диффузной инвазивной формой кандидоза кишечника госпитализируются в стационар. Препаратами выбора для инвазивных микозов являются азольные антимикотики (кетоконазол, флуконазол, итраконазол и пр.), которые активно всасываются из кишечника и оказывают системное действие. Начинают лечение обычно с введения амфотерицина В, затем переходят на терапию флуконазолом.
Для эрадикации грибковой флоры при неинвазивных формах кандидоза кишечника используют противогрибковые препараты нерезорбтивного действия – они плохо всасываются слизистой оболочкой кишки и оказывают сильное местное действие. Нерезорбтивные полиеновые антимикотики имеют ряд преимуществ – у них практически нет побочных действий, они не угнетают нормальную микрофлору кишечника, не вызывают привыкания. К полиеновым препаратам относят натамицин, нистатин. Так как в патогенезе неинвазивного кандидоза имеют значение состояние дисбиоза и смешанная флора, обязательно назначают противомикробные препараты, эубиотики. В качестве симптоматического лечения применяют пищеварительные ферменты, сорбенты, спазмолитики и анальгетики.
Прогноз и профилактика
При диффузной инвазивной форме кандидоза кишечника прогноз серьезный, так как она может приводить к генерализации процесса. Прогноз при инвазивном кандидозе кишечника значительно отягощается наличием тяжелых фоновых заболеваний. При остальных вариантах заболевания прогноз благоприятный при своевременном начале лечения.
Профилактика кандидоза кишечника заключается в устранении предрасполагающих к этой патологии факторов; лечении заболеваний пищеварительного тракта, приводящих к дисбиозу. Для поддержания нормальной микрофлоры кишечника следует разнообразно питаться, ограничивая содержание простых углеводов, употреблять достаточное количество клетчатки. Пациенты, входящие в группу риска по развитию кандидоза органов ЖКТ (ВИЧ, тяжелая эндокринная патология, полихимиотерапия, лечение кортикостероидными гормонами и пр.), требуют пристального внимания и регулярного обследования.

Видеоурок расскажет учащимся о многообразии плесневых грибов и грибов – паразитов. Будут рассмотрены особенности их строения. Учащиеся узнают о том, как можно использовать эти грибы в хозяйстве и медицине, что хлебная выпечка и квас получаются благодаря дрожжам.
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Плесневые грибы и дрожжи. Грибы – паразиты"
Многие грибы развиваются на отмерших частях растений и животных. Там они образуют плесени — налёты разнообразной окраски: серой, зелёной, жёлтой, чёрной. Поэтому такие грибы называются плесневыми грибами. Плесень представляет собой их мицелий и споры. Плесневые грибы приводят в негодность пищевые продукты (хлеб, варенье), изделия из кожи, картины, книги.

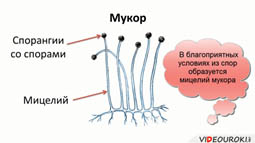
Если положить хлеб на несколько дней в тёплое и влажное место, на нём появляется белый пушистый налёт, который через некоторое время темнеет. Это плесневый гриб — мукор.

Этот гриб часто поселяется также на фруктах, овощах, почве. Мицелий мукора не разделён перегородками на клетки и сильно ветвится. В цитоплазме этой огромной клетки находится много ядер. Размножается мукор чаще всего участками мицелия и спорами, реже половым способом. Споры образуются внутри шаровидных спорангиев, которые хорошо заметны невооруженным глазом в виде буроватых или чёрных точек. При разрыве спорангиев микроскопические споры распространяются ветром. В благоприятных условиях из спор вновь образуется мицелий мукора.
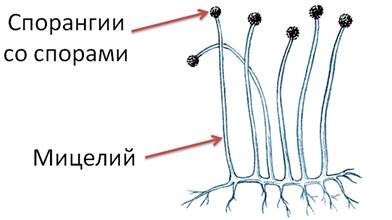
Пеницилл — также широко распространённый плесневый гриб. Он живёт на многих продуктах (хлебе, сыре, варенье), заложенных на хранение плодах и овощах. Она может появляться также на влажной одежде, обуви, бумаге и сырых стенах комнат. Плесень, вызванная пенициллом, чаще всего имеет зеленоватую окраску.
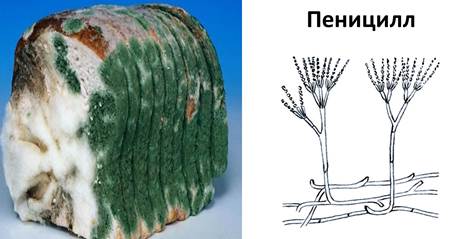
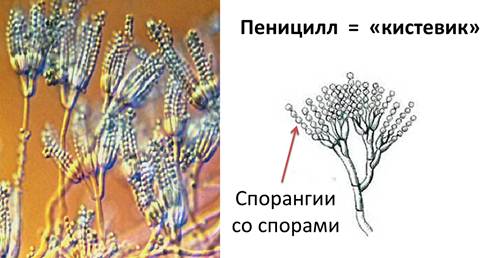
Пеницилл образует особое вещество, убивающее многие бактерии, — антибиотик пенициллин. Это вещество применяется для лечения многих болезней, вызванных бактериями (воспаление лёгких, ангина).
Многие плесневые грибы образуют вещества, вызывающие тяжёлые отравления человека и животных. Поэтому заплесневевшие продукты нельзя употреблять в пищу.
К особой группе грибов относятся дрожжи. Они живут там, где есть сахаристые вещества. Тело дрожжей — одиночные клетки.
Размножаются дрожжи чаще всего почкованием. При этом на клетке образуется выпячивание — почка. Она растёт и постепенно отделяется от материнской клетки. Почкование происходит быстро и новые клетки не успевают отделиться от материнской. В результате этого получаются короткие ветвящиеся цепочки клеток.
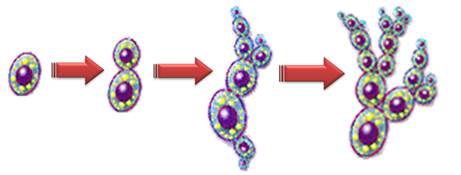
В сахаристых средах дрожжи осуществляют брожение, при котором образуется этиловый спирт и выделяется углекислый газ. Человек использует дрожжи для приготовления теста в хлебопечении, а также в виноделии и пивоварении.
Большую группу грибов составляют грибы-паразиты. Они живут и питаются на растениях, других грибах, животных и человеке, вызывая болезни — микозы. Особенно большой вред грибы-паразиты наносят сельскому и лесному хозяйству.

Ещё одним грибом паразитом является головня. Головня может поражать хлебные злаки: пшеницу, овёс, ячмень, просо, кукурузу. Вместе с зерном споры попадают в землю и прорастают в нити грибницы. Грибница проникает в проростки зерновых растений и растёт внутри стебля, питаясь его соками. Ко времени цветения злаков грибница головнёвого гриба достигает колоса. Здесь она сильно разрастается, образует массу спор, разрушает зерновки и превращает их в чёрную пыль. Колоски становятся похожи на обуглившиеся головешки.

На некоторых зерновых культурах поселяется гриб спорынья. У поражённых растений здоровые зерновки превращаются в ядовитые чёрно-фиолетовые рожки, плотные сплетения нитей грибницы спорыньи. Попав с мукой в пищу, они могут вызвать тяжёлое отравление.

К грибам-паразитам растений относятся некоторые трутовые грибы, или трутовики. Их споры попадают на повреждённые части живых деревьев. Из спор образуется мицелий. Плодовые тела трутовиков появляются значительно позже. Они, как правило, крупные, в виде копыт или наростов, одиночные или расположенные группами, твёрдые, деревянистые. Наиболее часто встречаются трутовики настоящий и ложный, корневая губка, чага.

Для борьбы с грибами, паразитирующими на растениях, применяют фунгициды — яды, убивающие грибы. Фунгицидами обрабатывают семена перед посевом, опрыскивают растения в период их роста.
Читайте также:

